-
为了说明影响化学反应快慢的因素,甲、乙、丙、丁4位同学分别设计了如下4个实验,你认为结论不正确的是( )
A. 将形状大小均相同的镁条和铝条与相同浓度的盐酸反应时,两者速率一样
B. 相同条件下等质量的块状和粉末状大理石与相同浓度的盐酸反应,粉末状反应快
C. 常温下将浓硝酸分别放在暗处和强光下,发现光照可加快浓硝酸的分解
D. 两支试管中分别加入浓度、体积均相同的双氧水,其中一支试管中再加入少量二氧化锰,产生氧气的快慢不同
高二化学单选题中等难度题查看答案及解析
-
为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位同学分别设计了如下四个实验,你认为结论不正确的是。( )
A.将铜片放入稀硫酸中,无现象。若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气生成
B.将除去氧化膜的相同大小、相同质量的镁条和铝条与相同浓度盐酸反应,前者速率大于后者
C.两支试管中分别加入根同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同
D.相同条件下等质量的块状和粉末状大理石与相同浓度盐酸反应时,粉末状的反应速率快
高二化学单选题中等难度题查看答案及解析
-
为了探究影响化学反应速率的因素,4位同学分别设计了下列4个实验,其中结论不正确的是
A. 将大小、形状相同的镁条和铝条与相同浓度、相同温度下的盐酸反应时,两者快慢相同
B. 盛有相同浓度双氧水的两支试管,一支加入MnO2放在冷水中,一支直接放在冷水中,前者反应快
C. 将浓硝酸分别放在冷暗处和强光下,发现强光下的浓硝酸分解得快
D. 升高温度,H2O2的分解速率加快,原因是反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多
高二化学单选题中等难度题查看答案及解析
-
为了探究影响化学反应速率的因素,4位同学分别设计了下列4个实验,其中结论不正确的是
A.将大小、形状相同的镁条和铝条与相同浓度、相同温度下的盐酸反应时,两者快慢相同
B.盛有相同浓度双氧水的两支试管,一支加入MnO2放在冷水中,一支直接放在冷水中,前者反应快
C.将浓硝酸分别放在冷暗处和强光下,发现强光下的浓硝酸分解得快
D.升高温度,H2O2的分解速率加快,原因是反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多
高二化学选择题中等难度题查看答案及解析
-
为了研究影响化学反应速率的因素,甲、乙、丙、丁四位学生分别设计了如下四个实验,你认为不正确的是
A.100 mL 2 mol·L-1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
B.将相同大小、形状的铝条与稀硫酸和浓硫酸反应时,稀硫酸产生氢气快
C.将氢气和氯气的混合气体分别放在冷暗处和强光照射下,会发现光照下有氯化氢生成
D.两支试管中分别加入相同浓度相同体积的双氧水,其中一支试管再加入少量二氧化锰,产生氧气的快慢不同
高二化学单选题中等难度题查看答案及解析
-
为了研究影响化学反应速率的因素,甲、乙、丙、丁四位学生分别设计了如下四个实验,你认为不正确的是
A.100 mL 2 mol·L-1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
B.将相同大小、形状的铝条与稀硫酸和浓硫酸反应时,稀硫酸产生氢气快
C.将氢气和氯气的混合气体分别放在冷暗处和强光照射下,会发现光照下有氯化氢生成
D.两支试管中分别加入相同浓度相同体积的双氧水,其中一支试管再加入少量二氧化锰,产生氧气的快慢不同
高二化学选择题中等难度题查看答案及解析
-
下列列举的四个选项是4位同学发表的观点,你认为不正确的是
A.化学反应进行的快慢及其影响因素是化学反应速率理论研究的问题
B.化学反应的限度是化学平衡理论研究的问题
C.化学反应速率理论是研究怎样提高原料转化率
D.怎样使原料尽可能多转化为产品是化学平衡理论研究的问题之一
高二化学选择题中等难度题查看答案及解析
-
实验室用Zn与稀H2SO4反应来制取氢气,常加少量CuSO4来加快反应速率。为了研究CuSO4的量对H2生成速率的影响,某同学用实验比较法设计了如下实验方案,将表中所给的试剂按一定体积混合后,分别加入四个盛有相同大小的Zn片(过量)的反应瓶(甲、乙、丙、丁)中,收集产生的气体,并记录收集相同体积的气体所需的时间。
实验
试剂
甲
乙
丙
丁
4 mol·L-1H2SO4/mL
20
V1
V2
V3
饱和CuSO4溶液/mL
0
2.5
V4
10
H2O/mL
V5
V6
8
0
收集气体所需时间/s
t1
t2
t3
t4
下列说法正确的是
A.t1 < t2 < t3 < t4 B.V4=V5=10 C.V6=7.5 D.V1<V2<V3<20
高二化学选择题简单题查看答案及解析
-
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:甲同学利用Al、Fe、Mg和2 mol/L的稀硫酸,设计实验方案研究影响反应速率的因素。
研究的实验报告如下表:
实验步骤
现象
结论
①分别取等体积的2 mol/L的硫酸于试管中;②分别投入大小、形状相同的Al、Fe、Mg
反应快慢:Mg>Al>Fe
反应物的性质越活泼,反应速率越快
(1)该同学的实验目的是_______________________;要得出正确的实验结论,还需控制的实验条件是________。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用下图装置同温下进行定量实验,用大小形状相同的Fe分别和0.5 mol/L及2 mol/L的足量稀H2SO4反应,通过________可以说明浓度对化学反应速率的影响。
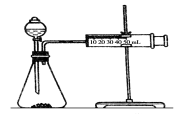
实验二:同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
P4(s,白磷)+5O2(g)===P4O10(s) ΔH1=-2983.2 kJ·mol-1①
P(s,红磷)+5/4O2(g)===1/4 P4O10(s) ΔH2=-738.5 kJ·mol-1②
则白磷转化为红磷的热化学方程式为 。相同状况下,能量状态较低的是________;白磷的稳定性比红磷________(填“高”或“低”)。)
高二化学实验题极难题查看答案及解析
-
19.下列说法正确的是
A.在“研究反应速率的影响因素”实验中:Na2S2O3+H2SO4=Na2SO4+S+SO2+H2O,可通过观察产生气泡的快慢来比较不同条件下该反应的速率大小
B.为了精确测定盐酸与氢氧化钠溶液反应的反应热,当两者混合后,立即读取温度计的读数,防止热量散失
C.将铁粉、碳粉、少量氯化钠和水混合放在塑料袋中搓揉,用手触摸会感觉到发热,袋里产生大量铁锈
D.酸碱中和滴定实验中,终点判断过迟,导致标准液滴多,只能重新滴定
高二化学选择题中等难度题查看答案及解析