-
实验室用Zn与稀H2SO4反应来制取氢气,常加少量CuSO4来加快反应速率。为了研究CuSO4的量对H2生成速率的影响,某同学设计了实验方案(见下表),将表中所给的试剂按一定体积混合后,分别加入四个盛有相同大小的Zn片(过量)的反应瓶(甲、乙、丙、丁)中,收集产生的气体,并记录收集相同体积的气体所需的时间。
实验
试剂
甲
乙
丙
丁
4 mol·L-1 H2SO4/mL
20
V1
V2
V3
饱和CuSO4溶液/mL
0
2.5
V4
10
H2O/mL
V5
V6
8
0
收集气体所需时间/s
t1
t2
t3
t4
下列说法正确的是( )
A. t1<t2<t3<t4 B. V4=V5=10 C. V6=7.5 D. V1<V2<V3<20
高二化学单选题中等难度题查看答案及解析
-
实验室用Zn与稀H2SO4反应来制取氢气,常加少量CuSO4来加快反应速率。为了研究CuSO4的量对H2生成速率的影响,某同学用实验比较法设计了如下实验方案,将表中所给的试剂按一定体积混合后,分别加入四个盛有相同大小的Zn片(过量)的反应瓶(甲、乙、丙、丁)中,收集产生的气体,并记录收集相同体积的气体所需的时间。
实验
试剂
甲
乙
丙
丁
4 mol·L-1H2SO4/mL
20
V1
V2
V3
饱和CuSO4溶液/mL
0
2.5
V4
10
H2O/mL
V5
V6
8
0
收集气体所需时间/s
t1
t2
t3
t4
下列说法正确的是
A.t1 < t2 < t3 < t4 B.V4=V5=10 C.V6=7.5 D.V1<V2<V3<20
高二化学选择题简单题查看答案及解析
-
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
(1)某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量CuSO4溶液可加快氢气 的生成速率。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。 请分析氢气生成速率下降的主要原因___________________________。
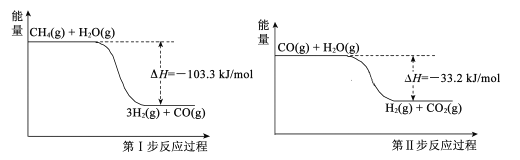
(2)用甲烷制取氢气的两步反应的能量变化如下图所示,则甲烷和水蒸气反 应生成二 氧化碳和氢气的热化学方程式是___________________________。
(3)科学家最近研究出一种环保,安全的储氢方法,其原理可表示为:NaHCO3
H2
HCOONa
H2O。下列有关说法正确的是_____________。
A.储氢、释氢过程均无能量变化
B.NaHCO3、HCOONa均具有离子键和共价键
C.储氢过程中,NaHCO3被氧化
D.释氢过程中,每消耗0.1 mol H2O放出2.24 L的H2
(4)Mg2Cu是一种储氢合金。350 ℃时,Mg2Cu与H2反应,生成MgCu2 和仅含一种 金属元素的氢化物(该氢化物中氢的质量分数为0.077)。Mg2Cu与H2反应的化学方程式为______________。
高二化学填空题困难题查看答案及解析
-
铝与过量的稀盐酸反应,为了加快反应速率,但是又不影响生成的氢气总量,可以采取的措施是( )
A.降低温度 B.加入适量的水
C.加入少量CuSO4溶液 D.加入浓度较大的盐酸
高二化学选择题简单题查看答案及解析
-
一定量铝片与过量的稀盐酸反应,为了加快反应速率,同时几乎不影响生成的氢气总量,不可以采取的措施是
A. 加热,升高溶液温度 B. 将铝片改为等质量的铝粉
C. 加入少量CuSO4溶液 D. 加入浓度较大的盐酸
高二化学单选题中等难度题查看答案及解析
-
过量的锌粉与一定量的稀盐酸反应,为了加快反应速率,但是又不影响生成的氢气总量,可以采取的措施是( )
A.加入适量的水
B.适当升高温度
C.加入少量CuSO4溶液
D.加入等体积的浓度较大的盐酸
高二化学选择题简单题查看答案及解析
-
100mL 2mol/L的硫酸和过量的锌反应,为了加快反应速率,但又不影响生成氢气的总量,可以采取的措施是
A.升高温度 B.加入少量的CuSO4溶液
C.改用纯度高的锌粒 D.改用小颗粒的锌粒
高二化学选择题简单题查看答案及解析
-
下列有关说法不正确的是( )
A. 实验室制取氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液
B. 铅蓄电池在放电过程中,负极和正极质量均增加
C. 在硫酸型酸雨地区,不纯的铜发生电化学腐蚀,正极反应为:O2+4e-+4H+=2H2O
D. 生铁发生吸氧腐蚀和析氢腐蚀的负极反应均为:Fe-2e- =Fe2+
高二化学选择题中等难度题查看答案及解析
-
下列有关说法不正确的是
A. 实验室制取氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液
B. 铅蓄电池在放电过程中,负极和正极质量均增加
C. 在硫酸型酸雨地区,不纯的铜发生电化学腐蚀,正极反应为:O2 + 4e- + 4H+ = 2H2O
D. 生铁发生吸氧腐蚀和析氢腐蚀的负极反应均为:Fe - 2e- = Fe2+
高二化学单选题中等难度题查看答案及解析
-
下列有关说法不正确的是
A.实验室制取氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液
B.为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解
C.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,则水电离的热化学方程式为:H2O(l)
H+(aq)+OH-(aq) ΔH= +57.3 kJ·mol-1
D.生铁发生吸氧腐蚀和析氢腐蚀的负极反应均为:Fe-2e- =Fe2+
高二化学选择题中等难度题查看答案及解析