N2和H2在催化剂表面合成氨气反应的能量变化如图,下列说法正确的是
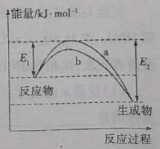
A.相同条件下,催化剂b的效果更好
B.使用催化剂,合成氨反应放出的热量减少
C.合成氨反应中,反应物断键吸收的能量大于生成物形成新键释放的能量
D.催化剂在吸附N2、H2时,催化剂与气体之间的作用力为化学键
高一化学单选题简单题
N2和H2在催化剂表面合成氨气反应的能量变化如图,下列说法正确的是

A.相同条件下,催化剂b的效果更好
B.使用催化剂,合成氨反应放出的热量减少
C.合成氨反应中,反应物断键吸收的能量大于生成物形成新键释放的能量
D.催化剂在吸附N2、H2时,催化剂与气体之间的作用力为化学键
高一化学单选题简单题
N2和H2在催化剂表面合成氨气反应的能量变化如图,下列说法正确的是

A.相同条件下,催化剂b的效果更好
B.使用催化剂,合成氨反应放出的热量减少
C.合成氨反应中,反应物断键吸收的能量大于生成物形成新键释放的能量
D.催化剂在吸附N2、H2时,催化剂与气体之间的作用力为化学键
高一化学单选题简单题查看答案及解析
工业合成氨反应在催化剂表面的反应历程及能量变化如图所示,下列说法正确的是( )
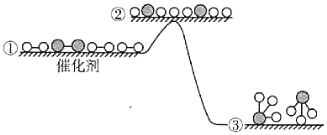
A.合成氨的正、逆反应的焓变相同
B.若使用催化剂,生成等量的NH3需要的时间更短
C.在该过程中,N原子和H原子形成了含有非极性键的氨气分子
D.合成氨反应中,反应物断键吸收能量大于生成物形成新键释放的能量
高一化学单选题中等难度题查看答案及解析
德国化学家F.Haber利用N2和H2在催化剂表面合成氨气而获得诺贝尔奖,该反应的微观历程及能量变化的示意图如下,用、
、
分别表示N2、H2、NH3,下列说法正确的是( )
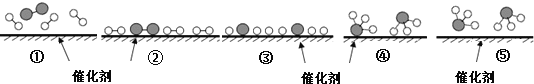
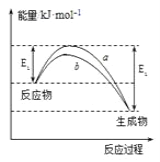
A. 合成氨反应中,反应物断键吸收能量大于生成物形成新键释放的能量
B. 催化剂在吸附N2、H2时,催化剂与气体之间的作用力为化学键
C. 在该过程中,N2、H2断键形成N原子和H原子
D. 使用催化剂,合成氨反应放出的热量减少
高一化学单选题中等难度题查看答案及解析
德国化学家F.Haber利用N2和H2在催化剂表面合成氨气而获得诺贝尔奖,该反应的微观历程及能量变化的示意图如下,用、
、
分别表示N2、H2、NH3,下列说法正确的是( )


A. 合成氨反应中,反应物断键吸收能量大于生成物形成新键释放的能量
B. 催化剂在吸附N2、H2时,催化剂与气体之间的作用力为化学键
C. 在该过程中,N2、H2断键形成N原子和H原子
D. 使用催化剂,合成氨反应放出的热量减少
高一化学单选题中等难度题查看答案及解析
N2和H2在催化剂表面合成氨的微观历程及能量变化的示意图如图所示,用、、
分别表示N2、H2、NH3,下列说法正确的是( )

A.使用催化剂时,合成氨的反应放出的热量减少
B.在该过程中,N2、H2 断键形成 N 原子和 H 原子
C.在该过程中,N原子和H原子形成了含有非极性键的NH3
D.合成氨反应中,反应物断键吸收的能量大于生成物形成新键释放的能量
高一化学单选题中等难度题查看答案及解析
N2和H2在催化剂表面合成氨的微观历程及能量变化的示意图如下,用、
、
分别表示N2、H2、NH3,下列说法正确的是( )


A.使用催化剂,改变了反应的途径,使合成氨反应放出的热量减少
B.该过程中,N2、H2吸收能量后断键形成N原子和H原子
C.该过程中,N原子和H原子形成含有非极性键的NH3分子
D.合成氨反应中,反应物断键吸收能量大于生成物形成新键释放的能量
高一化学单选题简单题查看答案及解析
N2和H2在催化剂表面合成氨的微观历程及能量变化的示意图如下,用、
、
分别表示N2、H2、NH3,下列说法正确的是( )
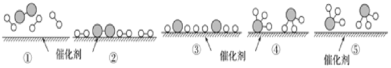

A.使用催化剂,改变了反应的途径,使合成氨反应放出的热量减少
B.该过程中,N2、H2吸收能量后断键形成N原子和H原子
C.该过程中,N原子和H原子形成含有非极性键的NH3分子
D.合成氨反应中,反应物断键吸收能量大于生成物形成新键释放的能量
高一化学单选题简单题查看答案及解析
合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
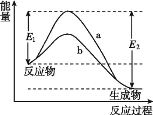
(1)德国化学家F·Haber利用N2和H2在催化剂表面合成氨气而获得诺贝尔奖,该反应的能量变化及微观历程的示意图如下,用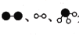 分别表示N2、H2、NH3。
分别表示N2、H2、NH3。

①该反应是____反应(填“吸热“或“放热”,其原因是反应物化学键断裂吸收的总能量_____(填“大于”或“小于”)生成物化学键形成放出的总能量。
②关于N2和H2在催化剂表面合成氨气的过程,下列说法正确的是________。
A.曲线b表示有催化剂时的能量变化情况
B.催化剂在吸附N2、H2时,催化剂与气体之间的作用力为化学键
C.在该过程中,N2、H2断键形成氮原子和氢原子
D.使用催化剂,使合成氨反应放出的能量增多
(2)一定温度下,向恒容的密闭容器中充入一定量的N2和H2发生反应,测得各组分浓度随时间变化如图所示。
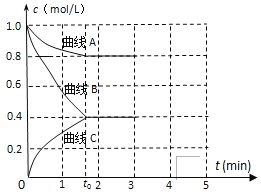
①表示c(N2)变化的曲线是_____(填“曲线A”或“曲线B”或“曲线C”)。
②0~t0时用H2表示的化学反应速率:v(H2)=_____ mol‧L-1‧min-1
③下列能说明该反应达到平衡状态的是______(填序号)。
a.容器中的压强不随时间变化
b.2c(H2)=3c(NH3)
c.容器中混合气体的密度不随时间变化
d.断裂3mol H-H键的同时断裂6molN-H键
(3)人们曾认为N2+3H2 =2NH3化学反应速率小,原材料利用率低,不可能用于工业化生产。化学家们不断地研究和改进该反应的条件,如催化剂、温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。下列反应条件的改变对反应速率的影响正确的是_______。
A.增大N2的浓度能加快反应速率
B.充入稀有气体增大压强能加快反应速率
C.升高温度能减慢反应速率
D.使用催化剂对反应速率无影响
高一化学原理综合题中等难度题查看答案及解析
工业上利用氮气与氢气合成氨气,关于该反应的说法正确的是( )
A. 其它条件不变时,增加N2的浓度能加快反应速率
B. 其它条件不变时,降低体系温度能加快反应速率
C. 使用催化剂不影响反应速率
D. 当N2和H2按体积比1:3混合时,N2和H2能100%转化为NH3
高一化学单选题中等难度题查看答案及解析
德国化学家 F.Haber 利用N2和H2在催化剂表面合成氨气而获得诺贝尔奖,该反应的微 观历程及能量变化的示意图如下,用 、
、  、
、 分别表示N2、H2、NH3,下列说法正确的是
分别表示N2、H2、NH3,下列说法正确的是
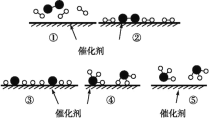

A.合成氨反应中,反应物断键吸收的能量大于生成物形成新键释放的能量
B.催化剂在吸附N2、H2时,催化剂与气体之间的作用力为化学键
C.在该过程中,N2、H2断键形成氮原子和氢原子
D.使用催化剂,合成氨反应放出的热量减少
高一化学单选题中等难度题查看答案及解析