-
十九大报告提出要对环境问题进行全面、系统的可持续治理。
回答下列问题:
(1)以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
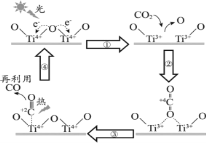
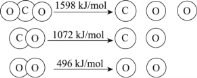
①上述过程中,能量的变化形式是由________转化为________。
②根据数据计算,分解1molCO2需________(填“吸收”或“放出”)________kJ的能量。
(2)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。
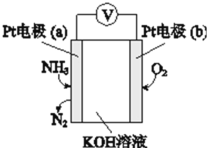
①Pt电极(a)为________极(填“正”或“负”);Pt电极(b)上的电极反应式为:________。
②该过程总反应的化学反应方程式为________,反应一段时间后,KOH溶液的浓度将________(填“增大”“减小”或“不变”)。
-
以 TiO2为催化剂的光热化学循环分解CO2 反应 ,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如下所示。

下列说法错误的是
A.过程①中吸收能量使钛氧键发生了断裂
B.该反应中,光能和热能转化为化学能
C.使用TiO2作催化剂可以提高化学反应速率
D.使用TiO2作催化剂可以减少分解CO2所需能量
-
以TiO2为催化剂的光热化学循环分解CO2反应,为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
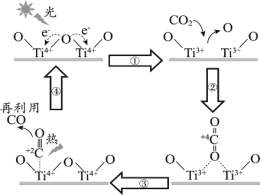
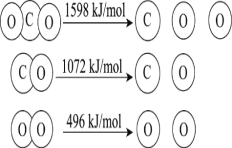
下列说法错误的是( )
A.过程①中吸收能量使钛氧键发生了断裂
B.该反应中,光能和热能转化为化学能
C.使用TiO2作催化剂可以提高化学反应速率
D.2mol二氧化碳完全分解成2mol一氧化碳和1mol氧气需要吸热30kJ
-
研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如下:
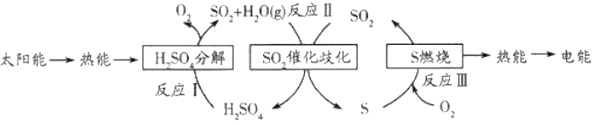
请回答下列问题:
(1)工业生产H2SO4时最后一步反应的化学方程式是_______________________。
(2)反应Ⅰ的化学方程式是_________________。其中氧化产物与还原产物的物质的量之比是________________________。
(3)反应Ⅱ为歧化反应,其中硫元素的化合价是由____________到________________。
(4)反应Ⅲ中硫在氧气中燃烧现象是________________________________。检验生成的二氧化硫的方法是_________________________________________________。观察到的现象是_______________________________。
(5)上述过程中有__________种形式的能量转化,此过程中可能造成一种环境问题是_____________________________。
-
习主席在十九大报告中指出:“绿水青山就是金山银山。”而利用化学知识降低污染、治理污染,改善人类居住环境是化学工作者当前的首要任务。下列做法不利于环境保护的是
A. 开发清洁能源 B. 有效提高能源利用率
C. 研制易降解的生物农药 D. 对废电池做深埋处理
-
化学与环境密切相关.近年来雾霾问题已成为百姓所关注的主要问题,今年入秋以来,我国大部分地区更是“霾伏”四起,部分地区持续出现中度至重度霾,环境治理刻不容缓。回答下列问题:
(1)下列有关说法正确的是
A.光化学烟雾是氮氧化物与碳氢化合物受紫外线作用后产生的有毒烟雾
B.PH小于7的雨水都是酸雨
C.PM2.5含量的增加是形成雾霾天气的重要原因之一
D.大气中CO2含量的增加会导致臭氧空洞的加剧
(2)盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就硫酸、硝酸与金属铜反应的情况,回答下列问题:
①工业上制备硫酸铜是利用废铜屑经灼烧后,在加热情况下跟稀硫酸反应,有关的化学方程式是: 、 ;(两个);不采用铜跟浓硫酸反应来制取硫酸铜的原因是 (答两点)
②在一定体积的10mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积 (填“大于”、“等于”或“小于”)180mL。
③若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为
④将8gFe2O3投入到150mL某浓度的稀硫酸中,再投入7g铁粉,充分反应后,收集到1.68LH2(标准状况),同时,Fe和Fe2O3均无剩余,为了中和过量的硫酸,且使溶液中铁元素完全沉淀,共消耗4mol·L-1的NaOH溶液150mL。则原硫酸的物质的量浓度为
-
化学与环境密切相关.近年来雾霾问题已成为百姓所关注的主要问题,今年入秋以来,我国大部分地区更是“霾伏”四起,部分地区持续出现中度至重度霾,环境治理刻不容缓。回答下列问题:
(1)下列有关说法正确的是
A.光化学烟雾是氮氧化物与碳氢化合物受紫外线作用后产生的有毒烟雾
B.PH小于7的雨水都是酸雨
C.PM2.5含量的增加是形成雾霾天气的重要原因之一
D.大气中CO2含量的增加会导致臭氧空洞的加剧
(2)某化学实验小组测得某地区的雾霾中可能含有如下几种无机离子:Na+、NH4+、Mg2+、Al3+、SO42﹣、NO3﹣、Cl﹣.对该地区雾霾处理后获得试样溶液进行了如下的实验:
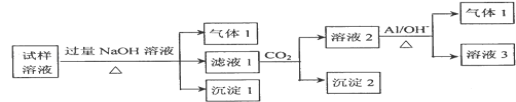
已知:3NO3﹣+8Al+5OH﹣+18H2O═3NH3↑+8[Al(OH)4]﹣
请回答下列问题:
①试样溶液加入过量NaOH溶液后生成沉淀Ⅰ的化学式是 .生成气体Ⅰ的离子方程式为 ,检验该气体的方法是 。
②根据实验结果,推测出雾霾中一定含有的离子有 ,若要确定原试样溶液存在的其它阴离子,可在试样溶液中先加入足量的 溶液,再取上层清液加入 溶液。
(3)若该实验小组测得另一地区雾霾试样中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32﹣、Cl﹣、NO3﹣中的几种.①若加入锌粒,排空法收集到无色无味气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间关系如图所示.则下列说法不正确的是
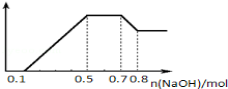
A.溶液中一定不含CO32﹣,可能含有SO42﹣和Cl﹣
B.溶液中n(Mg2+)=0.1mol
C.溶液中的阴离子的物质的量为0.35 mol
D.n(H+):n(Al3+):n(Mg2+)=1:1:1
-
化学与环境密切相关.近年来雾霾问题已成为百姓所关注的主要问题,今年入秋以来,我国大部分地区更是“霾伏”四起,部分地区持续出现中度至重度霾,环境治理刻不容缓。回答下列问题:
(1)下列有关说法正确的是
A.光化学烟雾是氮氧化物与碳氢化合物受紫外线作用后产生的有毒烟雾
B.PH小于7的雨水都是酸雨
C.PM2.5含量的增加是形成雾霾天气的重要原因之一
D.大气中CO2含量的增加会导致臭氧空洞的加剧
(2)盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就硫酸、硝酸与金属铜反应的情况,回答下列问题:
①工业上制备硫酸铜是利用废铜屑经灼烧后,在加热情况下跟稀硫酸反应,有关的化学方程式是: ; (两个);不采用铜跟浓硫酸反应来制取硫酸铜的原因是 (答两点)
②在一定体积的10 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9 mol。则浓硫酸的实际体积 (填“大于”、“等于”或“小于”)180 mL。
③若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为
④将8 g Fe2O3投入到150 mL某浓度的稀硫酸中,再投入7 g铁粉,充分反应后,收集到1.68 L H2(标准状况),同时,Fe和Fe2O3均无剩余,为了中和过量的硫酸,且使溶液中铁元素完全沉淀,共消耗4 mol·L-1的NaOH溶液150 mL。则原硫酸的物质的量浓度为
-
十九大报告提出“坚持保护环境,建设美丽中国”,下列物质不属于空气污染物的是
A. SO2 B. NO2 C. PM2.5 D. CO2
-
随着社会的发展 ,环境问题越来越受到人们的关注。请回答下列相关问题。
I.汽车尾气中含有 CO、NO 等有害气体 ,某新型催化剂能促使 NO、CO 转化为 2 种无毒气体。T℃时,将 0.8 molNO 和 0. 8molCO 充入容积为 2L 的密闭容器中,模拟尾气转化,容器中 NO 物质的量随时间变化如图所示 。
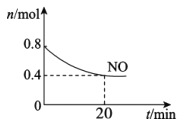
(1)将NO、CO转化为2种无毒气体的化学方程式是___________________。
(2)反应开始至20min,v (NO) =_________mol/ (L• min) 。
(3)下列说法正确的是__________。
a.新型催化剂可以加快 NO、CO的转化
b.该反应进行到 20 min 时达到化学平衡状态
c.平衡时CO的浓度是 0.4 mol/ L
d.混合气体的总压强不随时间的变化而变化说明上述反应达到平衡状态
e.保持容器体积不变,充入 He 增大压强,反应速率加快
II我国最近在太阳能光电催化— 化学耦合分解硫化氢研究中获得新进展 ,相关装置如图所示。
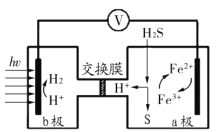
(1)负极为_________极(填“ a” 或“ b” ) 发生的电极反应式为______________。
(2)为使电池持续放电 ,交换膜需选用 ___________交换膜(填“阳离子” 或“阴离子”或“质子”)。
(3)分解硫化氢的离子方程式为_______________________。










