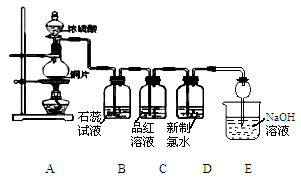-
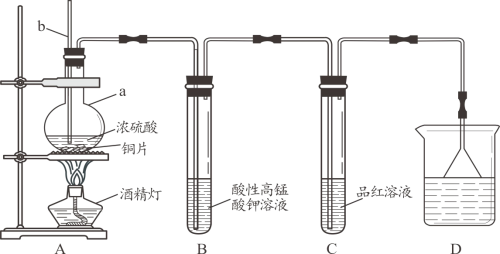
某化学兴趣小组为探究SO2的化学性质,设计了如下图所示的装置进行实验。回答下列问题:
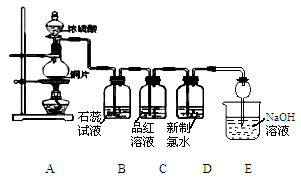
(1)装置A中盛放浓硫酸的仪器名称是________,写出圆底烧瓶发生反应的化学方程式________。
(2)E装置中干燥管的作用是____________________________。
(3)实验过程中,观察到B中的现象是_______________,原因是__________________;观察到C瓶中氯水褪色,这是因为SO2具有_______性,反应的离子方程式为__________________。
(4)用装置C还能探究SO2与品红作用的可逆性,请写出实验操作及现象__________________。
(5)充分反应后,小组同学发现铜和硫酸都有剩余,原因是___________________。若想使剩余的铜溶解,可再加入___________(填序号)。
①盐酸;②硝酸;③NaNO3固体;④K2SO4固体
-
硫代硫酸钠与稀硫酸的反应为:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O。某实验兴趣小组用如下图所示的实验装置探究外界条件对化学反应速率的影响(加热仪器和夹持仪器均已省略)
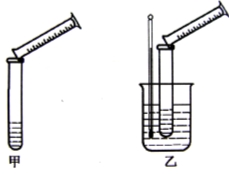
(1)实验目的:
装置甲,探究浓度对化学反应速率的影响;装置乙,探究 对化学反应速率的影响。
(2)装置乙中的加热方法称为 加热,该加热方法具有 、
等优点。
(3)通过甲、乙装置,分别进行了四组实验,数据记录如下,并经分析得出相关结论:
| 实验组号 | 温度 | Na2S2O3 | H2SO4 | 加入H2O 的体积 | 出现沉淀 所需时间 |
| 体积 | 浓度 | 体积 | 浓度 |
| Ⅰ | 0OC | 5mL | 0.1mol/L | 10mL | 0.1mol/L | 5mL | 8s |
| Ⅱ | 0OC | 5mL | 0.1mol/L | 5mL | 0.1mol/L | 10mL | 12s |
| Ⅲ | 30OC | 5mL | 0.1mol/L | 5mL | 0.1mol/L | 10mL | 4s |
| Ⅳ | 30OC | 5mL | 0.2mol/L | 5mL | 0.2mol/L | 10mL | 2s |
| | | | | | | |
结论1: ;
结论2: 。
-
(12分)某校化学兴趣小组为研究Cl2的性质,设计如下图所示装置进行实验。装置III中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
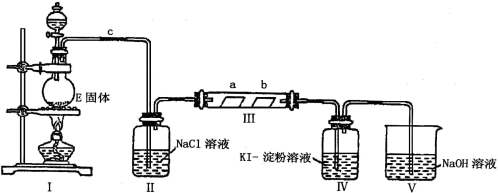
(1)实验室以二氧化锰和浓盐酸制备氯气的化学方程式是 。
(2)装置Ⅱ的作用是 。
(3)实验过程中,装置IV中的实验现象为___________________________________;发生反应的化学方程式为 。
(4)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置 与 之间添加下图中的 装置(填序号),该装置的作用是______________________。
(5)装置Ⅴ的目的是防止尾气污染空气,写出装置Ⅴ中发生反应的离子方程式 。
-
某校化学兴趣小组为研究Cl2的性质,设计如下图所示装置进行实验。装置III中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
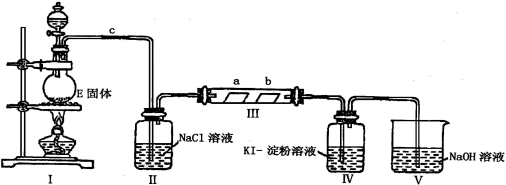
(1)实验室以二氧化锰和浓盐酸制备氯气的化学方程式是 。
(2)装置Ⅱ的作用是 。
(3)实验过程中,装置IV中的实验现象为____________________;发生反应的化学方程式为 。
(4)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置中某处,添加下图中的某种装置,该装置的作用是______________________。
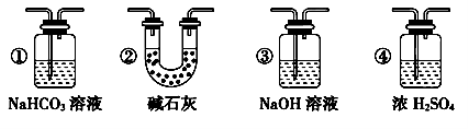
(5)装置Ⅴ的目的是防止尾气污染空气,写出装置Ⅴ中发生反应的离子方程式 。
-
(5分)硫代硫酸钠溶液与稀硫酸的反应方程式为:
Na2S2O3+H2SO4 = Na2SO4+S↓+SO2+H2O,
某实验兴趣小组用如下图所示的实验装置探究外界条件对化学反应速率的影响(加热仪器和夹持仪器均已省略)。
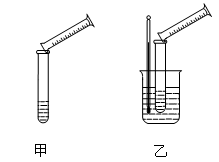
(1)实验目的:装置甲,探究浓度对化学反应速率的影响;装置乙,探究________对化学反应速率的影响。
(2)通过甲、乙装置,分别进行了三组实验,数据记录如下,并经分析得出相关结论:
| 实验 组号 | 温度] | Na2S2O3溶液 | H2SO4 | 加入H2O的体积 | 出现沉淀所需时间 |
| 体积 | 浓度 | 体积 | 浓度 |
| Ⅰ | 0℃ | 5mL | 0.1mol·L-1 | 10mL | 0.1mol·L-1 | 5mL | 8s |
| Ⅱ | 0℃ | 5mL | 0.1mol·L-1 | 5mL | 0.1mol·L-1 | 10mL | 12s |
| Ⅲ | 30℃ | 5mL | 0.1mol·L-1 | 5mL | 0.1mol·L-1 | 10mL | 4s |
结论1:由Ⅰ和Ⅱ两组数据可知 ;
结论2:由Ⅱ和Ⅲ两组数据可知________ ________。
-
某小组同学探究浓硫酸及其部分反应产物的化学性质,装置如下图所示(夹持装置略去)
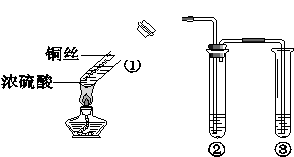
(1)试管①中反应的化学方程式是 。该反应表明浓硫酸具有 (填序号)。
a.酸性 b.强氧化性 c.还原性
(2)若试管②中的试剂为品红溶液,实验中观察到的现象是 ,说明试管①中生成的气体具有 性。
(3)若试管②中的试剂为酸化的Ba(NO3)2溶液,观察到生成不溶于硝酸的白色沉淀,说明试管①中生成的气体具有 性。
(4)试管③中的试剂为NaOH溶液,反应的离子方程式是 。
-
某化学兴趣小组为探究浓硫酸的性质,设计了如下图所示的装置进行实验。
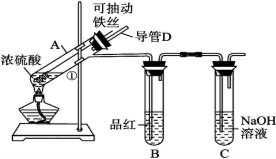
(1)用“可抽动的铁丝”代替“直接投入铁片”的优点是 。
(2)说明SO2气体产生的实验现象是 ;装置C的作用是 。
(3)反应一段时间后,他们对试管A中溶液的金属离子进行探究,请完成相关试题:
①提出假设: 假设1:只含有Fe3+;
假设2:只含有Fe2+;
假设3:既有Fe2+,又有Fe3+。
②请设计实验方案验证假设3。
限选试剂:稀硫酸、KMnO4溶液、KSCN溶液、NaOH溶液、H2O2溶液。
| 实验步骤 | 预期现象 |
| 步骤一:用胶头滴管取出A试管中的溶液,用水稀释后,并分装在试管Ⅰ、Ⅱ中备用 | 
|
| 步骤二:检验Fe3+,往试管Ⅰ中, | |
| 步骤三:检验Fe2+,往试管Ⅱ中, | |
(4)已知C+2H2SO4(浓) 2SO2↑+CO2↑+2H2O,该反应体现浓硫酸的 性。
2SO2↑+CO2↑+2H2O,该反应体现浓硫酸的 性。
A.脱水性 B.强氧化性 C.吸水性
若要验证反应产物中同时混有SO2气体和CO2气体,可选择以下试剂进行实验:
①NaOH溶液②品红溶液③溴水④Ca(OH)2溶液,选择合适试剂并安排合理的顺序为 。
-
某化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物性质,设计如下实验。请回答下列问题:
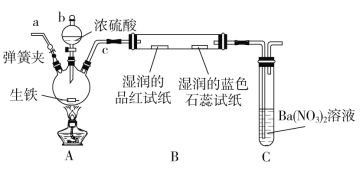
(1)按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为___;实验过程中,装置B中观察到的现象是______;装置C中有白色沉淀生成,该沉淀是_____(填化学式)。
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式:______。
(3)为了验证装置A中产生的气体中含有CO2,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为____(填序号);然后再进行的操作是从a处多次鼓入N2,其目的是___。

(4)某同学发现实验后期装置A中产生的气体中还含有H2,理由是___________ (用离子方程式表示)。
-
某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。 [制取氨气的反应原理: 2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O]
CaCl2+2NH3↑+2H2O]
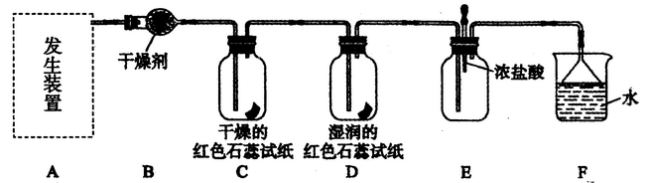
【实验探究】
(1) 利用上述原理,实验室制取氨气应选用下图中_______________发生装置进行实验。

(2)B 装置中的干燥剂可选用______________(填“碱石灰”或“浓硫酸”)。
(3)用 5.35 g NH4Cl 固体与足量 Ca(OH)2 反应,最多可制得标准状况下氨气的体积为 _________L。( NH4Cl 的摩尔质量为 53.5 g·mol-1)
(4)气体通过 C、D 装置时,试纸颜色会发生变化的是 __________( 填“C”或“D”)。
(5)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2 滴浓盐酸,可观察到的现象是______________。
(6)F装置中倒置漏斗的作用 _____________。
(7)某同学用氨气和滴加酚酞的水做喷泉实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有________性质(填序号)。
a.还原性 b.极易溶于水 c.与水反应生成碱性物质
(8)氨气的用途很广。如可用氨气处理二氧化氮: 8NH3 + 6NO2 =7N2 + 12H2O该反应中氨气体现________( 填“氧化性”或“还原性”)。请你列举出氨气的另一种用途__________。
-
某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。 [制取氨气的反应原理: 2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O]
CaCl2+2NH3↑+2H2O]
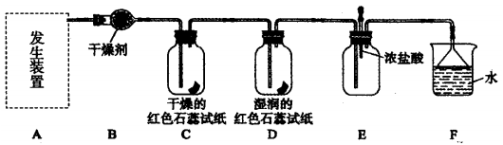
【实验探究】
(1) 利用上述原理,实验室制取氨气应选用下图中_______发生装置进行实验。

(2)B 装置中的干燥剂可选用________( 填“碱石灰”或“浓硫酸”)。
(3)用 5.35 g NH4Cl 固体与足量 Ca(OH)2 反应,最多可制得标准状况下氨气的体积为_________L。( NH4Cl 的摩尔质量为 53.5 g·mol-1)
(4)气体通过 C、D 装置时,试纸颜色会发生变化的是 __________( 填“C”或“D”)。
(5)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2 滴浓盐酸,可观察到的现象是__________。
(6)F装置中倒置漏斗的作用 _____________。
(7)某同学用氨气和滴加酚酞的水做喷泉实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有___________性质(填序号)。
a.还原性 b.极易溶于水 c.与水反应生成碱性物质
(8)氨气的用途很广。如可用氨气处理二氧化氮: 8NH3 + 6NO2 =7N2 + 12H2O该反应中氨气体现________( 填“氧化性”或“还原性”)。请你列举出氨气的另一种用途__________。