-
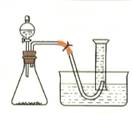
(6分)、右图是研究外界因素对过氧化氢分解反应速率影响的实验装置图。某学生研究小组在50mL量筒中盛满水,倒置于水槽中,通过分液漏斗把过氧化氢溶液加入锥形瓶中(内中已有适量二氧化锰催化剂),记录各时间段在室温下收集到的氧气的体积。
第1组:粉末状的二氧化锰0.2g+ 5ml 6% H2O2
第2组:粉末状的二氧化锰0.2g+ 3ml 12% H2O2
第3组:粉末状的二氧化锰0.1g+ 5ml 6% H2O2
第4组:颗粒状的二氧化锰0.1g+ 5ml 6% H2O2
| 催化剂:MnO2 | 第1组 | 第2组 | 第3组 | 第4组 |
| 前15s产生氧气的量(ml) | 11 | 15 | 8 | 7 |
| 前30s产生氧气的量(ml) | 21 | 24 | 11 | 9 |
| 前45s产生氧气的量(ml) | 31 | 35 | 18 | 12 |
| 前60s产生氧气的量(ml) | 45 | 48 | 26 | 15 |
(1)写出H2O2分解的反应方程式:________ ;
(2)从实验的几组数据中能得到的是:________;
(3)实验比较反应速率时可以测定相同时间内产生气体的体积,也可测________。
-
如图是研究催化剂对过氧化氢分解反应速率影响的实验装置图。某学生研究小组在50mL量筒中盛满水,倒置于水槽中,通过分液漏斗把过氧化氢溶液加入锥形瓶中(瓶中已有适量催化剂),记录各时间段收集到的氧气的体积。
实验一:以二氧化锰作催化剂,进行以下四组实验。
第1组:粉末状的二氧化锰0.2g+5mL6%H2O2
第2组:粉末状的二氧化锰0.2g+5mL10%H2O2
第3组:粉末状的二氧化锰0.1g+5mL6%H2O2
第4组:颗粒状的二氧化锰0.1g+5mL6%H2O2
| 催化剂:MnO2 | 0.2g粉末状的MnO2+5mL6%H2O2 | 0.2g粉末状的MnO2+5mL10%H2O2 | 0.1g粉末状的MnO2+5mL6%H2O2 | 0.1g颗粒状的MnO2+5mL6%H2O2 |
| 前15s产生O2(mL) | 11 | 15 | 8 | 7 |
| 前30s产生O2(mL) | 21 | 24 | 11 | 9 |
| 前45s产生O2(mL) | 31 | 35 | 18 | 12 |
| 前60s产生O2(mL) | 45 | 48 | 26 | 15 |
实验二:以不同的催化剂对过氧化氢(均为5mL6%H2O2)分解反应速率影响进行研究,记录反应的时间t和相应的量筒内的气体体积读数V,用 t作为反应速率的表达式(单位:mL•s﹣1),得到以下实验数据:
t作为反应速率的表达式(单位:mL•s﹣1),得到以下实验数据:
| 催化剂 | 产生气体速率/mL•s﹣1 | 催化剂 | 产生气体速率/mL•s﹣1 |
| MnO2 | 0.03 | 土豆 | 0.03 |
| CuO | 0.07 | 活性炭 | 0.12 |
(1)写出实验一中H2O2分解的反应方程式_________。
(2)实验一的几组数据能够说明在实验中影响反应速率的因素主要有_________。
(3)实验二的几组数据反映出的问题是_________。
(4)用碰撞理论解释使用正催化剂能增大化学反应速率的原因_________。
 .
.
-
I某课外兴趣小组对H2O2的分解速率做了如下实验探究。
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用 10mL H2O2制取
10mL H2O2制取 150mL O2所需的时间(秒)
150mL O2所需的时间(秒)
| 
| 
| 
| 
| 
|
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
|  催化剂、加热 催化剂、加热
| 10 | 25 | 60 | 120 |
①该研究小组在设计方案时,考虑了温度、________、催化剂等因素对过氧化氢分解速率的影响。
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响: _____________。
(2)将质量相同但颗粒大小不同的MnO2分别加入到5mL5%的双氧水中,并用带火星的木条测试。测定结果如下:
| 催化剂(MnO2) | 操作情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 混合不振荡 | 剧烈反应,带火星的布条复燃 | 3.5分钟 |
| 块状 | 反应较慢,火星红亮但木条未复燃 | 30分钟 |
实验结果说明催化剂作用的大小与_________________________有关。
Ⅱ 在体积为2L的密闭容器中充入1molH2 (g)和1molI2 (g),在一定温度下发生下列反应:
在体积为2L的密闭容器中充入1molH2 (g)和1molI2 (g),在一定温度下发生下列反应:

 ,回答下列问题:
,回答下列问题:
(1)保持容器体积不变,向其中充入1molHI(g),反应速率_________(填“加快”“减慢”或“不变”)。
(2)保持容器内气体压强不变,向其中充入1mol氦气,反应速率_________________。(填“加快”“减慢”或“不变”)。
(3)反应进行到2min,测得容器内HI的浓度为0.2mol/L,用H2表示前2min该反应的平均化学反应速率为________________________,此时I2的转化率为____________。
-
下列装置或操作能达到实验目的的是
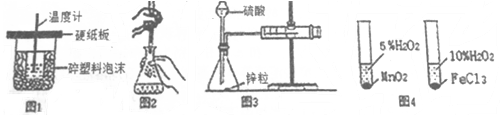
A.图1装置用于中和热的测定
B.图2装置用于高锰酸钾溶液滴定草酸
C.图3装置用于测定氢气的反应速率(单位mL/s)
D.图4装置用于研究不同催化剂对反应速率的影响
-
H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。

(1)若利用图甲装置,可通过观察__________现象,从而定性比较得出结论。
(2)有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是 ________。写出H2O2在二氧化锰催化作用下发生反应的化学方程式:___________。
(3)若利用乙实验可进行定量分析,图乙中仪器A的名称为________,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是________。
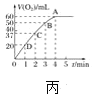
(4)将0.1molMnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图丙所示,解释反应速率变化的原因:________。H2O2初始物质的量浓度为_______(保留两位小数)。
-
某小组同学研究影响双氧水分解反应速率的因素。实验所用试剂:10%H2O2、蒸馏水、MnO2粉末
| 实验序号 | H2O2浓度 | V(H2O2溶液) | 温度 | 催化剂 | 实验现象 |
| 1 | 10% | 20mL | 室温 | 无 | 无明显现象 |
| 2 | 10% | 20mL | 50℃水浴 | 无 | 有较多气泡产生 |
| 3 | 10% | 20mL | 室温 | MnO2(0.2g) | 有较多气泡产生 |
(1)实验1、2的目的是研究________对双氧水分解反应速率的影响。
(2)通过对比实验_______(填序号),可研究催化剂对双氧水分解反应速率的影响。
(3)为了准确地比较反应速率的快慢,观测的方法是:收集相同体积的气体,__________。
(4)利用上述实验试剂,并结合已有实验方案,进一步设计实验研究双氧水浓度对其分解反应速率的影响。请将实验方案补全。
| 实验序号 | H2O2浓度 | | | | | 实验现象 |
| 4 | 10% | ①___ | ②___ | ③___ | ④___ | ⑤___ |
-
某化学研究性学习小组以海带为原料制取了少量碘水.现用四氯化碳从碘水中萃取碘并用分液漏斗分离两种溶液.其实验操作可分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50mL碘水和15mL四氯化碳加入分液漏斗中,并盖好玻璃塞;
C.检查分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转分液漏斗,用力振荡,并不时旋开活塞放气,最后关闭活塞,分液漏斗放正;
E.旋开活塞,用烧杯承接溶液;
F.从分液漏斗上口倒出上层水溶液;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
H.静置、分层;
就此实验,完成下列填空:
(1)正确操作步骤的顺序是(用上述各操作的编号字母填写)______________________
(2)上述E步骤的操作中应注意 ;上述G步骤操作的目的是_________
(3)能选用四氯化碳从碘水中萃取碘的原因是_______________________
(4)已知碘在酒精中的溶解度比在水中大得多,能不能用酒精来萃取碘水中的碘(填“能”或“不能”)_____________,其理由是 。
-
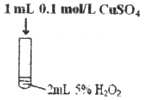
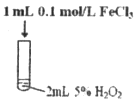
某研究小组设计了如下实验,探究常温下催化剂对过氧化氢分解反应的影响。
| Ⅰ | Ⅱ | Ⅲ |
| 实验操作 示意图 | 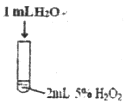
| 
| 
|
| 实验现象 | 有极少量气泡产生 | 产生气泡速率略有加快 | 产生气泡速率明显加快 |
(1)实验Ⅰ的作用是_______________。
(2)实验Ⅲ中反应的化学方程式为_______________。
(3)根据实验Ⅰ~Ⅲ中现象的不同,可以得出的结论是:
①使用合适的催化剂,可提高双氧水分解的反应速率;
②_______________。
(4)在一定温度下,10 mL 0.40 mol/L,H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表所示:
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
0~6 min,以H2O2的浓度变化表示的反应速率为v(H2O2)=_________mol/(L·min)。(计算结果精确到0.001)
-
某化学研究性学习小组以海带为原料制取了少量碘水。现用四氯化碳从碘水中萃取碘并用分液 漏斗分离两种溶液。其实验操作可分解为如下几步:
(A)把盛有溶液的分液漏斗放在铁架台的铁圈中;
(B)把50 mL碘水和15 mL四氯化碳加入分液漏斗中,并盖好玻璃塞;
(C)检查分液漏斗活塞和上口的玻璃塞是否漏液;
(D)倒转分液漏斗,振荡,并不时旋开活塞放气,最后关闭活塞,分液漏斗放正;
(E)旋开活塞,用烧杯承接溶液;
(F)从分液漏斗上口倒出上层水溶液;
(G)将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
(H)静置、分层;
就此实验,完成下列填空:
(1)正确操作步骤的顺序是:(用上述各操作的编号字母填写) → → →A→H→G →E→F。
(2)能选用四氯化碳从碘水中萃取碘的原因是 ;_________________________。
(3)已知碘在酒精中的溶解度比在水中大的多,能不能用酒精来萃取碘水中的碘 _________(填“能”或“不能”),其理由是 。
(4)上述G步骤的操作目的是__________________
-
某化学研究性学习小组以海带为原料制取了少量碘水.现用四氯化碳从碘水中萃取碘并用分液漏斗分离两种溶液.其实验操作可分解为如下几步:
| A.把盛有溶液的分液漏斗放在铁架台的铁圈中; |
| B.把50mL碘水和15mL四氯化碳加入分液漏斗中,并盖好玻璃塞; |
| C.检查分液漏斗活塞和上口的玻璃塞是否漏液; |
| D.倒转分液漏斗,用力振荡,并不时旋开活塞放气,最后关闭活塞,分液漏斗放正; |
E.旋开活塞,用烧杯承接溶液;
F.从分液漏斗上口倒出上层水溶液;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
H.静置、分层;
就此实验,完成下列填空:
(1)正确操作步骤的顺序是(用上述各操作的编号字母填写)______________________
(2)上述E步骤的操作中应注意________________;上述G步骤操作的目的是_________
(3)能选用四氯化碳从碘水中萃取碘的原因是_______________________
(4)已知碘在酒精中的溶解度比在水中大得多,能不能用酒精来萃取碘水中的碘(填“能”或“不能”)_____________,其理由是______________________。
 t作为反应速率的表达式(单位:mL•s﹣1),得到以下实验数据:
t作为反应速率的表达式(单位:mL•s﹣1),得到以下实验数据: .
.






