-
(9分) 在复习元素周期律过程中,某研究性学习小组的几位同学拟通过具体的实验来探讨某些金属元素的性质差异,下面是他们设计的探究性实验方案,请填写下列空白:
(1) 实验目的:比较钠、镁、铝金属性强弱。
(2) 实验用品:酒精灯、________、试管、试管夹、砂纸、滤纸;
钠、镁条、铝片、酚酞、蒸馏水、6 mol·L-1的盐酸
(3)实验过程与现象记录
I.甲同学的方案如下:
实验过程
预期现象
实际观察到的现象
a取已切去表皮的一小块金属钠,放入盛有水的某容器中
立即剧烈反应
开始时钠块浮在水面上不反应,稍后才开始与水剧烈反应
b向盛有适量水(内含2滴
酚酞的试管中加入一小段镁条
有气泡产生,溶液变红色
没有相应现象,加热后仍无明显变化
c向两支盛有3mL6mol·L-1盐酸的试管中加入大小相同的镁片和铝片
镁、铝与盐酸反应产生气泡剧烈程度不同
镁与盐酸反应产生气泡速率较快
①你认为a、b两步实验中出现异常现象的可能原因是:
a________;
b________。
②上面的实验表明:钠、镁、铝三种元素的金属性由强到弱的顺序为________。
II乙同学的方案:他认为只需要一种试剂就可以确定钠、镁、铝的金属性强弱,预计他的主要实验操作是________。
高一化学实验题简单题查看答案及解析
-
在复习元素周期律过程中,某研究性学习小组的几位同学拟通过具体的实验来探讨某些金属元素的性质差异,下面是他们设计的探究性实验方案,请填写下列空白:
(1)实验目的:比较钠、镁、铝金属性强弱。
(2)实验用品:酒精灯、________、试管、试管夹、砂纸、滤纸;
钠、镁条、铝片、酚酞、蒸馏水、6 mol·L-1的盐酸
(3)实验过程与现象记录
Ⅰ.甲同学的方案如下:
实验过程
预期现象
实际观察到的现象
a取已切去表皮的一小块金属钠,放入盛有水的某容器中
立即剧烈反应
开始时钠块浮在水面上不反应,稍后才开始与水剧烈反应
b向盛有适量水(内含2滴
酚酞的试管中加入一小段镁条
有气泡产生,溶液变红色
没有相应现象,加热后仍无明显变化
c向两支盛有3mL6mol·L-1盐酸的试管中加入大小相同的镁片和铝片
镁、铝与盐酸反应产生气泡剧烈程度不同
镁与盐酸反应产生气泡速率较快
①你认为a、b两步实验中出现异常现象的可能原因是:
a________;
b________。
②上面的实验表明:钠、镁、铝三种元素的金属性由强到弱的顺序为________。
Ⅱ乙同学的方案:他认为只需要一种试剂就可以确定钠、镁、铝的金属性强弱,预计他的主要实验操作是________。
高一化学实验题中等难度题查看答案及解析
-
某研究性学习小组设计了一组实验来探究元素周期律。
【甲同学】 设计了如图1装置来一次性完成验证非金属性S>C>Si的实验研究;
【乙同学】 设计了如图2装置来验证卤族元素性质的递变规律。
A、B两处分别是浸有NaBr溶液的棉花、湿润的淀粉KI试纸,
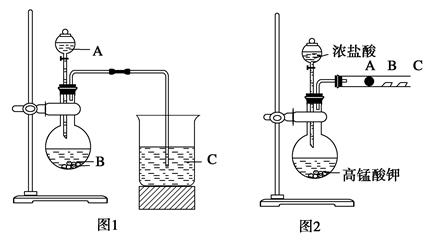
(1)①甲同学设计实验的依据是 。
② A溶液的名称是 。
③ 烧杯中C发生反应的离子方程式为 。
(2)乙同学的实验原理是通过观察玻璃管中的实验现象,验证卤族元素性质的递变。
① 写出A处发生反应的离子方程式 。
② B处的实验现象为 。
高一化学实验题困难题查看答案及解析
-
下面是某化学兴趣小组的同学学习元素周期律时设计的两套实验方案。
(实验一)实验步骤如下:
向新制的Na2S溶液中滴加新制的氯水
设计该实验方案的目的是:探究同周期元素的性质递变规律。
(1)实验①的现象是_____________________,反应的离子方程式是_________________。
(实验二)为验证Cl、Br的非金属性强弱,设计了如下实验:(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)实验步骤如图.
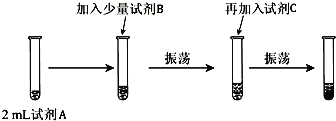
(2)试剂A是NaBr溶液,试剂B是氯水,加C后出现分层,则试剂C是____________.
(3)加入C振荡、静置后看到的现象是:______________________________________。以上反应可以证明Cl的非金属性__________(填“强于”或“弱于”)Br的非金属性。
高一化学实验题中等难度题查看答案及解析
-
某研究性学习小组设计了一组实验验证元素周期律. Ⅰ.甲同学设计了如如图装置来一次性完成元素氮、碳、硅非金属性强弱的比较。
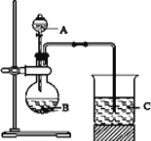
(1)甲同学在连接好仪器后,加入药品之前的具体操作是:______________
(2)要证明氮、碳、硅非金属性强弱,在 A 中加________________溶液,B 中加___________溶液,C 中加___________溶液,将观察到C 中________________的现象.但花花认为,该现象不足以证明三者非金属性强弱,请用文字叙述理由_____________。
(3)为避免上述问题,应在 B、C 之间增加一个盛有足量_____的洗气装置.改进后C 中发生反应的离子方程式是________________.
Ⅱ.丙同学设计了如如图装置来验证卤族元素性质的递变规律.A、B、C 三处分别是沾有NaBr 溶液的棉花、湿润淀粉 KI 试纸、湿润红纸.
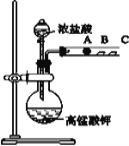
(4)请写出浓盐酸与高锰酸钾反应的离子方程式:______________
(5)A 中棉花颜色变_______,则说明非金属性 Cl>Br;向 NaBr 和 KI 的混合溶液中,通入足量的 Cl2 充分反应后,将所得溶液蒸干并灼烧,最后得到的物质是___________
高一化学综合题中等难度题查看答案及解析
-
(13分)某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种元素的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。

(1)图1中仪器A的名称是 。甲同学实验步骤:连接仪器、 、加药品、滴入试剂。
(2)①图1中烧瓶B中的盛放试剂为碳酸钙,C中盛放试剂为硅酸钠溶液,则甲同学设计实验的依据是 。
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是 。
(3)图2中A处反应的离子方程式 。
(4)乙同学发现图2中B处试纸变蓝,C处红纸褪色,据此 (填“能”或“不能”)得出溴的非金属性强于碘,理由是 。
高一化学实验题极难题查看答案及解析
-
某研究性学习小组设计了一组实验来探究元素周期律。
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素非金属性强弱比较的实验研究;
乙同学设计了如图2装置来验证卤族元素性质的递变规律,A、B、C三处分别是蘸有溴化钠溶液的棉花、湿润的淀粉碘化钾试纸、湿润的红色纸条。
已知常温下浓盐酸与高锰酸钾能反应生成氯气;
可选择的试剂有:大理石、碳酸钠粉末、浓盐酸、稀硝酸、硅酸钠溶液。
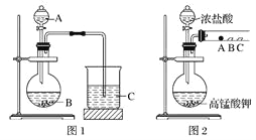
(1)甲同学实验中(图1):
①从给出试剂中选出最佳物质(填化学式):A________,B________。
②烧杯C中发生反应的离子方程式为__________________________。
(2)乙同学实验中(图2):
①写出A处反应的离子方程式________________________。
②B处实验现象是________________________。
③若高锰酸钾的还原产物为Mn2+,当有0.04 mol高锰酸钾参加反应时,则可生成标准状况下的氯气的体积为______________________。
高一化学实验题困难题查看答案及解析
-
某研究性学习小组设计了一组实验来探究元素周期律。
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素非金属性强弱比较的实验研究;
乙同学设计了如图2装置来验证卤族元素性质的递变规律,A、B、C三处分别是蘸有溴化钠溶液的棉花、湿润的淀粉碘化钾试纸、湿润的红色纸条。
已知常温下浓盐酸与高锰酸钾能反应生成氯气;
可选择的试剂有:大理石、碳酸钠粉末、浓盐酸、稀硝酸、硅酸钠溶液。
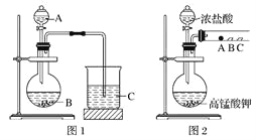
(1)甲同学实验中(图1):
①从给出试剂中选出最佳物质(填化学式):A________,B________。
②烧杯C中发生反应的离子方程式为__________________________。
(2)乙同学实验中(图2):
①写出A处反应的离子方程式________________________。
②B处实验现象是________________________。
③若高锰酸钾的还原产物为Mn2+,当有0.04 mol高锰酸钾参加反应时,则可生成标准状况下的氯气的体积为______________________。
高一化学实验题困难题查看答案及解析
-
(10分)某研究性学习小组设计了一组实验来探究元素周期律。甲同学设计了如图1装置,根据元素非金属性与对应最高价含氧酸之间的关系,可以一次性完成碳族元素中C与Si的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、蘸有碱液的棉花。已知常温下浓盐酸与高锰酸钾能反应生成氯气。

(1)甲同学设计实验的理论依据是_____________________________________;
写出选用试剂分别为:A____________,B__________,C____________;
其中装置B中所盛试剂的作用为_____________________________________;
C中反应的离子方程式为____________________________________________;
(2)乙同学的实验理论依据是______________________________________;
写出A处的离子方程式: ___________________________________________;
B处的现象________,C处药品的作用 ________。
高一化学实验题简单题查看答案及解析
-
某研究性学习小组设计了一组实验来探究元素周期律.
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素非金属性强弱比较的实验研究;
乙同学设计了如图2装置来验证卤族元素性质的递变规律,A、B、C三处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红色纸条.
已知常温下浓盐酸与高锰酸钾能反应生成氯气.
可选择的试剂有:大理石、碳酸钠粉末、浓盐酸、稀硝酸、硅酸钠溶液.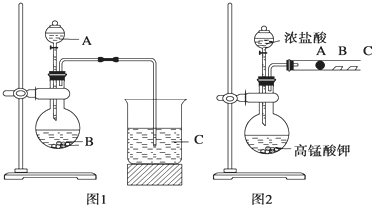
(1)甲同学实验中(图1):
①从给出试剂中选出最佳物质:A______,B______.(填化学式)
②烧杯C中发生反应的离子方程式为______.
(2)乙同学实验中(图2):
①写出A处反应的离子方程式______.
②B处实验现象是______.
③若高锰酸钾的还原产物为Mn2+,当有0.04mol高锰酸钾参加反应时,则可生成标准状况下的氯气的体积为______L.高一化学解答题中等难度题查看答案及解析