-
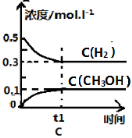
180℃时将0.5 mol H2和1 mol CO2通入1L的恒容密闭容器中,反应生成甲醇蒸汽(CH3OH)和某无机副产物,测得各物质的物质的量随时间的部分变化如图所示,下列说法中正确的是( )
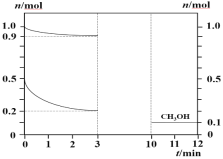
A. 该反应的化学方程式:2CO2+4H2 2CH3OH+O2
2CH3OH+O2
B. 在0~3 min内H2的平均化学反应速率为0.1 mol·L-1·min-1
C. 当容器内混合气体密度不再变化时,表明反应已经达到平衡状态
D. 在3~10 min内,反应仍未达到平衡状态
-
180℃时将0.5 mol H2和1 mol CO2通入1 L的恒容密闭容器中,反应生成甲醇蒸汽(CH3OH)和某无机副产物,测得各物质的物质的量随时间的部分变化如图所示,下列说法中正确的是

A. 该反应的化学方程式:2CO2+4H2 2CH3OH+O2
2CH3OH+O2
B. 在0~3 min内H2的平均化学反应速率为0.1 mol·L-1·min-1
C. 当容器内混合气体密度不再变化时,表明反应已经达到平衡状态
D. 在3~10 min内,反应仍未达到平衡状态
-
(1)180°C时将0.5molH2和1molCO2通入lL的恒容密闭容器中,反应生成甲醇(CH3OH)蒸汽和某无机副产物,测得各物质的物质的量随时间的部分变化如图所示。
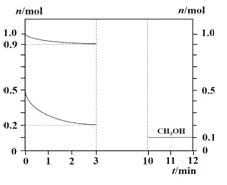
①该反应的化学方程式:____________。
②下列措施能够使该反应速率加快的是____________。
a.使用催化剂
b.降低温度
c.增大压强
③反应达到平衡状态的时间段____________。
a.0~3minb.3~10minc.10~12min
(2)如图所示是某公司批量生产的笔记本电脑所用的甲醇燃料电池的构造示意图。甲醇在催化剂作用下提供质子(H+)和电子,该电池总反应式为2CH3OH+3O2=2CO2+4H2O。(图中负载表示用电器)
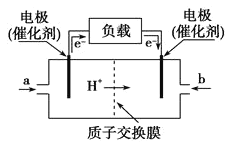
④左边的电极为电池的____________极。
⑤b处通入的是____________(填“空气”或“甲醇”)
⑥该电池正极的反应式为____________。
-
180℃时将0.5 mol H2和1 mol CO2通入2 L的恒容密闭容器中,此时容器内总压强为P0(已知分压=总压×物质的量分数),反应生成甲醇蒸汽(CH3OH)和H2O,测得各物质的物质的量随时间的部分变化如图所示,回答下列问题:
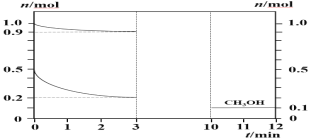
(1)该反应的化学方程式为:___________________
(2)在0~3 min内H2的平均化学反应速率为___________________
(3)0-1分钟的速率为V1,2-3分钟的速率为V2,10-11分钟的速率为V3,则V1、V2、V3由大到小的顺序为____________________________。
(4)3min内H2的转化率为______。
(5)平衡时,容器内的压强为__________,CO2的分压为____________(均保留2位有效数字)
(6)以(1)中反应设计成原电池(用硫酸作电解质溶液),则正极反应式为______________。
-
在一个容积为500mL的密闭容器中,充入5molH2和2molCO。在一定条件下发生如下反应:2H2(g) + CO(g) CH3OH(g),经过5min后达到平衡状态。若此时测得甲醇蒸汽的浓度为2mol/L,求:
CH3OH(g),经过5min后达到平衡状态。若此时测得甲醇蒸汽的浓度为2mol/L,求:
(1)以H2的浓度减少量来表示的反应速率。
(2)达到平衡时CO的转化率。
-
工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g)  CH3OH(g)。一定条件下,将0.5molCO和0.5molH2在体积为2L的密闭容器中发生上述反应,则下列示意图合理的是 ( )
CH3OH(g)。一定条件下,将0.5molCO和0.5molH2在体积为2L的密闭容器中发生上述反应,则下列示意图合理的是 ( )


-
在一个容积为500mL的密闭容器中,充入5molH2和2molCO。在一定条件下发生如下反应:2H2(g) + CO(g) CH3OH(g),经过5min后达到平衡状态。若此时测得甲醇蒸汽的浓度为2mol/L,求:
CH3OH(g),经过5min后达到平衡状态。若此时测得甲醇蒸汽的浓度为2mol/L,求:
(1)以H2的浓度减少量来表示的反应速率。
(2)达到平衡时CO的转化率。
-
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇:在容器为1L的密闭容器中充入1molCO2和3molH2 ,平衡时CO2的物质的量为0.25mol,CO2(g)+3H2(g) CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。
CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。

请回答下列问题:
(1)观察图象可知上述反应过程中,断裂反应物中的化学键吸收的总能量______(填“大于”“小于”或“等于”)形成生成物中的化学键释放的总能量。
(2)甲醇的结构类似于乙醇,试写出甲醇的结构式:__________。甲醇分子中的化学键类型是________(填“离子键”或“共价键”)。
(3)科研人员开发出一种新型甲醇燃料电池。其电解质溶液是KOH溶液,在该电池的负极发生反应的物质是__________,发生的是__________(填"氧化"或"还原")反应。
(4)欲使合成甲醇的化学反应速率加快,请写出两条措施:___________________
(5)平衡时H2的转化率为__________平衡时混合气体中CH3OH(g)的体积分数为__________。
(6)下列事实能表明该反应已达平衡状态的是(_______)(填序号)
A.CO2(g)的浓度不再发生变化
B.单位时间内消耗1mol CO2的同时生成3mol H2
C.在一个绝热的容器中,混合物的温度不再发生变化
D.在一个容积固定的容器内,压强不再发生变化
-
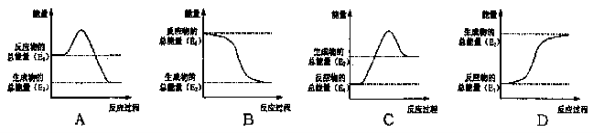
(17分)甲醇(CH3OH)是一种优质燃料,(1)已知一定条件下每1MolCO2和足量氢气完全反应可生成1Mol气态甲醇(CH3OH)和1Mol 水蒸汽并放出49 kJ的热量。请回答:
①该反应的热化学方程式: 。
②其反应过程中能量的变化与如图所示最相符的是 。
(2)为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:在体积为1L的密闭容器中,充入1MolCO2和3MolH2,一定条件下发生反应,测得CO2和CH3OH(g)的浓度随时间变化如图。
请回答:
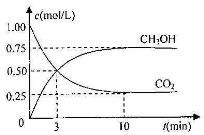
①从反应开始到平衡,甲醇和氢气的反应速率:
v(CH3OH)= 。
v(H2)= 。
②下列措施中能使v (CO2)增大的是 。
A.加入催化剂
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离
D.升高温度
③能够说明该反应已达到平衡的是_________。
A.恒温、恒容时,容器内的压强不再变化
B.恒温、恒容时,容器内混合气体的密度不再变化
C.一定条件下,CO2、H2和CH3OH的浓度不再变化
D.一定条件下,单位时间内消耗3MolH2的同时生成1MolCH3OH
-
目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)十H2O(g),该反应的能量变化如图所示:
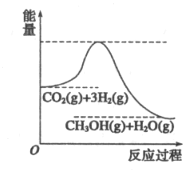
(1)该反应为______(填“放热”或“吸热”)反应。
(2)恒容容器中,对于以上反应,能加快反应速率的是______。
a.升高温度 b.充入氮气 C.加入合适的催化剂 d.降低压强
(3)在体积为2L的密闭容器中,充入1molCO2和3molH2,测得CO2的物质的量随时间变化如表所示。
| t/min | 0 | 2 | 5 | 10 | 15 |
| n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
从反应开始到5min末,用H2浓度变化表示的平均反应速率v(H2)=______;反应达到平衡状态,此时H2的转化率为______。
(4)在相同温度、容积不变的条件下,不能说明该反应已达平衡状态的是______。
a.CO2、H2、CH3OH、H2O的浓度均不再变化
b.体系压强不变
c.n(CO2):n(H2):n(CH3OH):n(H2O)=1:1:1:1
d.H2的消耗速率与CH3OH的消耗速率之比为3:1








 CH3OH(g),经过5min后达到平衡状态。若此时测得甲醇蒸汽的浓度为2mol/L,求:
CH3OH(g),经过5min后达到平衡状态。若此时测得甲醇蒸汽的浓度为2mol/L,求: CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。
CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。


