-
A、B、C、D、E、F代表原子序数依次增大的前四周期元素。其中A是空气中含量最高的元素;B是同周期中原子半径最大的元素;C原子的最外层电子数与核外电子层数相等;D、E元素的基态原子3p能级上都有两个未成对电子;F原子的外围电子排布为(n-1)d10ns1。根据以上信息,回答下列问题:
(1)A元素基态原子核外电子的轨道表达式为________________;在同周期元素中第一电离能介于C、E之间的元素是______(用化学式表示)。
(2)将以下三种物质:①A与硼元素按原子个数比为1∶1形成的空间网状结构化合物,②B的氯化物, ③D的氯化物。按熔点由高到低的顺序排列:______________(用化学式表示)。
(3)A的最简单氢化物易液化,其原因是_______________,E的次高价含氧酸根离子的VSEPR模型名称是_________,该离子的空间构型为__________。
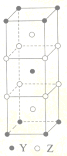
(4)F单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
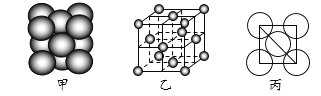

若已知F晶胞参数为a pm,F相对原子质量为M,NA代表阿伏加德罗常数,请回答:
①晶胞中F原子的配位数为_______;F单质晶体中原子的堆积方式是_________堆积。
②F原子半径r =________ pm,F单质晶体密度计算式为:______________ g·cm-3。
(5)A与F形成的某种化合物晶胞结构如图丁所示,该晶体的化学式为___________。该化合物能与稀盐酸剧烈反应,生成一种白色沉淀和一种全部由非金属元素组成的离子化合物,该反应的化学方程式为________。
-
已知前四周期A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态;D原子L电子层上有2对成对电子;E基态原子有6个未成对电子:
请填写下列空白:
(1)E元素在元素周期表的位置是______,E元素基态原子的价电子排布式为_____;
(2)C基态原子的价层电子的轨道表达式______;
(3)B2A4是重要的基本石油化工原料。1molB2A4分子中含_____molσ键;
(4)BD2电子式为_____,此分子键角为_______;
(5)BD32-中心原子孤电子对数为______,离子的立体构型为______;
(6)B、C、D三种元素的第一电离能由小到大的顺序为______(填元素符号),其原因为______。
-
原子序数依次增大的A、B、C、D、E、F六种元素.其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E、F和C位于同一主族,F处于第一个长周期.
(1)F 原子基态的外围核外电子排布式为 ;
(2)由A、B、C形成的离子CAB﹣与AC2互为等电子体,则CAB﹣的结构式为 ;
(3)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为 ;
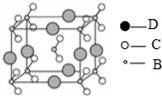
(4)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为 ;
(5)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、CH2═CHCHO、HCOOH、CH3COONO2(PAN)等二次污染物.
①下列说法正确的是 ;
A.N2O为直线型分子
B.C、N、O的第一电离能依次增大
C.CH2═CH一CHO分子中碳原子均采用sp2杂化
D.相同压强下,HCOOH沸点比CH3OCH3高,说明前者是极性分子,后者是非极性分子
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4该配合物中心离子的配体为 ,其中提供空轨道的是 (填微粒符号)
-
原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E、F和C位于同一主族,F处于第一个长周期。
(1) F原子基态的外围电子排布式为_________;
(2)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的结构式为_________;
(3)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为_________;
(4)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、CH2=CHCHO、HCOOH. CH3COONO2(PAN)等二次污染物。
①下列说法正确的是_________
A.N2O为直线型分子
B.C、N、O的第一电离能依次增大
C.CH2=CHCHO分子中碳原子均采用sp2杂化
D.相同压强下,HCOOH沸点比CH3OCH3高,说明前者是极性分子,后者是非极性分子
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中中心离子的配体为_________ (填微粒符号)。
-
原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为29。
(1)F基态原子的核外电子排布式为______________________。
(2)在A、B、C三种元素中,第一电离能由小到大的顺序是___________(用元素符号回答)。
(3)元素B的简单气态氢化物的沸点___________(填“高于”或“低于”)元素A的简单气态氢化物的沸点,其主要原因是______________________。
(4)由A、B、C形成的离子CAB−与AC2互为等电子体,则CAB−的结构式为___________。
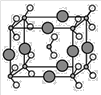
(5)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为___________。
(6)FC在加热条件下容易转化为F2C,从原子结构的角度解释原因______________________。
-
原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为29。
(1)F原子基态的外围核外电子排布式为___________________。
(2)在A、B、C三种元素中,第一电离能由小到大的顺序是____________(用元素符号回答)。
(3)元素B的简单气态氢化物的沸点________(高于,低于)元素A的简单气态氢化物的沸点,其主要原因是________________________。
(4)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的结构式为__________。
(5)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为________。
(6)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为______。
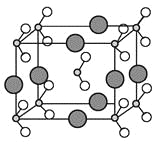
(7)FC在加热条件下容易转化为F2C,从原子结构的角度解释原因____________。
-
原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为29。
(1)F基态原子的核外电子排布式为______________________。
(2)在A、B、C三种元素中,第一电离能由小到大的顺序是___________(用元素符号回答)。
(3)元素B的简单气态氢化物的沸点___________(填“高于”或“低于”)元素A的简单气态氢化物的沸点,其主要原因是______________________。
(4)由A、B、C形成的离子CAB−与AC2互为等电子体,则CAB−的结构式为___________。
(5)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为___________。
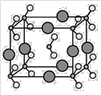
(6)FC在加热条件下容易转化为F2C,从原子结构的角度解释原因______________________。
-
原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为24。
(1)F原子基态的价电子排布式为_______________。
(2)在A、B、C三种元素中,电负性由大到小的顺序是______>______>_____(用元素符号回答)。
(3)元素C的简单气态氢化物的沸点远高于元素E的简单气态氢化物的沸点,其主要原因是________________________。
(4)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的空间构型为_____________。
(5)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为_______________。
(6)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为________________________。
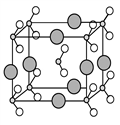
-
【选修三-物质结构与性质】原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E、F和C位于同一主族,F处于第一个长周期。
(1) F原子基态的外围核外电子排布式为_________;
(2)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的结构式为_________;
(3)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为_________;
(4)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、CH2=CHCHO、HCOOH. CH3COONO2(PAN)等二次污染物。
①下列说法正确的是_________
A. N2O为直线型分子
B. C、N、O的第一电离能依次增大
C. CH2=CHCHO分子中碳原子均采用sp2杂化
D.相同压强下,HCOOH沸点比CH3OCH3高,说明前者是极性分子,后者是非极性分子
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中中心离子的配体为_________ (填微粒符号)。
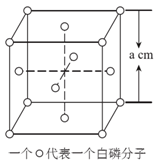
(5) 白磷(P4)的晶体属于分子晶体,其晶胞结构如图2(小圆圈表示白磷分子).己知晶胞的边长为a cm,阿伏加德罗常数为NA mol-l,则该晶胞中含有的P原子的个数为_________,该晶体的密度为_________ g•cm-3(用含NA、a的式子表示)
-
有U、V、W、X、Y、Z六种前四周期元素,原子序数依次增大,其相关信息如下表:
| 元素编号 | 相关信息比 |
| U | 所处的周期数、族序数分别与其原子序数相等 |
| V | 基态时,电子分布在三个能级上,且各能级中电子数相等 |
| W | 基态时, 2p 轨道处于半充满状态 |
| X | 自然界中含量最多 |
| Y | 是第四周期元素中未成对电子数最多的元素 |
请回答下列问题:
(1)W、X、V第一电离能由大到小顺序:________________________(用元素符号表示)
(2)V的最高价氧化物对应含氧酸中,酸根的立体构型为:_________,中心原子的杂化方式为:_______________;
(3)Y的基态原子的价电子排布图为____________________________;
(4)乙和丙分别是V和X的氢化物,这两种氢化物分子中都含有10个电子。两者沸点的关系为乙______丙(填“>”或“<”),原因是__________________________________________;
(5)V与W原子结合形成的V3W4晶体,其硬度比金刚石大,则V3W4晶体中属于____________晶体
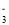 的空间构型为_______(用文字描述)。
的空间构型为_______(用文字描述)。