-
已知前四周期A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态;D原子L电子层上有2对成对电子;E基态原子有6个未成对电子:
请填写下列空白:
(1)E元素在元素周期表的位置是______,E元素基态原子的价电子排布式为_____;
(2)C基态原子的价层电子的轨道表达式______;
(3)B2A4是重要的基本石油化工原料。1molB2A4分子中含_____molσ键;
(4)BD2电子式为_____,此分子键角为_______;
(5)BD32-中心原子孤电子对数为______,离子的立体构型为______;
(6)B、C、D三种元素的第一电离能由小到大的顺序为______(填元素符号),其原因为______。
高二化学推断题中等难度题查看答案及解析
-
【化学-选修3: 物质结构与性质】
已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B 原子核外电子s 轨道电子数是p轨道电子数的两倍;D 原子L 层上有2对成对电子;E2+原子核外有3 层电子且M层3d轨道电子半满。请回答下列问题:
(1)A元素位于周期表_____区,CD3-的空可构型为_____,中心C 原子的杂化方式为______。
(2)第一电离能C>D的原因是__________________。
(3)下列表述中能证明D元素比氟元素电负性弱这一事实的是______。
A.常温下氟气的颜色比D 单质的颜色深
B. 氟气与D 的氢化物剧烈反应,产生D单质
C. 氟与D形成的化合物中D元素呈正价态
D.比较两元素单质与氢气化合时得电子的数目
(4)黄血盐是一种配合物,其化学式为K4[E (CN)6] ·3H2O,黄血盐溶液与稀硫酸加热时发生非氧化还原反应,生成硫酸盐和一种与该配体互为等电子体的气态化合物,该反应的化学方程式为_________________。
(5).铜能与类卤素(SCN)2反应生成Cu (SCN)2,1mol (SCN)2分子中含有σ键的数目为_____;类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H—S—C≡N) 的沸点低于异硫氰酸(H—N=C=S) 的沸点,其原因是______________。
高二化学综合题困难题查看答案及解析
-
(1、2、3班必做)(12分)已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E的+1价阳离子的核外有3层电子且各层均处于全满状态。
(1)E元素基态原子的核外电子排布式为___________________。
(2)B、C、D三种元素的第一电离能由小到大的顺序为_______(用元素符号表示)。
(3)B2A4是石油炼制的重要产物之一 。B2A4分子中B原子轨道的杂化类型为________;1 mol B2A2分子
中含________mol σ键。
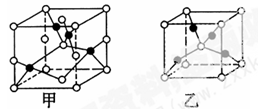
(4)已知D、E能形成晶胞结构如图所示的两种化合物,则化学式:甲
为______,乙为______;高温时,甲易转化为乙的原因为______________________________。
高二化学填空题困难题查看答案及解析
-
A、B、C、D、E、F为原子序数依次增大的六种元素,其中A、B、C、D、E为短周期元素,F为第四周期元素,F还是前四周期中电负性最小的元素。已知:A原子的核外电子数与电子层数相等;B元素原子的核外p电子数比s电子数少1个;C原子的第一至第四电离能为I1=738kJ/mol,I2=1451kJ/mol,I3=7733kJ/mol,I4=10540kJ/mol;D原子核外所有p轨道为全充满或半充满;E元素的族序数与周期序数的差为4;
(1)写出E元素在周期表位置________________;D元素的原子的核外电子排布式________________;
(2)某同学根据题目信息和掌握的知识分析C的核外电子排布为__________________;该同学所画的轨道式违背了__________________;
(3)已知BA5为离子化合物,写出其电子式__________________;
(4)DE3中心原子杂化方式为_____________,其空间构型为____________;
高二化学填空题中等难度题查看答案及解析
-
(10分)已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E的+1价阳离子的核外有3层电子且各层均处于全满状态。
(1)E元素基态原子的核外电子排布式为___________________。
(2)B、C、D三种元素的第一电离能由小到大的顺序为______(填元素符号),其原因是____________。
(3)B2A4是石油炼制的重要产物之一 。B2A4分子中B原子轨道的杂化类型为________;1 mol B2A2分子中含________mol σ键。
高二化学填空题中等难度题查看答案及解析
-
(12分)
已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E的+1价阳离子的核外有3层电子且各层均处于全满状态。
(1)(2分)E元素基态原子的核外电子排布式为___________________。
(2)(4分)B、C、D三种元素的第一电离能由小到大的顺序为________(填元素符号)。其原因是_______________ 。
(3)(4分)已知D、E能形成晶胞结构如图所示的两种化合物,
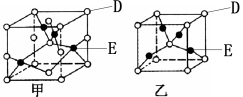
则化学式:甲为____________________,乙为______________________;
(4)(每空1分)B2A4是石油炼制的重要产物之一 。B2A4分子中B原子轨道的杂化类型为________;1 mol B2A2分子中含________mol σ键。
高二化学填空题困难题查看答案及解析
-
(10分)已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E的+1价阳离子的核外有3层电子且各层均处于全满状态。
(1)E元素基态原子的核外电子排布式为___________________。
(2)B、C、D三种元素的第一电离能由小到大的顺序为_______(填元素符号)。其原因是 。
(3)B2A4是石油炼制的重要产物之一 。B2A4分子中B原子轨道的杂化类型为________;1 mol B2A2分子中含________mol σ键。
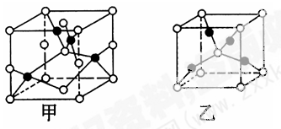
(4)已知D、E能形成晶胞结构如图所示的两种化合物,则化学式:甲为______,乙为______;高温时,甲易转化为乙的原因为______________________________。
高二化学填空题困难题查看答案及解析
-
已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L层上有2对成对电子;E+原子核外有3个电子层且M层3d轨道电子全充满。请回答下列问题:
(1)E元素基态原子的电子排布式为:__,该元素在周期表中属于__区元素。
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为:__(填元素符号)。
(3)下列表述中能证明氟元素电负性比D元素大的事实是__(填选项序号)。
A.HF比D的氢化物稳定
B.F2与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.D的单质与氢气化合时没有F2与氢气化合时剧烈
(4)写出由A、B、C三种元素形成的化合物ABC的结构式:__。
(5)写出一种由A、B、C、D四种元素形成的共价化合物的名称:__。
高二化学推断题中等难度题查看答案及解析
-
已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L层上有2对成对电子;E+离子核外有3层电子且M层3d轨道电子全充满。请回答下列问题:
(1)E元素基态原子的电子排布式为________。
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为________(填元素符号),其原因是________________________________________________________________________。
(3)D元素与氟元素相比,电负性:D________(填“>”“=”或“<”)F,下列表述中能证明这一事实的是______(填选项序号)。
A.常温下氟气的颜色比D单质的颜色深 B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态 D.比较两元素的单质与氢气化合时得电子的数目
(4)由A、C两元素可形成化合物CA5含有的化学键类型为________。
(5)B2A4是重要的石油化工原料,B2A4的结构式为________。B2A4通过聚合反应可以生成一种有机高分子化合物,反应方程式为________。
高二化学综合题中等难度题查看答案及解析
-
已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E的+1价阳离子的核外有3层电子且各层均处于全满状态。
(1)E元素基态原子的核外电子排布式为___________________。
(2)B、C、D三种元素的第一电离能由小到大的顺序为________(填元素符号), (3)B2A4是石油炼制的重要产物之一 。B2A4分子中B原子轨道的杂化类型为_________;1molB2A2分子中含σ键数目为________。
高二化学填空题简单题查看答案及解析