-
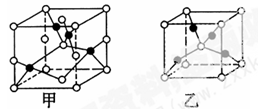
A、B、C、D、E是五种短周期元素。已知:它们的原子序数依次增大,A是元素周期表中原子半径最小的元素;B原子最外层电子数比其次外层电子数多2,C是E的邻族元素;D和E的原子序数之和为30,且D的族序数与周期数相等。甲、乙、丙、丁是它们两两形成的化合物,其中甲分子中含有18个电子。
| 物质组成 | 甲 | 乙 | 丙 | 丁 |
| 化合物中各元素 原子个数比 | A和C 1:1 | B和A 1:4 | D和E 1:3 | B和E 1:4 |
请回答下列问题:
(1)元素E在周期表中的位置为___________________________;
(2)把D的单质放到NaOH溶液中,反应的化学方程式为:_______________________;
(3)用电子式表示甲的形成过程:_________________________;
(4)在密闭容器中充入BC2、BC和乙的混合气体共mg,若加入足量Na2O2,充分振荡并不断用电火花点燃至反应完全,测得固体质量增重mg,则BC2与乙的体积比为________________;
(5)有200mL MgCl2和丙的混合溶液,其中c(Mg2+)= 0.2 mol· L-1,c(Cl-)= 1.3mol·L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4 mol·L-1 NaOH 溶液的体积是:______。
-
已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素.其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍.D、E为同主族元素,且E的原子序数为D的2倍.F元素在地壳中含量位于金属元素的第二位.试回答下列问题:
(1)F元素价层电子排布式为______.
(2)关于B2A2的下列说法中正确的是______.
A.B2A2中的所有原子都满足8电子结构
B.每个B2A2分子中σ键和π键数目比为1:1
C.B2A2是由极性键和非极性键形成的非极性分子
D.B2A2分子中的B-A键属于s-spσ键
(3)B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的空间构型是______.
(4)C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因______.
(5)A与D可以形成原子个数比分别为2:1,1:1的两种化合物X和Y,其中 Y含有______ 键(填“极性键”“非极性键”),A与C组成的两种化合物M和N所含的电子数分别与X、Y相 等,则M的电子式为______,N的结构式为______.
(6)E的氢化物的价层电子对互斥理论模型为______,E 原 子的杂化方式为______杂化.
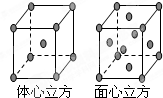
(7)F单质的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示.面心立方晶胞和体心立方晶胞的棱边长分别为acm、bcm,则F单质的面心立方晶胞和体心立方晶胞的密度之比为______,F原子配位数之比为______.
-
已知A、B、C、D、E、F、G都是元素周期表中前四周期的元素,它们的原子序数依次增大。A是宇宙中含量最丰富的元素,B、D原子的L层有2个未成对电子。E3+离子M层3d轨道电子为半满状态,F比E原子序数大1且位于同一族,G的最外层只有1个电子。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)写出E的电子排布式____________,E位于周期表____区。
(2)B、C、D的第一电离能由小到大的顺序为___________。
(3)A、B、D三种元素可以形成组成为A2BD、A4BD、A2BD2的分子,其中B原子采取sp3 杂化的是_________(填结构简式)
(4) 的空间构型为___________,键角为_______。
的空间构型为___________,键角为_______。
(5)F可形成分子式均为F(NH3)5BrSO4的两种配合物,其中一种化学式为[F(NH3)5Br]SO4往其溶液中加BaCl2溶液时,现象是_______;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时产生淡黄色沉淀,则第二种配合物的化学式为_______
(6)B元素在自然界有多种同素异形体,硬度最大晶体中每个晶胞中平均含有___个B原子。若晶胞的棱长为acm,则它的密度为____g/cm3(NA表示阿伏加德罗常数)
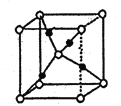
(7)G的一种氧化物M的晶胞结构如图所示(小圆圈代表氧原子),则M的化学式为________,该晶体中氧原子的配位数为_______。
-
已知 A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数, A的原子半径小于B,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素。E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子。
(1)基态E原子的价电子排布图_______________。
(2)B、C、D三元素第一电离能由大到小的顺序为(用元素符号表示)______________。
(3)BD 中心原子杂化轨道的类型为______杂化;CA
中心原子杂化轨道的类型为______杂化;CA 的空间构型为_______(用文字描述)。
的空间构型为_______(用文字描述)。
(4)1 mol BC-中含有π键的数目为______。
(5)比较D、E元素最简单氢化物的稳定性_______(填化学式,用“>”连接),理由是_______________。
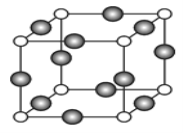
(6)C、F两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是____,C原子的配位数是_____。若相邻C原子和F原子间的距离为anm,阿伏伽德罗常数为NA,则该晶体的密度为______g/cm3(用含a、NA的符号表示)。
-
已知A、B、C、D、E是短周期原子序数依次增大的五种元素,A原子在元素周期表中原子半径最小,B与E同主族,且E的原子序数是B的两倍,C、D是金属,它们的氢氧化物均难溶于水。下列说法不正确的是( )
A. 单质D可用于冶炼某些难熔金属
B. 工业上常用电解法制得C和D的单质
C. 稳定性:A2B>A2E
D. 简单离子的半径:C>D>E>B
-
已知A、B、C、D、E是短周期原子序数依次增大的5种元素,A原子在元素周期表中原子半径最小,B与E同主族,且E的原子序数是B的两倍,C、D是金属,它们的氢氧化物均难溶于水。下列说法错误的是
A. 稳定性:A2B>A2E B. 工业上常用电解法制得C和D的单质
C. 简单离子的半径:C>D>E>B D. 单质D可用于冶炼某些难熔金属
-
已知A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素。E是第四周期元素且最外层只有2对成对电子,F元素与Cr元素位于同一周期的副族元素中且基态原子的最外层电子数与Cr原子相同。
(1)B、C、D三元素第一电离能由大到小的顺序为 (用元素符号表示)
(2)BD32-中心原子杂化轨道的类型为________杂化;CA4+的空间构型为______________。
(3)基态E原子的价电子排布图______________________________。
(4)1mol BC-中含有π键的数目为______________。
(5比较D、E元素最简单氢化物的沸点高低: (用化学式表示)。
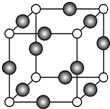
(6)C、F两元素形成的某化合物的晶胞结构如图所示,顶点为C原子。则该化合物的化学式是 ,C原子的配位数是 。若相邻C原子和F原子间的距离为a cm,阿伏伽德罗常数为NA,则该晶体的密度为________________g/cm3(用含a、NA的符号表示)。
-
X、Y、Z、R和W代表原子序数依次增大的5种短周期元素,X元素原子最外层电子数比次外层电子数多2,R与Y同主族,W元素族序数等于周期数的2倍。已知常温下:W氢化物(气态)+Z单质(气态)=Z氢化物(液态)+W单质(固态)。下列说法正确的是
A.Y、W元素氧化物对应的水化物一定是强酸
B.R元素位于第二周期第VA族
C.稳定性:Z氢化物>W氢化物
D.原子半径从小到大:Z<X<Y<R
-
位于短周期的四种元素A、B、C、D,它们的原子序数依次增大,已知A、C位于同一主族,A在周期表中原子半径最小。B、D的最外层电子数相等,且B、D的原子序数之和为A、C原子序数之和的两倍。回答下列问题:
(1)上述元素可以形成多种具有漂白性的物质,请写出任意两种物质的化学式:_________,______________;
(2)C与D形成D的最低价化合物的电子式:_________ ;
(3)写出C与水反应的离子方程式:______________________________;
(4)A、B组成的物质E可形成甲、乙两种微粒,它们均有10个电子。写出E生成甲、乙的方程式:_________________________________________。
-
已知前四周期A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态;D原子L电子层上有2对成对电子;E基态原子有6个未成对电子:
请填写下列空白:
(1)E元素在元素周期表的位置是______,E元素基态原子的价电子排布式为_____;
(2)C基态原子的价层电子的轨道表达式______;
(3)B2A4是重要的基本石油化工原料。1molB2A4分子中含_____molσ键;
(4)BD2电子式为_____,此分子键角为_______;
(5)BD32-中心原子孤电子对数为______,离子的立体构型为______;
(6)B、C、D三种元素的第一电离能由小到大的顺序为______(填元素符号),其原因为______。
中含________mol σ键。
为______,乙为______;高温时,甲易转化为乙的原因为______________________________。