-
电化学在我们的生产生活中占有越来越重要的地位。
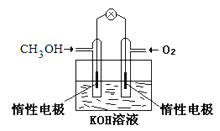
(1)①燃料电池是一种绿色环保、高效的化学电源。上图为甲醇燃料电池,则负极反应式为____。
②用甲醇燃料电池电解300mL饱和食盐水,则电解的化学方程式为_________。电解一段时间后,当溶液的pH值为13时,消耗O2的质量为______g。(忽略溶液体积变化,不考虑损耗)
③用甲醇燃料电池电解2L,1mol/L硫酸铜溶液,一段时间后:两极共收集到标准状况下的气体89.6L,则电路中共转移_______mol电子。
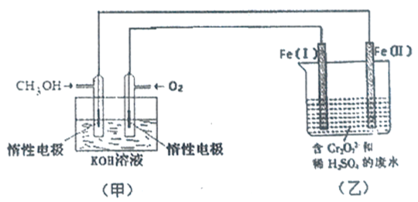
(2)利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来处理含Cr2O72-废水,如下图所示;电解过程中溶液发生反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。

①甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用,则石墨Ⅱ附近发生的电极反应式为__。
②向完全还原为Cr3+的乙池工业废水中滴加NaOH溶液,可将铬以Cr(OH)3沉淀的形式除去,已知Cr(OH)3存在以下溶解平衡:Cr(OH)3(s) Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Ksp=c(Cr3+)•c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol•L-1,溶液的pH应调至________。
Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Ksp=c(Cr3+)•c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol•L-1,溶液的pH应调至________。
-
电化学在生产生活中都具有重要的作用和意义。
(1)图1为绿色电源“二甲醚(CH3OCH3)燃料电池”的工作原理示意图,该电池的负极反应式为_________。
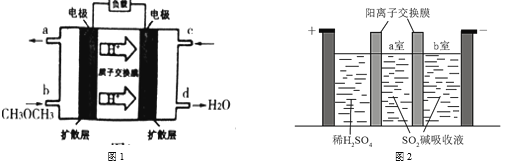
(2)制备焦亚硫酸钠(Na2S2O5)可采用三室膜电解技术,装置如图2所示,其中SO2碱吸收液中含有NaHSO3和Na2SO3。阳极的电极反应式为_______。电解后,____室的NaHSO3浓度增加。将该室溶液进行结晶脱水,可得到Na2S2O5。
(3)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问题:
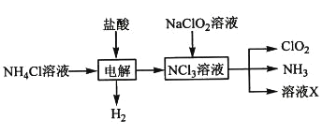
实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2,电解时发生反应的化学方程式为________________。溶液X中大量存在的阴离子有________________。
(4)测定混合气中ClO2的含量:
Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入3 mL稀硫酸。将一定量的混合气体通入混合溶液中充分吸收。
Ⅱ.用0.1000 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-=2I-+S4O62-),以淀粉溶液为指示剂显示终点时共用去20.00 mL硫代硫酸钠溶液。
①锥形瓶内ClO2与碘化钾反应的离子方程式为__________________。
②测得混合气中ClO2的质量为______。
③测定混合气中ClO2的含量的操作中可能使测定结果偏低的是____(填字母)。
a.滴定管未润洗就直接注入硫代硫酸钠标准液
b.滴定管读取标准液体积时,开始仰视读数,滴定结束时俯视读数
c.锥形瓶用蒸馏水洗净后没有干燥
-
电池在生产、生活中应用越来越广泛。下列说法错误的是
A.化学电源有一次电池、可充电电池和燃料电池等,一次电池只能放电,不能充电
B.铅蓄电池应用广泛,主要优点是单位重量的电极材料释放的电能大
C.燃料电池具有能量利用率高、可连续使用和污染轻等优点
D.锂电池是一种高能电池,体积小、重量轻,单位质量能量比高
-
电池在生产、生活中应用越来越广泛。下列说法错误的是
A.化学电源有一次电池、可充电电池和燃料电池等,一次电池只能放电,不能充电
B.铅蓄电池应用广泛,主要优点是单位重量的电极材料释放的电能大
C.燃料电池具有能量利用率高、可连续使用和污染轻等优点
D.锂电池是一种高能电池,体积小、重量轻,单位质量能量比高
-
(14分)电化学原理在现代生产生活中有着重要应用。
⑴燃料电池是目前发展势头强劲的优秀绿色环保电池。某新型氢氧燃料电池以H2为燃料,O2为氧化剂,H2SO4溶液为电解液),写出该电池的总反应方程式:________。
⑵铝电池性能优越,Al—AgO电池可用作水下动力电源,该电池反应的原理为:
Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O。

①该电池反应的负极电极反应式________。
②图中隔膜为阴离子交换膜,溶液中OH-通过向________极移动(选填“正”或“负”)。
用Al—AgO电池作为电源,使用Pt电极电解500mL饱和NaCl溶液,电解一段时间后,恢复至室温,所得溶液pH=13(假设NaCl溶液足量且电解前后体积不变)。
③使用Pt电极电解NaCl溶液的离子方程式________;
电解过程中放出氢气的体积(标准状况下)为________L。
④若电池的效率为50%,该过程中消耗金属铝的质量为________g。
⑶用电解法制取镁时,若原料氯化镁含有水时,在电解温度下,原料会形成Mg(OH)Cl,并发生电离:Mg(OH)C1 = Mg(OH)+ + C1一。
电解时在阴极表面会产生氧化镁钝化膜,此时阴极的反应式为________。
-
某化学兴趣小组在实验室利用质子酸甲醇燃料电池作电源,电解硫酸铜溶液。
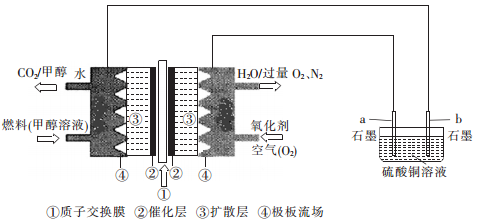
请回答下列问题:
(1)通入氧气的电极为______(填“正极”或“负极”),通入甲醇一极的电极反应式为_________。
(2)b电极上的现象为________________。
(3)假设硫酸铜溶液的体积为600 mL(电解前后溶液的体积变化忽略不计),若消耗336 mL(标准状况)O2,则电解后硫酸铜溶液的pH为________。
(4)若a、b均换成铜电极,则电解一段时间后硫酸铜溶液的浓度________(填“增大”“减小”或“不变”)。
-
过氧化氢和臭氧都是常见的绿色氧化剂,在工业生产中有着重要的用途。
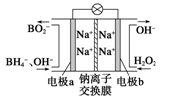
(1)据报道以硼氢化合物NaBH4(B为+3价)和H2O2作原料的燃料电池,可用作通信卫星电源。负极材料采用Pt或C,正极材料采用MnO2,其工作原理如图所示。该电池放电时正极的电极反应式为_________________________;MnO2除了作正极材料外,还可能对电极反应具有_________________作用。
(2)火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂。已知:
N2H4(l)+O2(g)===N2(g)+2H2O(g),ΔH=-534 kJ·mol-1
H2O2(l)===H2O(l)+O2(g),ΔH=-98 kJ·mol-1
H2O(l)===H2O(g),ΔH=+44 kJ·mol-1
试写出N2H4和液态H2O2反应生成气态水的热化学方程式___________________。
(3)O3可由臭氧发生器(原理如右图所示)电解稀硫酸制得。

①图中阴极为___________(填“A”或“B”)。
②若C处不通入O2,A极的电极反应式为_________________。
③若C处通入O2 ,则A极的电极反应式为_________________。
(4)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+O3(g) NO2(g)+O2(g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应,正反应速率随时间变化的示意图如图所示。由图可得出的正确说法是________。
NO2(g)+O2(g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应,正反应速率随时间变化的示意图如图所示。由图可得出的正确说法是________。

a.反应在c点达到平衡状态
b.反应物浓度:b点小于c点
c.该反应为放热反应
d.Δt1=Δt2时,NO的转化量:a~b段小于b~c段
-
(18分)
(1)氢气被看做是理想的“绿色能源”。用高压氢气、氧气制作氢氧燃料电池是利用氢能的一种重要方式。请写出氢氧燃料电池(电解质溶液为KOH溶液)的电极反应式。
正极 ;
负极 。
(2)电解原理在化学工业中有广泛应用。下图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

①Y的电极名称是 (填写“阳极”或“阴极”)。
②若X、Y都是惰性电极,a是饱和食盐水,实验开始时,同时在两边各滴入几滴酚酞试液,一段时间后,在X极附近观察到的现象是 ,如何检验Y极上的产物: 。(试剂及现象)
(3)若X、Y都是惰性电极,a是CuSO4溶液,电解一段时间后,阳极上产生气体的体积为4.48L(标 准状况下),则阴极上析出金属的质量为 g。
(4)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是 ,Y电极的材料是 。
(5)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是 。
| 方案 | X | Y | a溶液 |
| A | 铁 | 银 | AgNO3 |
| B | 铁 | 银 | Fe(NO3)3 |
| C | 银 | 铁 | AgNO3 |
| D | 银 | 石墨 | AgNO3 |
-
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A. 氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH-
B. 铅蓄电池充电时,标示“+”的接线柱连电源的正极,电极反应式为:PbSO4(S) - 2e-+2H2O(l)═PbO2(S)+4H+(aq)+SO42-(aq)
C. 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-═Cu2+
D. 钢铁发生电化学腐蚀的正极反应式:Fe-2e-═Fe2+
-
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A.氢氧燃料电池的负极反应式:O2 + 2H2O + 4e- = 4OH -
B.铅蓄电池充电时,标示“+”的接线柱连电源的正极,电极反应式为:PbSO4(S) -2e - + 2H2O(l)=PbO2(S) + 4H+(aq)+ SO42-(aq)
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e- = Cu2+
D.钢铁发生电化学腐蚀的正极反应式:Fe-2e - = Fe2+
 废水,如上图所示。
废水,如上图所示。 Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Kgp=c(Cr3+).c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至______________。
Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Kgp=c(Cr3+).c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至______________。







