-
已知五种短周期元素的原子序数的大小顺序为C>A>B>D>E;其中E元素为原子半径最小的元素,且A、C同周期,B和C同主族;A与B可形成离子化合物A2B,其含有的离子具有相同的电子层结构,且电子总数为30;D和E可形成4核10电子分子,该分子可使湿润的红色石蕊试纸变蓝。试回答下列问题:
(1)C元素的元素符号为________;
(2)B、D元素的第一电离能大小关系为:B_____D(填“<”、“>”或“=”);
(3)写出D元素形成的单质的结构式为______________,其中σ键:π键=______。
(4)A2B对应的水化物的碱性比LiOH _______(填“强”或“弱”);化合物A2B2属于_______(选“离子”或“共价”)化合物,写出A2B2的电子式_________________,A2B2溶于水时发生反应的化学方程式为__________________________________________________
(5)化合物E2B、E2C,它们结构与组成相似,热稳定性更强的是__________(填化学式)
但E2B的沸点比E2C高得多的原因是___________________________________。
高二化学综合题中等难度题查看答案及解析
-
X、Y、Z均为第三周期元素,X的第一电离能在同周期中最小,Y的电负性在同周期中最大,Z的离子半径在同周期中最小,下列关于X、Y、Z叙述中不正确的是 ( )
A. 原子序数和原子半径大小顺序均为:X<Y<Z
B. 元素X与元素Y能形成离子化合物
C. 元素Z最高价氧化物对应水化物具有两性
D. 元素Y形成的气态氢化物水溶液呈强酸性
高二化学单选题中等难度题查看答案及解析
-
X、Y、Z均为第三周期元素,X的第一电离能在同周期中最小,Y的电负性在同周期中最大,Z的离子半径在同周期中最小,下列关于X、Y、Z叙述中不正确的是 ( )
A.原子序数和原子半径大小顺序均为:X<Y<Z
B.元素X与元素Y能形成离子化合物
C.元素Z最高价氧化物对应水化物具有两性
D.元素Y形成的气态氢化物水溶液呈强酸性
高二化学选择题简单题查看答案及解析
-
短周期元素X、Y、Z、W的原子序数依次增大,X是原子半径最小的元素,Y原子最外层电子数是次外层的3倍;Z与X处于同一主族,W的原子序数是Y的2倍。下列叙述不正确的是( )
A. 原子半径的大小顺序:r(Z)>r(W)>r(Y)>r(X)
B. Y的气态氢化物的热稳定性比W的弱
C. X、Y两种元素可形成化合物X2Y、X2Y2
D. Z、W两种元素最高价氧化物对应的水化物之间能发生反应
高二化学单选题中等难度题查看答案及解析
-
A元素的阴离子、B元素的阴离子和C元素的阳离子具有相同的电子层结构。已知A的原子序数大于B的原子序数。则根据元素周期律可知:A、B、C三种原子半径大小的顺序是( )
A. A > B > C B. B > A > C C. C > A > B D. C > B > A
高二化学单选题中等难度题查看答案及解析
-
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,已知:四种原子最外层电子数之和为24。下列说法正确的是
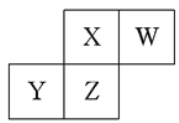
A.元素Ⅹ和元素Z的最高正化合价相同
B.单核阴离子半径的大小顺序为:r(W)>r(X)
C.气态简单氢化物的热稳定性顺序为:Y<Z<X<W
D.元素Z的氧化物对应水化物都是强酸
高二化学单选题中等难度题查看答案及解析
-
短周期元素X、Y、Z、W 的原子序数依次增大,且原子最外层电子数之和为13。X 的原子半径比Y 的小,X 与W 同主族,Z 是地壳中含量最高的元素。下列说法正确的是( )
A. 原子半径的大小顺序: r(Y)>r(Z)>r(W)
B. 元素Z、W 的简单离子的电子层结构不同
C. 元素Y 的简单气态氢化物的热稳定性比Z 的强
D. 只含X、Y、Z 三种元素的化合物,可能是离子化合物,也可能是共价化合物
高二化学单选题困难题查看答案及解析
-
短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13。X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素。下列说法正确的是
A.原子半径的大小顺序:r(Y)>r(Z)>r(W)
B.元素Z、W的简单离子的电子层结构不同
C.元素Y的简单气态氢化物的热稳定性比Z的强
D.只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物
高二化学选择题中等难度题查看答案及解析
-
.A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的电负性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是( )
A.A、B、C、D、E B.E、C、D、B、A
C.B、A、D、C、E D.C、D、A、B、E
高二化学选择题简单题查看答案及解析
-
A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的电负性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是( )
A.A、B、C、D、E B.E、C、D、B、A
C.B、A、D、C、E D.C、D、A、B、E
高二化学选择题简单题查看答案及解析