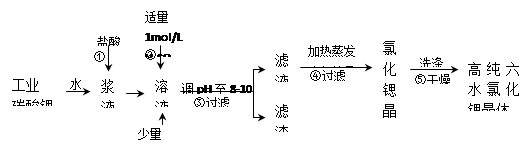-
一种工业制备SrCl2·6H2O的生产流程如下图所示:
已知:①M(SrCl2·6H2O)=267 g/mol;
②Ksp(SrSO4)=3.3×10-7、Ksp(BaSO4)=1.1×10-10;
③经盐酸浸取后,溶液中有Sr2+和Cl-及少量Ba2+。
(1)隔绝空气高温焙烧,若2 mol SrSO4中只有S被还原,转移了16 mol电子。写出该反应的化学方程式:______________________________ 。
(2)过滤2后还需进行的两步操作是_____、_____。
(3)加入硫酸溶液的目的是_____;为了提高原料的利用率,滤液中Sr2+的浓度应不高于_____ mol/L(注:此时滤液中Ba2+浓度为1×10-5 mol/L)。
(4)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×10-2 mol的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应的离子),待Cl-完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+ 以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是_____。
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为_____。
-
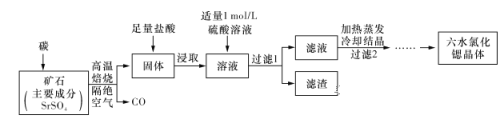
锶(Sr)为第五周期ⅡA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
已知:① 经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+杂质;
② SrSO4、BaSO4的溶度积常数分别为3.3×10-7、1.1×10-10;
③ SrCl2·6H2O的摩尔质量为:267 g/mol。
(1)天青石焙烧前先研磨粉碎,其目的是_________________________________________。
(2)隔绝空气高温焙烧,若0.5 mol SrSO4中只有S被还原,转移了4 mol电子。写出该反应的化学方程式:_____________________________________________。
(3)为了得到较纯的六水氯化锶晶体,过滤2后还需进行的两步操作是_______________。
(4)加入硫酸的目的是______________________。为了提高原料的利用率,滤液中Sr2+的浓度应不高于_________ mol/L(注:此时滤液中Ba2+浓度为1×10-5 mol/L)。
(5)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×10-2 mol的AgNO3溶液(溶液中除Cl―外,不含其它与Ag+反应的离子),待Cl―完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+ 以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是_________________________________________。
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为______________(保留4位有效数字)。
-
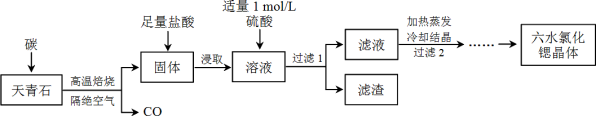
锶(Sr)为第五周期第ⅡA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
已知:①经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+杂质
②SrSO4、BaSO4的溶度积常数分别为3.3×10-7、1.1×10-10
③SrCl2·6H2O的摩尔质量为267 g·mol-1
(1)工业上天青石焙烧前先研磨粉碎,其目的是___
(2)工业上天青石隔绝空气高温焙烧,若0.5 mol SrSO4中只有硫元素被还原,转移了3 mol电子。写出该反应的化学方程式____
(3)加入硫酸的目的是_____;为了提高原料的利用率,滤液1中Sr2+的浓度应不高于__________mol·L-1(注:此时滤液1中Ba2+浓度为1×10-5 mol·L-1 )。
(4)滤渣1的主要成分是____________,滤液1经蒸发浓缩、冷却结晶、过滤后,需对所得的六水氯化锶晶体进行洗涤、干燥。证明六水氯化锶晶体已洗涤干净的实验操作及现象为___________
(5)工业上常通过电解熔融SrCl2制锶单质。由SrCl2·6H2O制取氯化锶的方法是_________
-
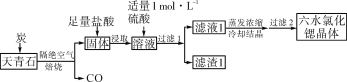
锶(Sr)为第五周期ⅡA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
已知:①经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+杂质;
②SrSO4、BaSO4的溶度积常数分别为3.3×10-7、1.1×10-10;
③SrCl2·6H2O的摩尔质量为267 g/mol。
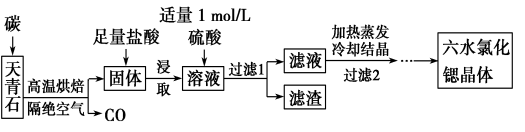
(1) 工业上天青石焙烧前先研磨粉碎,其目的是______________。
(2) 工业上天青石隔绝空气高温焙烧,若0.5 mol SrSO4中只有S被还原,转移了4 mol电子。写出该反应的化学方程式:_________________________。
(3)加入硫酸的目的是____________________________。为了提高原料的利用率,滤液中Sr2+的浓度应不高于___________mol/L(注:此时滤液中Ba2+浓度为1×10-5 mol/L)。
(4)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×10-2mol的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应的离子),待Cl-完全沉淀后,用含Fe3+的溶液作指示剂,用0.200 0 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是_______________________。
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为______________(保留4位有效数字)。
(5)工业上常用电解熔融SrCl2制锶单质。由SrCl2·6H2O制取无水氯化锶的方法是 。
-
锶(Sr)为第五周期IIA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
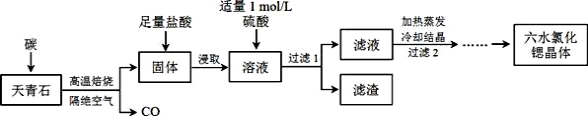
(1)SrCl2的电子式为_____________。
(2)工业上天青石隔绝空气高温焙烧,若0.5 mol SrSO4中只有S被还原,转移了4 mol电子。写出该反应的化学方程式:_______________________。
(3)加入硫酸的目的是______________________。为了提高原料的利用率,滤液中Sr2+的浓度应不高于_________ mol/L(注:此时滤液中Ba2+浓度为1×10-5mol/L;SrSO4和BaSO4溶度积常数依次为3×10-7、1×10-10。)
(4)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO31.100×10-2mol的AgNO3溶液(溶液中除Cl-外,不含其它与Ag+反应的离子),待Cl-完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是_______________________。
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为______________(保留4位有效数字)。
(5)工业上常用电解熔融SrCl2制锶单质。由SrCl2·6H2O制取无水氯化锶的方法是_________。
-
锶(Sr)为第五周期IIA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
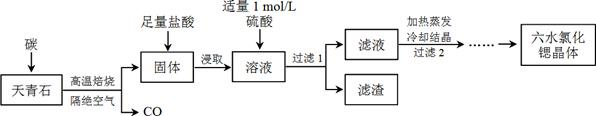
(1)工业上天青石焙烧前先研磨粉碎,其目的是_______________________________。
(2)工业上天青石隔绝空气高温焙烧,若0.5 mol SrSO4中只有S被还原,转移了4 mol电子。写出该反应的化学方程式:__________________________。
(3)加入硫酸的目的是____________________________。为了提高原料的利用率,滤液中Sr2+的浓度应不高于_________ mol/L[注:此时滤液中Ba2+浓度为1×10−5 mol/L,Ksp(BaSO4)=1.1×10−10,Ksp(SrSO4)=3.3×10−7]。
(4)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×10−2 mol的AgNO3溶液(溶液中除Cl−外,不含其它与Ag+反应的离子),待Cl−完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是_________________________。
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为______________(保留4位有效数字)。
(5)工业上常用电解熔融SrCl2制锶单质。由SrCl2·6H2O制取无水氯化锶的方法是____________。
-
六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主成分为SrSO4)为原料制备,生产流程如下:

(1)第①步反应前天青石先研磨粉碎,其目的是________________。
第③步加入适量稀硫酸的目的是_______________。
(2)第①步反应若0.5 mol SrSO4中只有S被还原,转移了4 mol电子。写出该反应的化学方程式:________________________________________。
(3)第④步操作依次是蒸发浓缩、冷却结晶、过滤、________、_______。
(4)称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×10-2 mol的AgNO3溶液(产品中不含其它与Ag+反应的离子),待Cl―完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的KSCN标准溶液滴定剩余的AgNO3,使剩余的Ag+ 以AgSCN白色沉淀的形式析出。若滴定过程用去上述浓度的KSCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为________(保留4位有效数字)。
-
锶(Sr)为第五周期第II A族元素。高纯六水氯化锶晶体(SrCl2·6H2O)具有很高的经济价值,用工业碳酸锶粉末(含少量钡、铁的化合物等杂质)制备高纯六水氯化锶晶体的过程如下图所示。
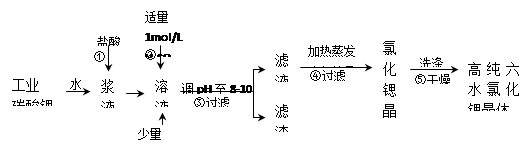
已知:SrCl2·6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。请回答:
(1)操作①加快反应速率的措施有 (任写一种方法)。碳酸锶与盐酸反应的离子方程式为________。
(2)加入少量30% H2O2溶液的发生反应的离子方程式为________。
(3)步骤③中调节溶液pH至8—10,宜选用的试剂为_______(填序号):
A.氨水 B.氢氧化钠 C. 氢氧化锶粉末 D.碳酸钠晶体
所得滤渣的主要成分是Fe(OH)3和________ (填化学式)。
(4)工业上用热风吹干六水氯化锶,选择的适宜温度范围是________ 。
A.50~60℃ B.70~80℃ C.80~100℃ D.100℃以上
(5)若滤液中Ba2+ 浓度为1×10-5mol/L,依下表数据推算出滤液中Sr2+物质的量浓度不大于________mol/L。
| SrSO4 | BaSO4 | Sr(OH)2 |
| Ksp | 3.3×10—7 | 1.1×10—10 | 3.2×10—4 |
-
锶(Sr)为第五周期IIA族元素,其化合物六水氯化锶(SrCl2•6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如图:
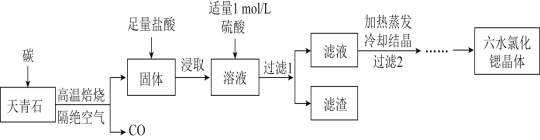
已知:①经盐酸浸取后的溶液中除含有Sr2+和Cl-外,还有少量的Ba2+杂质。
②BaSO4的溶度积常数为1.1×10-10,SrSO4的溶度积常数为3.3×10-7。
③SrCl2•6H2O的摩尔质量为267g/mol。
(1)工业上天青石焙烧前应先研磨粉碎,其目的是__。
(2)工业上天青石隔绝空气高温焙烧时,若0.5molSrSO4中只有S元素被还原,且转移了4mol电子。则该反应的化学方程式为__。
(3)浸取后加入硫酸的目的是 用离子方程式表示 __。为了提高原料的利用率,滤液中Sr2+的浓度应不高于__mol/L。
(注:此时滤液中Ba2+浓度为1.0×10-5mol/L)。
(4)产品纯度检测:称取1.000g产品溶解于适量水中,向其中加入含AgNO30.01mol的AgNO3溶液。溶液中除Cl-外,不含其它与Ag+反应的离子 ,待Cl-完全沉淀后,滴入1—2滴含Fe3+的溶液作指示剂,用0.2000mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出。已知:SCN-先与Ag+反应。
①滴定反应达到终点的现象是__。
②若滴定过程用去上述浓度的NH4SCN溶液20.00mL,则产品中SrCl2•6H2O的质量百分含量为___(保留3位有效数字)。
(5)由SrCl2•6H2O晶体制取无水氯化锶的主要仪器除了酒精灯、泥三角、三脚架外,还有___。
-
锶(Sr)为第五周期IIA族元素,其化合物六水氯化锶(SrCl2•6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如图:
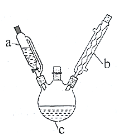
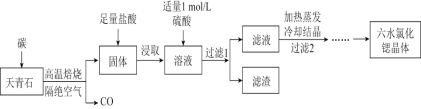
已知:①经盐酸浸取后的溶液中除含有Sr2+和Cl-外,还有少量的Ba2+杂质。
②BaSO4的溶度积常数为2.2×10-10,SrSO4的溶度积常数为3.3×10-7。
③SrCl2•6H2O的摩尔质量为267g/mol。
(1)工业上天青石焙烧前应先研磨粉碎,其目的是__。
(2)工业上天青石隔绝空气高温焙烧时,若0.5molSrSO4中只有S元素被还原,且转移了4mol电子。则该反应的化学方程式为__。
(3)浸取后加入硫酸的目的是___,用离子方程式表示___。
(4)产品纯度检测:称取2.000g产品溶解于适量水中,向其中加入含AgNO30.01mol的AgNO3溶液。溶液中除Cl-外,不含其它与Ag+反应的离子,待Cl-完全沉淀后,滴入1—2滴含Fe3+的溶液作指示剂,用0.2000mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出。已知:SCN-先与Ag+反应。
①滴定反应达到终点的现象是__。
②若滴定过程用去上述浓度的NH4SCN溶液20.00mL,则产品中SrCl2•6H2O的质量百分含量为___(请列出计算式,无需计算)。
(5)由SrCl2•6H2O晶体制取无水氯化锶的主要仪器除了酒精灯、泥三角、三脚架外,还有___。