-
以菱镁矿(主要成分为MgCO3,含少量FeCO3等)为原料制备高纯氧化镁的流程如下:
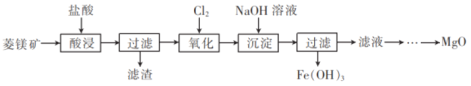
(1)采用搅拌、______、适当增大盐酸的浓度等措施可以提高“酸浸”率。
(2)“氧化”过程中发生反应的化学方程式为________。
(3)“沉淀”时需严格控制NaOH溶液的用量,其目的是________。
(4)“滤液”中继续加入NaOH溶液,______、________、灼烧,制得氧化镁。
(5)工业可用氯化镁和碳酸铵为原料,采用直接沉淀法制备纳米MgO,写出该反应的化学方程式:____。取少量制得的该物质溶于某种液体溶剂中(两者不反应),能说明有纳米MgO存在的简单方法是____。
-
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下,下列说法正确的是( )
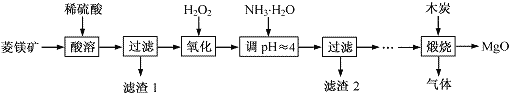
A. MgCO3与稀硫酸反应的离子方程式为CO32-+2H+=CO2↑+H2O
B. 加入H2O2氧化的离子方程式为Fe2+ + H2O2+2H+ =Fe3+ + 2H2O
C. 滤渣2的成分是Fe(OH)3 和Mg(OH)2
D. 流程图中过滤与煅烧之间有一系列的的实验操作,最后得到MgSO4·7H2O晶体,对MgSO4·7H2O晶体直接加热可以得到无水MgSO4固体
-
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下,下列说法正确的是( )

A. MgCO3与稀硫酸反应的离子方程式为CO32-+2H+=CO2↑+H2O
B. 加入H2O2氧化的离子方程式为Fe2+ + H2O2+2H+ =Fe3+ + 2H2O
C. 滤渣2的成分是Fe(OH)3 和Mg(OH)2
D. 流程图中过滤与煅烧之间有一系列的的实验操作,最后得到MgSO4·7H2O晶体,对MgSO4·7H2O晶体直接加热可以得到无水MgSO4固体
-
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为(MgCO3,舍少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
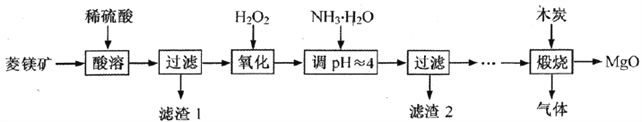
(1)加入H2O2氧化时,发生反应的化学方程式为___________________________。
(2)滤渣2的成分是_________(填化学式)。
煅烧过程存在以下反应:
2MgSO4+C 2MgO+2SO2↑+CO2↑;MgSO4+C
2MgO+2SO2↑+CO2↑;MgSO4+C MgO+SO2↑+CO↑;MgSO4+3C
MgO+SO2↑+CO↑;MgSO4+3C MgO+S↑+3CO↑。
MgO+S↑+3CO↑。
利用下图装置对煅烧产生的气体进行分步吸收或收集。
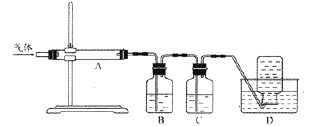
(3)D中收集的气体是__________(填化学式)。
(4)B中盛放的溶液是_________(填序号)。
a.NaOH溶液 b.Na2CO3溶液 c.稀硝酸 d..KMnO4溶液
(5)A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:_________________________
-
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为(MgCO3,舍少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
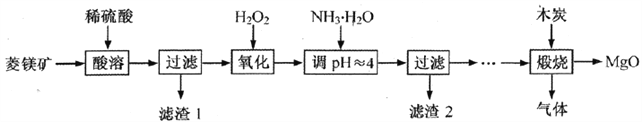
(1)加入H2O2氧化时,发生反应的化学方程式为___________________________。
(2)滤渣2的成分是_________(填化学式)。
煅烧过程存在以下反应:
2MgSO4+C 2MgO+2SO2↑+CO2↑;MgSO4+C
2MgO+2SO2↑+CO2↑;MgSO4+C MgO+SO2↑+CO↑;MgSO4+3C
MgO+SO2↑+CO↑;MgSO4+3C MgO+S↑+3CO↑。
MgO+S↑+3CO↑。
利用下图装置对煅烧产生的气体进行分步吸收或收集。

(3)D中收集的气体是__________(填化学式)。
(4)B中盛放的溶液是_________(填序号)。
a.NaOH溶液 b.Na2CO3溶液 c.稀硝酸 d..KMnO4溶液
(5)A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:_________________________
-
工业上以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备金属镁的实验流程如下:
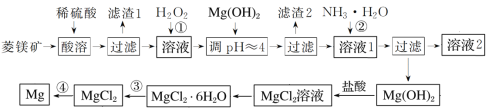
已知:一些金属离子转化为氢氧化物沉淀时溶液的pH如表所示
| Fe3+ | Al3+ | Fe2+ | Mg2+ |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 完全沉淀时 | 3.7 | 5.2 | 9.7 | |
请回答:
(1)如果没有过程①,后果是:__________________________________。
(2)上述流程中被循环使用的物质是:____________。
(3)滤渣2的主要成分为:____________;溶液2中的主要溶质为:_____________。
(4)通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,为保证Mg2+沉淀完全,过程②中控制溶液的pH至少为________。(保留小数点后一位)(已知Mg(OH)2的Ksp=2×10-11,lg2=0.3)
(5)已知MgCl2·6H2O受热时发生水【解析】
MgCl2·6H2O=Mg(OH)Cl+HCl↑+5H2O,过程③应该如何操作才能得到无水MgCl2?:_______________________________________________。
(6)写出过程④中发生反应的化学方程式:_____________________________________。
(7)为测定菱镁矿中铁的含量。称取12.5 g菱镁矿样品溶于过量的稀硫酸并完全转移到锥形瓶中,用0.010 mol·L—1H2O2溶液进行滴定。平行测定4组,消耗H2O2溶液的体积数据记录如下表所示。
| 实验编号 | 1 | 2 | 3 | 4 | 平均值 |
| 消耗H2O2溶液的体积/mL | 15.00 | 15.02 | 15.62 | 14.98 | |
①根据表中数据,可计算出菱铁矿中铁的质量分数为__________%。(保留两位小数)
②H2O2溶液应装在__________ 滴定管中(填“酸式”或“碱式”)
③误差
a.其它操作均正常,滴定终点时仰视读数会导致所测结果_________。
b.滴定之前没有排除滴定中的气泡会导致所测结果_________。
-
工业上以菱镁矿(主要成分为MgCO3含少量FeCO3)为原料制备金属镁的实验流程如下:
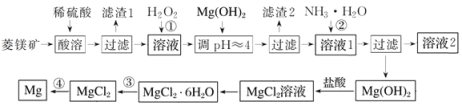
已知:一些金属离转化为氢氧化物沉淀时溶液的pH如表所示
| Fe3+ | Al3+ | Fe2+ | Mg2+ |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 完全沉淀时 | 3.7 | 5.2 | 9.7 | |
请回答:
(1)上述流程中H2O2的作用是:_____________
(2)滤渣2的主要成分为:_______________;溶液2中的主要溶质为:__________________。
(3)通常认为残留在溶液中的离子浓度小于1×10-5mol·L-1时就认为沉淀完全,为保证Mg2+沉淀完全,过程②中控制溶液的pH至少为__________________(保留小数点后一位)(已知Mg(OH)2的Ksp=2×10-11,lg2=0.3)
(4)已知MgCl2·6H2O受热时发生水解:MgCl2·6H2O=Mg(OH)Cl+HCl↑+H2O,过程③应该如何操作才能得到无水MgCl2__________________
(5)写出过程④中发生反应的化学方程式:____________________________________
-
以菱镁矿(主要成分为MgCO3、含少量FeCO3、SiO2)制备高纯氧化镁的流程如下图所示:
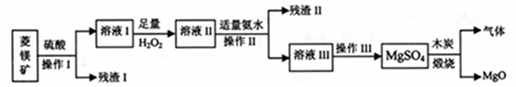
己知:25℃时,指示剂变色pH范围和几种氢氧化物的ksp及pH的关系如下表:
| 指示剂 | 酚酞 | 甲基酸 |
| 变色范围(pH) | 8.2-10.0 | 3.1-4.4 |
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀时pH | 1.1 | 5.9 | 8.4 |
| 沉淀完全时pH | 3.7 | 9.6 | 10.2 |
| 溶度积常数 | 4×10-34 | 8×10-16 | 2×10-13 |
(1)操作II和III中涉及的分离方法分别是____________、_______________。
(2)残渣I的主要成分是____________,加入H2O2的过程中可观察到的现象是___________,其中发生的离子反应方程式是_________________________。
(3)MgSO4和木炭在800℃煅烧时,只生成MgO和两种气体,将混合气体通入NaOH溶液时,气体被完全吸收。煅烧时发生反应的化学方程式是_____________。
(4)采用滴定法测定溶液II与加入氨水的最佳体积比,可以减少氨水的消粍和Mg2+的损失。实验中应选取_______________指示剂,加入氨水是为了沉淀溶液II中的___________离子,若终点时该离子浓度=1.0×10-5mol·L-1,则溶液III的 pH=_____________ (己知:lg2=0.3)。
-
硫酸镁晶体(MgSO4·7H2O)是一种重要的化工原料,可用作制革、炸药、造纸、瓷器等。以菱镁矿(主要成分是碳酸镁,含少量FeCO3和不溶性杂质)为原料制取硫酸镁晶体的流程如下:
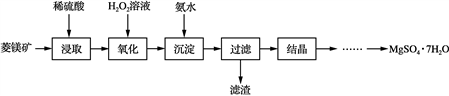
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Mg2+ | Fe2+ | Fe3+ |
| 开始沉淀 | 9.1 | 7.6 | 1.9 |
| 完全沉淀 | 11.1 | 9.7 | 3.2 |
(1) “氧化”步骤中,加入H2O2溶液的目的是________(用离子方程式表示)。“沉淀”步骤中,用氨水调节pH的范围是________。
(2) “过滤”所得滤液中含有的阳离子为Mg2+、________。
(3) “结晶”步骤中需蒸发浓缩滤液,使用的实验仪器有铁架台(含铁圈)、酒精灯、玻璃棒、____________________。
(4) 测定硫酸镁晶体样品中MgSO4·7H2O的含量常采用下列实验方法:
Ⅰ. 称取待测硫酸镁晶体样品1.500 g加入过量的EDTA,配成100 mL pH在9~10之间的溶液A。
Ⅱ. 移取25.00 mL溶液A于锥形瓶中,用0.1000 mol·L-1 Zn2+标准溶液与过量的EDTA反应,消耗Zn2+标准溶液20.00 mL。
Ⅲ. 另移取25.00 mL溶液A于另一只锥形瓶中,调节pH为5~6,用0.100 0 mol·L-1 Zn2+标准溶液与之充分反应,消耗Zn2+标准溶液35.00 mL。
已知:①pH为9~10时,Mg2+、Zn2+均能与EDTA(H2Y2-)反应:Mg2++H2Y2-===MgH2Y Zn2++H2Y2-===ZnH2Y
②pH为5~6时,Zn2+除与EDTA反应,还能与MgH2Y反应:Zn2++MgH2Y===ZnH2Y+Mg2+
③样品中杂质不参与反应。
计算硫酸镁晶体样品中MgSO4·7H2O的质量分数________。(写出计算过程)。
-
以菱镁矿(主要成分是碳酸镁,含少量FeCO3和不溶性杂质)为原料制取硫酸镁晶体(MgSO4·7H2O)的流程如图:

(1)“浸取”时通常将菱镁矿石进行粉碎,其目的是___。
(2)写出碳酸镁与稀硫酸反应的化学方程式___。
(3)“氧化”和“沉淀”是将“浸取”过程中产生的Fe2+转化为Fe(OH)3沉淀,则“过滤”所得滤液中含有的阳离子主要有___和___。











