-
[化学—选修3:物质结构与性质] 化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用。
(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7,其中1/3的Cu以罕见的Cu3+形式存在。Cu在元素周期表中的位置为____ ,基态Cu3+的核外电子排布式为_ _______。
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性。下列物质适合作录音磁带磁粉原料的为____(填选项字母)。
A. V2O5 B.CrO2 C.PbO D.ZnO
(3)屠呦呦因在抗疟药——青蒿素研究中的杰出贡献,成为首获科学类诺贝尔奖的中国人。青蒿素的结构简式如图l所示,其组成元素的电负性由大到小的顺序为 ;碳原子的杂化方式有____ 。
(4)“可燃冰”因储量大、污染小被视为未来石油的替代能源,由甲烷和水形成的“可燃冰”结构如图2所示。
①“可燃冰”中分子间存在的2种作用力为 。
②H2O的VSEPR模型为 ,比较键角的大小:H2O CH4(填“>”“<”或“=”),原因为 。
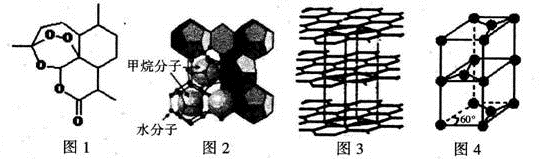
(5)锂离子电池在便携式电子设备以及电动汽车、卫星等领域显示出广阔的应用前景,该电池负极材料为石墨,石墨为层状结构(如图3),其晶胞结构如图4所示,该晶胞中有 个碳原子。已知石墨的层间距为apm,C-C键长为b pm,阿伏伽德罗常数的值为NA,则石墨晶体的密度为 g·cm-3(列出计算式)。
-
[化学—选修3:物质结构与性质] 化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用。
(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7,其中1/3的Cu以罕见的Cu3+形式存在。Cu在元素周期表中的位置为_______,基态Cu3+的核外电子排布式为____________。
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性。下列物质适合作录音磁带磁粉原料的为____(填选项字母)。
A.V2O5 B.CrO2 C.PbO D.ZnO
(3)屠呦呦因在抗疟药——青蒿素研究中的杰出贡献,成为首获科学类诺贝尔奖的中国人。青蒿素的结构简式如图l所示,其组成元素的电负性由大到小的顺序为___________;碳原子的杂化方式有_______。
(4)“可燃冰”因储量大、污染小被视为未来石油的替代能源,由甲烷和水形成的“可燃冰”结构如图2所示。
①“可燃冰”中分子间存在的2种作用力为________________。
②H2O的VSEPR模型为___________,比较键角的大小:H2O_______CH4(填“>”“<”或“=”),原因为___________________________________。
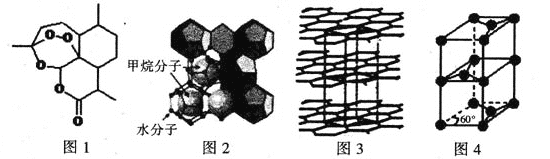
(5)锂离子电池在便携式电子设备以及电动汽车、卫星等领域显示出广阔的应用前景,该电池负极材料为石墨,石墨为层状结构(如图3),其晶胞结构如图4所示,该晶胞中有__________个碳原子。已知石墨的层间距为apm,C-C键长为b pm,阿伏伽德罗常数的值为NA,则石墨晶体的密度为_________________g·cm-3(列出计算式)。
-
[化学一选修3:物质结构与性质]化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用。
(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7,其中1/3的Cu以罕见的Cu3+形式存在。Cu在元素周期表中的位置为____ ,基态Cu3+的核外电子排布式为_ _______。
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性。下列物质适合作录音磁带磁粉原料的为____(填选项字母)。
A. V2O5 B.CrO2 C.PbO D.ZnO
(3)屠呦呦因在抗疟药——青蒿素研究中的杰出贡献,成为首获科学类诺贝尔奖的中国人。青蒿素的结构简式如图l所示,其组成元素的电负性由大到小的顺序为 ;碳原子的杂化方式为____ 。
(4)“可燃冰”因储量大、污染小被视为未来石油的替代能源,由甲烷和水形成的“可燃
冰”结构如图2所示。
①“可燃冰”中分子间存在的2种作用力为____。
②H20的VSEPR模型为____.,
比较键角的大小:H20 __CH4(填“>”“<”或“=”),原因为
该电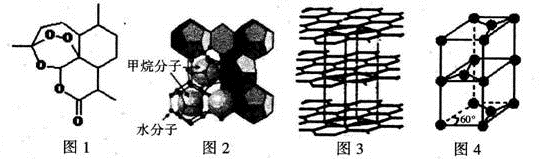
(5)锂离子电池在便携式电子设备以及电动汽车、卫星等领域显示出广阔的应用前景,池负极材料为石墨,石墨为层状结构(如图3),其晶胞结构如图4所示,该晶胞中有 个碳原子。已知石墨的层间距为apm,C-C键长为b pm,阿伏伽德罗常数的值为NA,则石墨晶体的密度为____g.cm-3(列出计算式)。
-
化学科学与技术在宇宙探索、改进生活、改善环境与促进发展方面均发挥着关键性的作用。下列说法正确的是
A. “玉兔号”月球车帆板太阳能电池的材料是氮化硅或二氧化硅
B. “乙醇汽油”、肼(N2H4)和水煤气的主要成分都是可再生能源
C. “神舟”和“天宮”系列飞船使用的碳纤维材料、光导纤维都是新型无机非金属材料
D. 所有糖类、油脂和蛋白质等营养物质在人体吸收后都能被水解利用
-
化学科学与技术在宇宙探索、改进生活、改善环境与促进发展方面均发挥着关键性的作用。正确的是
A. “玉兔号”月球车帆板太阳能电池的材料是氮化硅或二氧化硅
B. “乙醇汽油”、肼(N2H4)和水煤气的主要成分都是可再生能源
C. “神舟”和“天宮”系列飞船使用的碳纤维材料、光导纤维都是新型无机非金属材料
D. 所有糖类、油脂和蛋白质等营养物质在人体吸收后都能被水解利用
-
(14分)氨在国防、工农业等领域发挥着重要作用。
(1)工业以甲烷为原料生产氨气的过程如下:
①过程Ⅰ中,有关化学反应的能量变化如下图所示
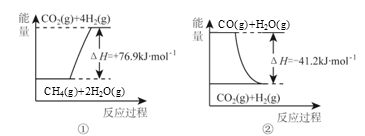
反应①为 反应(填“吸热”或“放热”),CH4 (g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式是 。
②CO可降低过程Ⅱ所用催化剂的催化效率,常用乙酸二氨合铜(Ⅰ)溶液吸收,其反应原理为:
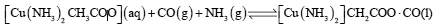 ,所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是 。(选填字母)。
,所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是 。(选填字母)。
a.高温、高压 b.高温、低压
c.低温、低压 d.低温、高压
③下表是过程Ⅱ中,反应物的量相同时,不同条件下平衡体系中氨的体积分数
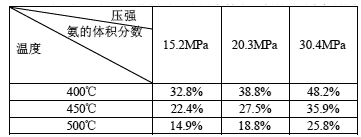
Ⅰ.根据表中数据,得出的结论是 。
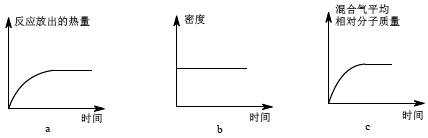
Ⅱ.恒温时,将N2和H2的混合气体充入2L密闭容器中,10分钟后反应达到平衡时n (N2)= 0.1mol,
n(H2)= 0.3mol。下列图象能正确表示该过程中相关量的变化的是 。(选填字母)。
(2)直接供氨式固体氧化物燃料电池能量转化率达85%,其结构示意图如图所示:
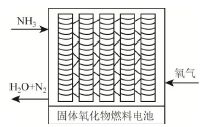
①负极的电极反应式是______。
②用该电池电解300ml的饱和食盐水。一段时间后,溶液pH=13(忽略溶液体积的变化),则消耗NH3溶液的体积是_____L。(标准状况)
-
自然界中时刻存在着含氮元素不同物质间的转化,实现氮按照一定的方向转化一直是科学领域研究的重要课题。氮气在催化剂作用下的一系列转化如图所示:
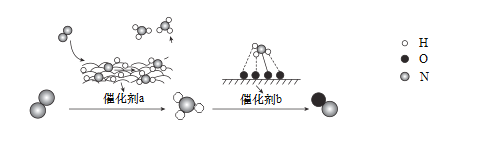
下列叙述正确的是
A.N2转化为NH3、NH3转化为NO均属于氮的固定
B.在催化剂a的作用下,氮原子发生了氧化反应
C.催化剂a、b表面均发生了极性共价键的断裂
D.催化剂a、b均可以提高单位时间内反应物的转化率
-
氨在国防、工农业等领域发挥着重要作用。工业以甲烷为原料生产氨气的过程如下:
(1)过程Ⅰ中,有关化学反应的能量变化如下图所示
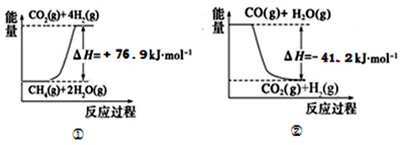
反应①为___________(“吸热”或“放热”),CH4(g)与H2O(g)反应生成CO(g)和H2 (g)的热化学方程式是________________。
(2)CO可降低过程Ⅱ所用催化剂的催化效率,常用乙酸二氨合铜(Ⅰ )溶液吸收,其反应原理为:[Cu(NH3)2CH3COO](aq)+CO(g)+NH3(g) [Cu(NH3)3]CH3COO•CO(1),
[Cu(NH3)3]CH3COO•CO(1), 
①N元素在周期表中的位置为__________,NH3的电子式为__________。
②所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是__________(选填字母)。
a.高温、高压 b.高温、低压 c.低温、低压 d.低温、高压
(3)合成NH3的反应为放热反应,如果该反应平衡时,只改变一个条件,再次达到新平衡时,平衡常数K值变大。关于该反应的说法正确的是__________(填字母序号)。
A.一定向正反应方向移动 B.在平衡移动时正反应速率先增大再减小
C.一定向逆反应方向移动 D.在平衡移动时逆反应速率先减小再增大
(4)400℃,28MPa时,将1molN2和3mol H2混合充入体积可变的密闭容器中,加入催化剂,10分钟后反应达到平衡时N2转化率为60%。该温度下的平衡常数Kp=__________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
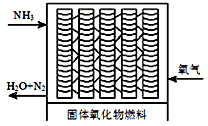
(5)一种直接供氨式固体氧化物燃料电池能量转化率达85%,其结构示意图如图所示:
①负极的电极反应式是_____________。
②用该电池电解300mL的饱和食盐水。一段时间后,溶液pH=13(忽略溶液体积的变化),则消耗NH3溶液的体积是_____L。(标准状况)
-
我们的生活离不开铁元素。从古至今,铁及其化合物在人类生产生活中的作用发生了巨大变化。
(1)古代中国四大发明之一的司南是由天然磁石制成的,其主要成分是______(填化学式)。
(2)现代利用铁的氧化物循环裂解水制氢气的过程如下图所示。

①已知:3FeO(s)+CO2(g) Fe3O4(s)+CO(g)△H1═ —19.3kJ•mol﹣1
Fe3O4(s)+CO(g)△H1═ —19.3kJ•mol﹣1
Fe3O4(s)+H2(g) 3FeO(s)+H2O(g)△H2═+57.2kJ•mol﹣1
3FeO(s)+H2O(g)△H2═+57.2kJ•mol﹣1
C(s)+CO2(g) 2CO(g)△H3═ +172.4kJ•mol﹣1
2CO(g)△H3═ +172.4kJ•mol﹣1
铁氧化物循环裂解水制氢气总反应的热化学方程式是
C(s)+H2O(g)═H2(g)+CO(g)△H═_____________ 。
②整个过程与温度密切相关,当温度低于570℃时,Fe3O4(s)和CO(g)反应得到的产物是Fe(s)和CO2(g),阻碍循环反应的进行。下图表示其他条件一定时,Fe3O4(s)和CO(g)反应达平衡时CO(g)的体积百分含量随温度的变化关系。
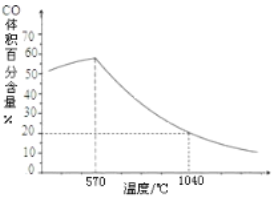
i.反应Fe3O4(s)+4CO(g) 3Fe(s)+4CO2(g)△H______0(填“>”、“<”或“=”),理由是______。
3Fe(s)+4CO2(g)△H______0(填“>”、“<”或“=”),理由是______。
ii.在低于570℃的某温度时,发生上述反应,增加CO浓度,C(CO)/C(CO2)比值_______(填“增大”“减小”“不变”)。
(3)①18世纪有一个名叫狄斯巴赫的德国人,他是制造和使用涂料的工人,因此对各种有颜色的物质都感兴趣。他实验合成出古老而神奇的蓝色染料普鲁士蓝。他的合成方法如下:
复分解反应ii的化学方程式为______。
②利用普鲁士蓝合成原理也可以用于检测食品中CN﹣,通过试纸变蓝与否则证明食品中含有CN﹣,检测过程方案如下:

FeSO4碱性试纸用于检测HCN的工作原理为__________________________。
-
2007年诺贝尔化学奖授予德国科学家格哈德•埃特尔,以表彰他在表面化学研究领域作出的开拓性贡献.物质接触表面发生的化学反应对工业生产运作至关重要.同时,表面化学研究有助于我们理解各种不同的过程.以下事实或现象与表面化学无密切关系的是( )

A.熔化的铝不易滴落下来
B.利用铁的表面作为催化剂用氮气和氢气合成氨
C.常温下,可以用铁、铝制做的容器来盛装冷的浓硫酸
D.CuSO4溶液中加入BaCl2溶液时产生白色沉淀
 27H2O +10MgO+3Al2O3写出该化合物作阻燃剂的两条依据:__________、__________。
27H2O +10MgO+3Al2O3写出该化合物作阻燃剂的两条依据:__________、__________。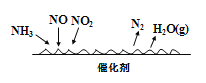




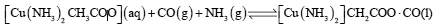 ,所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是
,所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是









