-
[化学—选修3:物质结构与性质] 化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用。
(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7,其中1/3的Cu以罕见的Cu3+形式存在。Cu在元素周期表中的位置为____ ,基态Cu3+的核外电子排布式为_ _______。
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性。下列物质适合作录音磁带磁粉原料的为____(填选项字母)。
A. V2O5 B.CrO2 C.PbO D.ZnO
(3)屠呦呦因在抗疟药——青蒿素研究中的杰出贡献,成为首获科学类诺贝尔奖的中国人。青蒿素的结构简式如图l所示,其组成元素的电负性由大到小的顺序为 ;碳原子的杂化方式有____ 。
(4)“可燃冰”因储量大、污染小被视为未来石油的替代能源,由甲烷和水形成的“可燃冰”结构如图2所示。
①“可燃冰”中分子间存在的2种作用力为 。
②H2O的VSEPR模型为 ,比较键角的大小:H2O CH4(填“>”“<”或“=”),原因为 。
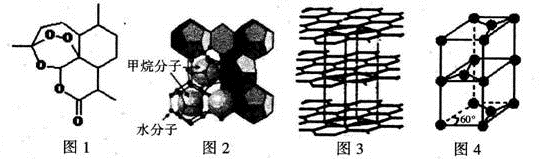
(5)锂离子电池在便携式电子设备以及电动汽车、卫星等领域显示出广阔的应用前景,该电池负极材料为石墨,石墨为层状结构(如图3),其晶胞结构如图4所示,该晶胞中有 个碳原子。已知石墨的层间距为apm,C-C键长为b pm,阿伏伽德罗常数的值为NA,则石墨晶体的密度为 g·cm-3(列出计算式)。
-
[化学—选修3:物质结构与性质] 化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用。
(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7,其中1/3的Cu以罕见的Cu3+形式存在。Cu在元素周期表中的位置为_______,基态Cu3+的核外电子排布式为____________。
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性。下列物质适合作录音磁带磁粉原料的为____(填选项字母)。
A.V2O5 B.CrO2 C.PbO D.ZnO
(3)屠呦呦因在抗疟药——青蒿素研究中的杰出贡献,成为首获科学类诺贝尔奖的中国人。青蒿素的结构简式如图l所示,其组成元素的电负性由大到小的顺序为___________;碳原子的杂化方式有_______。
(4)“可燃冰”因储量大、污染小被视为未来石油的替代能源,由甲烷和水形成的“可燃冰”结构如图2所示。
①“可燃冰”中分子间存在的2种作用力为________________。
②H2O的VSEPR模型为___________,比较键角的大小:H2O_______CH4(填“>”“<”或“=”),原因为___________________________________。
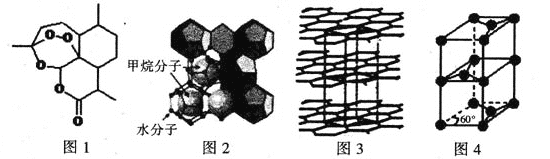
(5)锂离子电池在便携式电子设备以及电动汽车、卫星等领域显示出广阔的应用前景,该电池负极材料为石墨,石墨为层状结构(如图3),其晶胞结构如图4所示,该晶胞中有__________个碳原子。已知石墨的层间距为apm,C-C键长为b pm,阿伏伽德罗常数的值为NA,则石墨晶体的密度为_________________g·cm-3(列出计算式)。
-
[化学一选修3:物质结构与性质]化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用。
(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7,其中1/3的Cu以罕见的Cu3+形式存在。Cu在元素周期表中的位置为____ ,基态Cu3+的核外电子排布式为_ _______。
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性。下列物质适合作录音磁带磁粉原料的为____(填选项字母)。
A. V2O5 B.CrO2 C.PbO D.ZnO
(3)屠呦呦因在抗疟药——青蒿素研究中的杰出贡献,成为首获科学类诺贝尔奖的中国人。青蒿素的结构简式如图l所示,其组成元素的电负性由大到小的顺序为 ;碳原子的杂化方式为____ 。
(4)“可燃冰”因储量大、污染小被视为未来石油的替代能源,由甲烷和水形成的“可燃
冰”结构如图2所示。
①“可燃冰”中分子间存在的2种作用力为____。
②H20的VSEPR模型为____.,
比较键角的大小:H20 __CH4(填“>”“<”或“=”),原因为
该电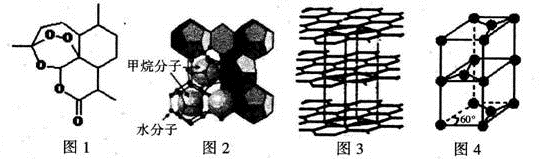
(5)锂离子电池在便携式电子设备以及电动汽车、卫星等领域显示出广阔的应用前景,池负极材料为石墨,石墨为层状结构(如图3),其晶胞结构如图4所示,该晶胞中有 个碳原子。已知石墨的层间距为apm,C-C键长为b pm,阿伏伽德罗常数的值为NA,则石墨晶体的密度为____g.cm-3(列出计算式)。
-
化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用,其中铁和铜是两种应用广泛的元素。
(1)基态铁原子的价电子轨道表达式为_____。
(2)磁性材料铁氧体在制备时常加入 CH3COONa、尿素[CO(NH2)2]等碱性物质。尿素分子中所含元素的电负性由小到大的顺序是_____,1mol 尿素分子中含有的 σ 键数目为_____。 CH3COONa 中碳原子的杂化类型为_________。
(3)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则 Fe(CO)5的晶体类型是_____,写出与CO互为等电子体的分子的电子式_____(任写一种)。
(4)CuO在高温时分解为 O2和 Cu2O,请从阳离子的结构来说明在高温时,Cu2O比 CuO更稳定的原因_____。
(5)磷青铜是含少量锡、磷的铜合金,某磷青铜晶胞结构如图所示:
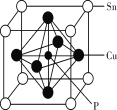
①其化学式为_____。
②若晶体密度为 8.82g/cm3,则最近的 Cu原子核间距为_____pm(用含 NA 的代数式表示)。
-
化学是一门以实验为基础的自然科学,是研究物质的性质的重要途径。某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。

已知:Na2SO3+H2SO4(浓) Na2SO4+SO2↑+H2O,请回答下列问题:
Na2SO4+SO2↑+H2O,请回答下列问题:
(1) 装置A中盛放浓硫酸的仪器名称是__________________。
(2) 实验过程中,C中的现象是____________,说明SO2具有_________性。
(3) 实验过程中,观察到装置B中出现了明显的白色沉淀。为探究该白色沉淀的成分,该小组同学进行了如下实验:
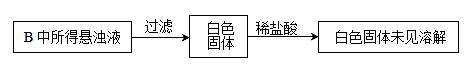
根据实验事实判断该白色沉淀的成分是_______________(填化学式),产生该白色沉淀的原因可能是_____________(填字母编号)。
a.BaSO3既不溶于水也不溶于酸
b.BaCl2溶液中可能溶解有氧气
c.BaCl2溶液中可能混有NaOH
d.由A制得的SO2气体中可能混有氧气
(4)如果将装置A中的浓H2SO4换作浓HNO3,对此实验是否有影响并说明理由_________________
-
[化学一选修3:物质结构与性质](15分)第四周期的过渡元素在工业、农业、科学技术以及人类生活等方面有重要作用。其中Ni-Cr-Fe合金是常用的电热元件材料。请回答:
(1)基态Ni原子核外电子排布式为_______;第二周期中基态原子未成对电子数与Ni相同且电负性大的元素为________。金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO) ,该分子呈正四面体构型。试推测Ni(CO)
,该分子呈正四面体构型。试推测Ni(CO) 的晶体类型为________,Ni(CO)
的晶体类型为________,Ni(CO) 易溶于下列_______(填选项字母)中。
易溶于下列_______(填选项字母)中。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(2)FeO、NiO晶体中r(Ni2+)和r(Fe2+)分别为69 pm和78 pm,则熔点NiO_________FeO(填“>”或“<”),原因为_____________;黄血盐是一种配合物,其化学式为K4[Fe(CN)6] ·3H2O,该配合物中配体的化学式为_________,黄血盐溶液与稀硫酸加热时发生非氧化还原反应,生成硫酸盐和一种与该配体互为等电子体的气态化合物,该反应的化学方程式为_______________。
(3)酸性高锰酸钾溶液能氧化硝基苯酚,邻硝基苯酚和对硝基苯酚在20 水中的溶解度之比为0.39,其原因为_________。
水中的溶解度之比为0.39,其原因为_________。
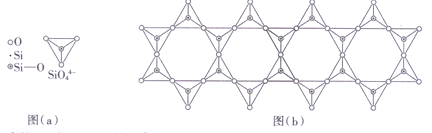
(4)在铬的硅酸盐中,SiO44-四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大结构型式。图(b)为一种链状结构的多硅酸根,其中Si原子的杂化形式为________,其化学式为_________。
-
化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用.
(1)如图实验没有错误的是______.
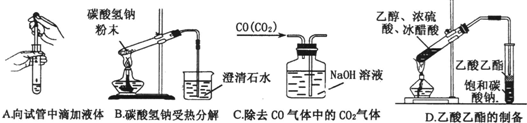
(2)如图为常见仪器的部分结构(有的仪器被放大)、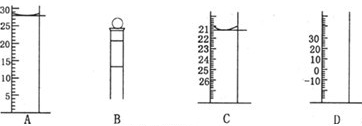
A图中液面所示溶液的体积为______mL,用上述四种仪器中的某种测量一液体的体积,平视时读数为NmL,仰视时读数为MmL,若M>N,则所使用的仪器是______(填字母标号).
(3)化学研究小组,通过网上查找资料发现,Cl2的制取有下列不同方案:
a、方案:加热条件下二氧化锰与浓盐酸反应制得C2
b、方案:浓盐酸与氯酸钾固体反应制得Cl2
c、方案:电解饱和食盐水法制得Cl2
现实验室有供选择的如下几种仪器来制取Cl2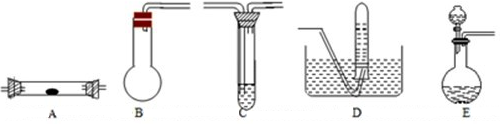
①用上述仪器不能实现的方案为______.不考虑固定装置的仪器,可行但缺仪器的方案是______,所缺的仪器是______.
若按b方案制Cl2时发生化学方程为______,
②若要设计联合实验探究氯气的漂白原理,从制备装置中产生氯气后应连接的装置中所使用的试剂或用品依次是______.
-
(化学——选修3:物质结构与性质)
2016年诺贝尔化学奖授予在“分子机器设计和合成”领域有突出成就的三位科学家,其研究对象之一“分子开关”即与大环主体分子苯芳烃、硫或氮杂环杯芳烃等有关。回答下列问题:
(1)对叔丁基杯[4]芳烃(如图Ⅰ所示)可用于ⅢB族元素对应离子的萃取,如La3+、Sc2+。写出基态二价钪离子(Sc2+)的核外电子排布式:________,其中电子占据的轨道数为________个。
(2)对叔丁基杯[4]芳烃由4个羟基构成杯底,其中羟基氧原子的杂化方式为________,羟基间的相互作用力为________。
(3)不同大小的苯芳烃能识别某些离子,如: 、SCN-等。一定条件下,SCN-与MnO2反应可得到(SCN)2,试写出(SCN)2的结构式______________________________。
、SCN-等。一定条件下,SCN-与MnO2反应可得到(SCN)2,试写出(SCN)2的结构式______________________________。
(4)NH3分子在独立存在时H-N-H键角为106.7°。如图 [Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因:______。
(5)橙红色的八羰基二钴[Co2(CO)8]的熔点为52℃,可溶于乙醇、乙醚、苯等有机溶剂。该晶体属于________晶体,八羰基二钴在液氨中被金属钠还原成四羰基钴酸钠[NaCo(CO)4],四羧基钴酸钠中含有的化学键为_________________。
(6)已知C60分子结构和C60晶胞示意图(如图Ⅱ、图Ⅲ所示):
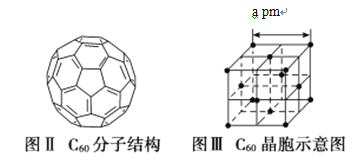
则一个C60分子中含有σ键的个数为________,C60晶体密度的计算式为________ g·cm-3。(NA为阿伏伽德罗常数的值)
-
C1化学又称一碳化学,研究以含有一个碳原子的物质为原料合成工业产品的有机化学及工艺,因其在材料科学和开发清沽燃料方面的重要作用已发展成为一门学科。燃煤废气中的CO、CO2均能转化为基础化工原料、清洁能源甲醇:
①3H2(g)+CO2(g)  CH3OH (g) + H2O(l) △H1
CH3OH (g) + H2O(l) △H1
②CO(g)+2H2(g)  CH3OH(g) △H2
CH3OH(g) △H2
Ⅰ.已知:18g水蒸气变成液态水放出44KJ的热量。
| 化学键 | C-H | C-O | C=O | H-H | O-H |
| 键能/KJ/mol | 412 | 351 | 745 | 436 | 462 |
则△H1_____________________
Ⅱ.一定条件下,在恒容的密闭容器中投入1molCO 和2mol H2,反应②在催化剂作用下充分反应,CH3OH在平衡混合气中的体积分数在不同压强下随温度的变化如图l所示:
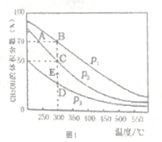
(1)图中压强的相对大小是P1______P2(填“>”“<”或“=”),判断的理由是________
(2)A、B、C三点的化学平衡常数的相对大小K(A)______K(B)_____ K(C)(填“>”“<”或“=”) ,计算C点的压强平衡常数Kp=__________(用平衡分压代替平衡浓度计算,分压=总压×体积分数)
(3)300℃,P2条件下,处于E点时V正________V逆(填“>”“<”或“=”)
(4)某温度下,不能说明该反应己经达到平衡状态的是______________。
a.容器内的密度不再变化
b. 速率之比v(CO):v(H2): v(CH3OH)=l: 2:l
c.容器内气体体积分数不再变化
d. 容器内混合气体的平均相对分子质量不再变化
e.容器内各组分的质量分数不再变化
(5)反应开始至在C点达平衡,各物质的浓度随时间变化曲线如图2所示,保持温度不变,t1时改变条件为_________,此时平衡_______。(填“正向移动”“逆向移动”“不移动” )
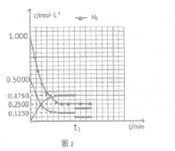
Ⅲ.工业上可通过甲醛羰基化法制取甲酸甲酯,25℃时,其反应的热化学方程式为:CH3OH(g)+CO(g)  HCOOCH3(g),部分研究如下图所示:
HCOOCH3(g),部分研究如下图所示:
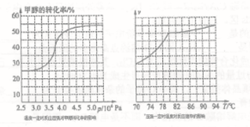
①根据反应体系的压强对甲醇转化率的影响并综合考虑生产成本因素的是_____(填下列序号字母)
a. 3.5×106Pa b. 4.0×106Pa c. 5.0×106Pa
②用上述方法制取甲酸甲酯的实际工业生产中,采用的温度是80℃,其理由是_______
-
下列说法不正确的是 ( )
A.人类使用的物质都是纯度越高越好
B.分子是保持物质化学性质的一种微粒,如果分子的组成或结构变了其化学性质就变了
C.定量研究的方法是化学发展为一门科学的重要标志
D.改变物质的性质不一定要通过化学变化













