-
某研究型学习小组的同学根据化学反应中的能量和速率变化对生产生活有着重要意义,进行下面的探究活动。
(1)甲同学为探究反应Fe+H2SO4(稀)=FeSO4+H2↑中的能量变化,向装有铁片的试管中滴加lmol/L的H2SO4,试管内产生气泡,触摸试管外壁,温度升高。
①该反应为______(填“放热” 或“吸热” ) 反应。
②下列措施中,能加快氢气生成速率的是______(填字母)。
a.将铁片改成铁粉 b. 将稀H2SO4改成浓硫酸 c.加硫酸钠溶液
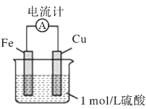
(2)乙学生依据原电池原理也可加快反应速率,设计了Fe与稀硫酸反应的装置图,观察到的现象是_____;铜片上发生反应的电极反应式为_____。
(3)丙同学根据4NH3+6NO 5N2+6H2O反应的发生条件,在老师的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能。若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。
5N2+6H2O反应的发生条件,在老师的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能。若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。

①写出实验室用固体混合物加热的方法制备 NH3的化学方程式________。
②为了比较不同催化剂的催化性能,需要测量并记录的数据是__________。
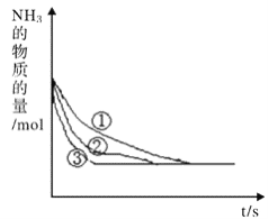
③在不同催化剂时测得混合气体中NH3的物质的量与时间的关系如下图,则曲线_______(填“①”或“②” 或“③”)使用的催化剂催化性能最好,理由是________。
-
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。某化学兴趣小组同学对氯气的性质进行如下探究:
(1)兴趣小组同学按下图装置进行实验,探究 Cl2 的漂白性。
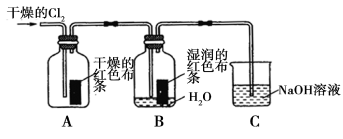
① 通 入Cl2 后 , 观 察 到 的 现 象 是 根 据 现 象 可 得 出 的 结 论是 。
②集气瓶 B发生反应的离子方程式是 。
③C装置的作用是 ,若有2.24L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子为 _mol。
(2)兴趣小组同学按下图装置进行实验,探究 Cl2 的氧化性。
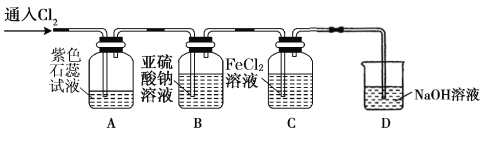
①实验开始后,观察装置 A 中的现象是 。
②装置 C 中发生反应的离子方程式是 。
③停止通入氯气,取装置 B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入 Cl2 时装置 B 中发生 反应的离子方程式是 。
-
(16分)氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。某化学兴趣小组同学对氯气的性质进行如下探究:
(1)兴趣小组同学按下图装置进行实验,探究Cl2的漂白性。
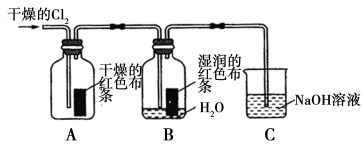
①通入Cl2后,观察到的现象是 根据现象可得出的结论是______。
②集气瓶B发生反应的离子方程式是______。
③C装置的作用是______,若有2.24 L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子数为________mol。
(2)兴趣小组同学按下图装置进行实验,探究Cl2的氧化性。
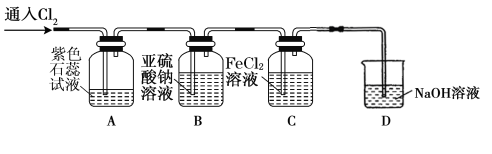
①实验开始后,观察装置A中的现象是: 。
②装置C中发生反应的离子方程式是 。
③停止通入氯气,取装置B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入Cl2时装置B中发生反应的离子方程式是 。
-
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。某化学兴趣小组同学对氯气的性质进行如下探究:
(1)兴趣小组同学按下图装置进行实验,探究Cl2的漂白性。
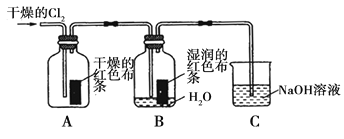
①通入Cl2 后,观察到的现象是 根据现象可得出的结论是 。
②集气瓶B发生反应的离子方程式是 。
③C装置的作用是 ,若有2.24L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子为 _mol。
(2)兴趣小组同学按下图装置进行实验,探究Cl2的氧化性。
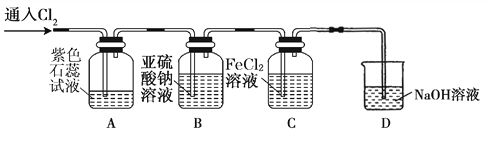
①实验开始后,观察装置A 中的现象是 。
②装置C中发生反应的离子方程式是 。
③停止通入氯气,取装置B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入Cl2时装置B中发生 反应的离子方程式是 。
-
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。某化学兴趣小组同学对氯气的性质进行如下探究:
(1)兴趣小组同学按下图装置进行实验,探究Cl2的漂白性。
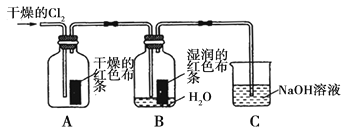
①通入Cl2 后,观察到的现象是 根据现象可得出的结论是 。
②集气瓶B发生反应的离子方程式是 。
③C装置的作用是 ,若有2.24L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子为 _mol。
(2)兴趣小组同学按下图装置进行实验,探究Cl2的氧化性。
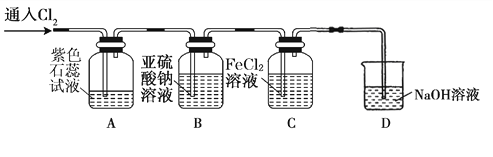
①实验开始后,观察装置A 中的现象是 。
②装置C中发生反应的离子方程式是 。
③停止通入氯气,取装置B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入Cl2时装置B中发生 反应的离子方程式是 。
-
在人类生产、生活所需能量日益增多的今天,研究化学反应及其能量变化对合理利用常规能源和开发新能源具有十分重要的意义。下列说法中不正确的是 ( )
A.任何化学反应都伴随着能量的变化
B.化学反应中的能量变化都表现为热量的变化
C.反应物的总能量高于生成物的总能量,反应释放能量
D.若化学键形成时释放的能量小于旧化学键被破坏时需要吸收的能量,反应吸收能量
-
在人类生产、生活所需能量日益增多的今天,研究化学反应及其能量变化对合理利用常规能源和开发新能源具有十分重要的意义。下列说法中不正确的是
A.任何化学反应都伴随着能量的变化
B.化学反应中的能量变化都表现为热量的变化
C.反应物的总能量高于生成物的总能量,反应释放能量
D.若化学键形成时释放的能量小于旧化学键被破坏时需要吸收的能量,反应吸收能量
-
在人类生产、生活所需能量日益增多的今天,研究化学反应及其能量变化对合理利用常规能源和开发新能源具有十分重要的意义。下列说法中不正确的是
A. 任何化学反应都伴随着能量的变化
B. 因地制宜开发利用风能、水能、地热能、潮汐能
C. 若化学键形成时释放的能量小于旧化学键被破坏时需要吸收的能量,反应吸收能量
D. 煤、石油天然气均为化石能源,是可再生能源
-
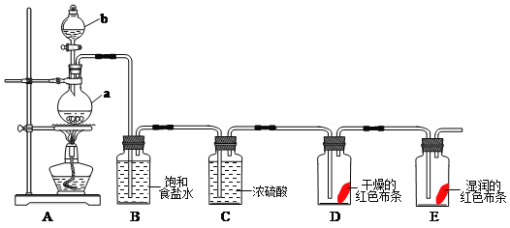
氯气是一种重要的化工原料,在工农业生产生活中有着重要的应用。某化学兴趣小组同学利用以下装置制备氯气并对氯气的性质进行探究:
(1)有关氯气、氯水和氯离子的性质,下列说法正确的是_____________
A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl2
B.Cl-和Cl2都具有很强的氧化性
C.新制氯水可以用来杀菌消毒是因为生成强酸 次氯酸
D.将新制氯水滴入AgNO3溶液,会出现白色沉淀
(2)仪器a的名称为___________,装置B中饱和食盐水的作用是_______________。
(3)装置A中发生反应的离子方程式为:____________________________________。
(4)装置D中的实验现象为__________________,装置E中的实验现象为________
(5)整套实验装置存在着明显缺陷,你的改进措施是__________________________。
(6)8.7gMnO2固体与足量浓盐酸充分反应,在标准状况下产生Cl2的体积为_____L;其中被氧化的HCl的物质的量为_______mol。
-
在人类生产、生活对能量的需求日益增长的今天,研究化学反应及其能量变化,对合理利用常规能源和开发新能源具有十分重要的意义。能源是人类赖以生存和发展不可缺少的因素。请完成下列问题:
(1)人类利用能源分为三个阶段,即________、________、________。
(2)矿物能源是现代人类社会赖以生存的重要物质基础。目前,全球仍主要处于化石能源时期。下列不属于化石能源的是________。(填序号,下同)
A.石油 B.煤 C.天然气 D.生物质能
(3)下列对能源的看法合理的是 ( )。
A.化石能源属于不可再生能源,只会越用越少
B.生物能是一种可再生能源,有广泛的前景
C.太阳能、氢能、核能、地热能都属于新能源
D.我国人口众多、资源相对匮乏、环境承载能力较弱,因此要建设节约型社会

 5N2+6H2O反应的发生条件,在老师的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能。若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。
5N2+6H2O反应的发生条件,在老师的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能。若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。









