-
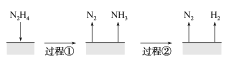
肼(N2H4)在不同条件下分解产物不同,200 ℃时在Cu表面分解的机理如图1。已知200 ℃时:
反应Ⅰ:3N2H4(g)=N2(g)+4NH3(g) ΔH1=-32.9 kJ/mol
反应Ⅱ:N2H4(g)+H2(g)=2NH3(g) ΔH2=-41.8 kJ/mol
下列说法不正确的是( )
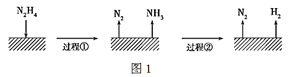
A.图1所示过程①是放热反应,②是吸热反应
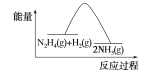
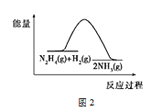
B.反应Ⅱ的能量过程示意图如图2所示
C.断开3 mol N2H4(g)中的化学键吸收的能量小于形成1 mol N2(g)和4 mol NH3(g)中的化学键释放的能量
D.200 ℃时,肼分解生成氮气和氢气的热化学方程式为:N2H4(g)= N2(g)+2H2(g) ΔH=-50.7 kJ/mol
-
已知硝酸铵在不同温度下分解会有不同的产物,反应方程式如下,
①NH4NO3 NH3↑+HNO3↑②NH4NO3
NH3↑+HNO3↑②NH4NO3 N2O↑+2H2O↑
N2O↑+2H2O↑
③2NH4NO3 2N2↑+O2↑+4X↑④4NH4NO3
2N2↑+O2↑+4X↑④4NH4NO3 3N2↑+2NO2↑+8H2O↑
3N2↑+2NO2↑+8H2O↑
请回答下列问题:
(1)这四个反应中属于氧化还原反应的有___个。
(2)反应③中物质X的化学式是___。
(3)反应④中氧化产物和还原产物依次是___、___。(填化学式)
(4)若反应③生成标准状况下的11.2L氧气,则转移电子数为___。
-
已知甲烷在不同条件下有两种热分解反应:
①CH4(g) C(s)+2H2(g);②2CH4(g)
C(s)+2H2(g);②2CH4(g) C2H2(g)+3H2(g)。
C2H2(g)+3H2(g)。
现将两份标准状况下等体积的甲烷分别通入两个容积可变的密闭容器中,按①式和②式热解,待完全反应后,恢复至标准状况,则两容器中气体体积关系正确的是( )
A. ①和②相等 B. ①小于② C. ①大于② D. 无法判断
-
已知1g火箭燃料肼(N2H4)气体燃烧生成N2和H2O(g)时,放出16.7kJ的热量,则该反应的热化学方程式正确的是
A.N2H4+O2=N2+2H2O△H=-534.4kJ/mol
B.N2H4(g)+ O2(g)=N2(g)+2H2O(g)△H=-16.7kJ/mol
C.N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-534.4kJ/mol
D.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534.4kJ/mol
-
一定条件下,乙醛可发生分解:CH3CHO(l)→CH4+CO,已知该反应的活化能为190 kJ·mol-1。 在含有少量I2的溶液中,该反应的机理如下:
反应Ⅰ:CH3CHO+I2 CH3I+HI+CO(慢)
CH3I+HI+CO(慢)
反应Ⅱ:CH3I+HI CH4+I2(快)
CH4+I2(快)
下列有关该反应的叙述正确的是 ( )
A. 反应速率与I2的浓度有关 B. HI在反应Ⅰ中是氧化产物
C. 反应焓变的绝对值等于190 kJ·mol-1 D. 乙醛的分解速率主要取决于反应Ⅱ
-
已知二氧化硫可使高锰酸钾溶液褪色,反应的化学方程式为:5SO2+2KMnO4+2H2O═K2SO4+2MnSO4+2H2SO4
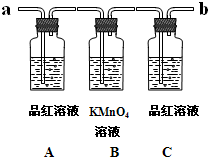
用如图装置来验证浓硫酸与木炭在加热条件下反应的产物中含有SO2和CO2
①实验时,反应产生的气体应从______端通入; 从______端连接盛有澄清石灰水的实验装置(用“a”或“b”填空).
②可观察到A瓶的溶液的现象______.
③B瓶溶液的作用是______.
④C瓶溶液的作用是______.
-
过氧化氢(O为—1价)在二氧化锰催化作用下分解放出氧气的反应机理如下:
①MnO2 + H2O2 + 2H+ = Mn2+ + O2↑ + 2H2O ②Mn2+ + H2O2 = MnO2 + 2H+
下列说法正确的是( )
A.H2O2在①中是氧化剂,在②中是还原剂
B.在①中每生成1 mol O2,转移的电子数为1.204×1024
C.Mn2+在①中是还原产物,在②中是氧化产物
D.在二氧化锰催化作用下,1 mol H2O2分解生成22.4 L O2
-
过氧化氢(O为—1价)在二氧化锰催化作用下分解放出氧气的反应机理如下:
①MnO2 + H2O2 + 2H+ = Mn2+ + O2↑ + 2H2O ②Mn2+ + H2O2 = MnO2 + 2H+
下列说法正确的是
A.H2O2在①中是氧化剂,在②中是还原剂
B.在①中每生成1 mol O2,转移的电子数为1.204×1024
C.Mn2+在①中是还原产物,在②中是氧化产物
D.在二氧化锰催化作用下,1 mol H2O2分解生成22.4 L O2
-
在反应2N2H4 + 2NO2 = 3N2 + 4H2O 中,氧化产物和还原产物的物质的量之比为 ( )
A. 1:1 B. 3:4 C. 4:3 D. 2:1
-
卫星发射时是以N2H4(联氨)和N2O4为火箭的动力源。反应温度高达2700 ℃,反应式为2N2H4+N2O4===3N2+4H2O。对于该反应的说法正确的是( )
A. 联氨是氧化剂 B. 氧化产物和还原产物的质量比为1∶2
C. 属于置换反应 D. 该反应的优点有热值高、无污染等