-
“北大富硒康”中含有微量元素(Se),对人体有保健作用。已知硒为第4周期ⅥA族元素,根据它在周期表中的位置推测硒不可能具有的性质为( )
A.硒化氢很稳定
B.硒化氢的水溶液显弱酸性
C.得电子能力强于硫
D.其最高价氧化物的水化物酸性强于砷弱于溴
高三化学选择题中等难度题查看答案及解析
-
已知34Se、35Br位于同一周期,根据元素在周期表中的位置,下列说法正确的是( )
A.离子还原性:Se2->Br- B.气态氢化物的稳定性:H2S>H2Se
C.原子半径:Cl>Br>Se D.酸性:H2SeO4>HBrO4>HClO4
高三化学多选题简单题查看答案及解析
-
已知34Se、35Br位于同一周期,根据元素在周期表中的位置,下列说法正确的是
A. 还原性:Cl->Br- B. 酸性:H2SeO4>HBrO4>HClO4
C. 原子半径:Se>Br>Cl D. 气态氢化物的稳定性:H2Se>H2S
高三化学单选题中等难度题查看答案及解析
-
已知34Se、35Br位于同一周期,根据元素在周期表中的位置,下列说法正确的是
A. 还原性:Cl->Br- B. 酸性:H2SeO4>HBrO4>HClO4
C. 原子半径:Cl>Br>Se D. 气态氢化物的稳定性:H2S>H2Se
高三化学单选题简单题查看答案及解析
-
9.已知34Se、35Br位于同一周期,根据元素在周期表中的位置,判断下列说法正确的是
A.离子还原性:Cl->Br- B.气态氢化物的稳定性:H2S>H2Se
C.原子半径:Cl>Br>Se D.酸性:H2SeO4>HBrO4>HClO4
高三化学选择题中等难度题查看答案及解析
-
A、B、C、D、E、F、G 为短周期主族元素,其原子半径与最外层电子数的关系如图,下列说法正确的是
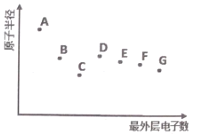
A.根据元素B 在元素周期表中的位置推测,其最高价氧化物对应的水化物可能具有两性
B.元素D在自然界中主要以游离态存在,其单质可用作半导体材料
C.元素A的离子半径大于元素G的离子半径
D.元素F 的气态氢化物比元素G的气态氢化物更稳定
高三化学单选题中等难度题查看答案及解析
-
1. 根据砷元素在元素周期表中的位置,推测砷元素单质及其化合物不可能具有的性质是( )
A. 砷元素单质在通常情况下是固体
B. 砷元素有-3、+3、+5等多种化合价
C. As2O5对应的水化物的酸性比磷酸强
D. 砷化氢不稳定
高三化学选择题中等难度题查看答案及解析
-
硒(Se)是第34号元素,是人体内不可或缺的微量元素,可以形成H2Se、SeO2、H2SeO3、H2SeO4、CuSe等多种化合物。请回答下列问题:

(1)硒在元素周期表中的位置________________________。
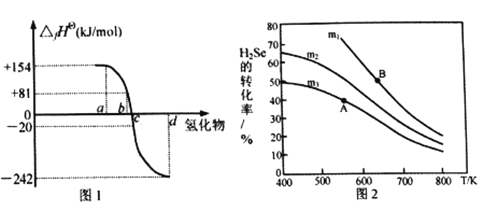
(2)在101kPa、一定温度(一般是298K)下,由稳定单质发生反应生成1mol化合物的反应热叫该化合物的标准生成热(△fHθ)。图1为氧族元素氢化物a、b、c、d呈气态时的生成热数据。
①图1中氢化物d的电子式为__________________________。
②在298K时,硒化氢分解反应的热化学反应方程式为__________________________。
③由图中数据计算,2H2Se(g)+O2(g)
2Se(s)+2H2O(g) △H=_____________KJ/mol
(3)在恒容反应器中,将H2Se(g)和O2(g)按不同比例[n(H2Se)/n(O2)=m]投入反应器,测得反应2H2Se(g)+O2(g)
2Se(s)+2H2O(g)中H2Se的平衡转化率随温度变化如图2所示。则A、B两点平衡常数大小关系为KA________KB(填“<”、“>”或“=”),图中m1、m2、m3由大到小的顺序为 ____________,理由是____________________________________。
(4)常温下溶度积:Ksp(CuSe)=7.9x10-49,Ksp(CuS)=1.3×10-36。则反应CuS(s)+Se2-(aq)
CuSe(s)+S2-(aq)的化学平衡常数K为____________(结果用科学记数法表示,并保留2位小数)。当溶液中c(S2-)=100c(Se2-)时,反应中v(正)_____v(逆)(填“<”、“>”或“=”) 。
高三化学综合题中等难度题查看答案及解析
-
硒(Se)是第34号元素,是人体内不可或缺的微量元素,可以形成H2Se、SeO2、H2SeO3、H2SeO4、CuSe等多种化合物。请回答下列问题:
(1)硒在元素周期表中的位置________________________。
(2)在101kPa、一定温度(一般是298K)下,由稳定单质发生反应生成1mol化合物的反应热叫该化合物的标准生成热(△fHθ)。图1为氧族元素氢化物a、b、c、d呈气态时的生成热数据。
①图1中氢化物d的电子式为__________________________。
②在298K时,硒化氢分解反应的热化学反应方程式为__________________________。
③由图中数据计算,2H2Se(g)+O2(g)
2Se(s)+2H2O(g) △H=_____________KJ/mol
(3)在恒容反应器中,将H2Se(g)和O2(g)按不同比例[n(H2Se)/n(O2)=m]投入反应器,测得反应2H2Se(g)+O2(g)
2Se(s)+2H2O(g)中H2Se的平衡转化率随温度变化如图2所示。则A、B两点平衡常数大小关系为KA________KB(填“<”、“>”或“=”),图中m1、m2、m3由大到小的顺序为 ____________,理由是____________________________________。
(4)常温下溶度积:Ksp(CuSe)=7.9x10-49,Ksp(CuS)=1.3×10-36。则反应CuS(s)+Se2-(aq)
CuSe(s)+S2-(aq)的化学平衡常数K为____________(结果用科学记数法表示,并保留2位小数)。当溶液中c(S2-)=100c(Se2-)时,反应中v(正)_____v(逆)(填“<”、“>”或“=”) 。
高三化学综合题中等难度题查看答案及解析
-
砷为第四周期、第VA族元素,根据它在元素周期表中的位置推测,砷不可能具有的性质是
A.砷在通常状况下是固体
B.可以是+5、+3、-3等多种化合价
C.As2O5对应水化物的酸性比H3PO4强
D.砷的还原性比磷强
高三化学选择题中等难度题查看答案及解析