-
聚乙二醇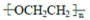 )电解质散剂,常用于肠镜检查前的肠道清洁准备。下图是以具有 芳香气味的有机物A 为原料制取聚乙二醇的过程(部分产物已略去)。烃 C 中碳与氢元素的质量比为 6∶1,是同系物中最简单的物质;E 不能发生银镜反应。
)电解质散剂,常用于肠镜检查前的肠道清洁准备。下图是以具有 芳香气味的有机物A 为原料制取聚乙二醇的过程(部分产物已略去)。烃 C 中碳与氢元素的质量比为 6∶1,是同系物中最简单的物质;E 不能发生银镜反应。
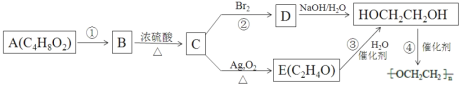
(1)E 物质的名称是_____。
(2)D 的键线式是_____。
(3)反应④的化学方程式是_____。
(4)下列说法正确的是_____。
a.A 在酸性或碱性条件下都可以反应得到B,反应②中的 Br2 可以是溴水或溴的 CCl4 溶液
b.工业上获得C 的的主要方法是催化裂化
c.可以用饱和碳酸钠溶液除去 B 中混有的少量A
d.反应①的反应类型为水解反应
-
(12分)工业上电解饱和食盐能制取多种化工原料,其中部分原料可用于制备多晶硅。
(1)下图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是________;NaOH溶液的出口为________(填字母);精制饱和食盐水的进口为________(填字母);干燥塔中应使用的液体是________。
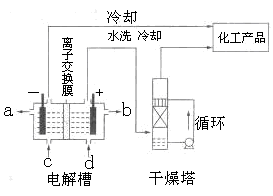
(2)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用受到广泛关注。
① SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为________。
② SiCl4可转化为SiHCl3而循环使用。一定条件下,在20L恒容密闭容器中的反应:
3 SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g)
4SiHCl3(g)
达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的质量为______kg。
(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0kg,则生成氢气________ (标准状况)。
(标准状况)。
-
下列说法中,不正确的是
A.卤代烃一般易溶于水,常用作有机溶剂
B.苯酚是重要的有机化工原料,可用于制备酚醛树脂
C.乙二醇水溶液的凝固点低,可用作汽车发动机的抗冻剂
D.福尔马林具有防腐杀菌作用,能用于浸制生物标本
-
(12分)乙烯是重要的化工原料,可以合成很多有机物。以下转化关系中A-J均为有机化合物,H为有芳香气味的液体,F的分子式为C2H2O2,I分子中有一个六原子环状结构。部分反应条件和生成物已略去。完成下列问题:
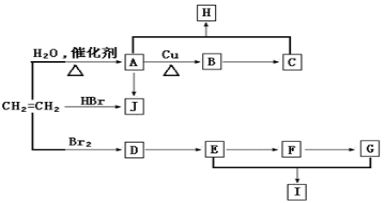
(1)写出A生成B的化学方程式: 。
(2)写出A生成J的化学方程式: 。
(3)写出D生成E的化学方程式:________________________________________。
(4)写出E和G生成I的化学方程式: 。
-
(12分)乙烯是重要的化工原料,可以合成很多有机物。以下转化关系中A-J均为有机化合物,H为有芳香气味的液体,F的分子式为C2H2O2,I分子中有一个六原子环状结构。部分反应条件和生成物已略去。
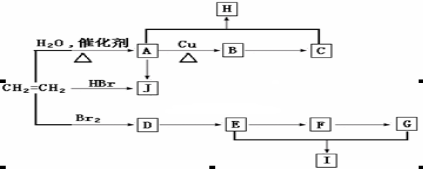
完成下列问题:
(1)写出A生成B的化学方程式:
(2)写出A生成J的化学方程式:
(3)写出D生成E的化学方程式:
(4)写出E和G生成I的化学方程式:
-
有效利用现有资源是解决能源问题的一种实际途径,发展“碳一化学”,开发利用我国相对丰富的煤炭资源具有重要的战略意义和经济价值。下面是以焦炭为原料,经“碳一化学”途径制取乙二醇的过程:

(1)以CO和CO2分别与H2为原料,在一定条件下均可合成甲醇(CH3OH)。你认为用哪种合成设计路线更符合“绿色化学”理念:(用化学反应方程式表示)____________;
(2)下图表示在恒容容器中230℃催化剂条件下,0.5molCO2和1.5molH2反应得到甲醇蒸气,产率达80%时的能量变化示意图。
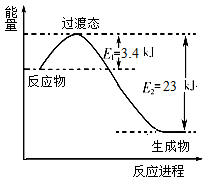
①写出该反应的热化学方程式:_____________________。
②能判断该反应达到化学平衡状态的依据是_____________________。
a.容器中压强不变 b.H2的体积分数不变
c.c(H2)=3c(CH3OH) d.容器中气体密度不变
(3)如图所示是用于合成甲醇产品中甲醇含量的检测仪。写出该仪器工作时的电极反应式:负极______。
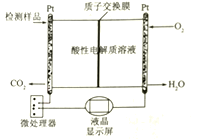
(4)“催化还原”反应制乙二醇(HOCH2-CH2OH)原理如下:
CH3OOC-COOCH3(g)+4H2(g) HOCH2-CH2OH(g)+2CH3OH(g) △H=-34kJ/mol
HOCH2-CH2OH(g)+2CH3OH(g) △H=-34kJ/mol
为探究实际生产的最佳条件,某科研小组进行了多方面研究,下图表示乙二醇达平衡时的产率随原料投料比[n(氢气)/n(草酸二甲酯)]和压强的变化关系,其中三条曲线分别表示体系压强为1.5MPa、2.5MPa、3.5MPa的情况,则曲线丙对应的压强时P(丙)=___________。

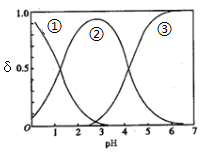
(5)草酸二甲酯水解产物草酸(H2C2O4)为二元中强酸。H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示曲线①代表的粒子是___________;草酸氢钾溶液中存在如下平衡:H2O H++OH-,HC2O4-
H++OH-,HC2O4- H++C2O42-和___________;一定温度下,往CaC2O4饱和溶液[已知Ksp(CaC2O4=2.3×10-9)]中加入少量CaCl2固体,c(Ca2+)将_________,CaC2O4的溶解度将____________。(填“增大”“减小”或“不变”)
H++C2O42-和___________;一定温度下,往CaC2O4饱和溶液[已知Ksp(CaC2O4=2.3×10-9)]中加入少量CaCl2固体,c(Ca2+)将_________,CaC2O4的溶解度将____________。(填“增大”“减小”或“不变”)
-
(5分)乙酸苯甲酯可提高花或水果的芳香气味,常用于化妆品工业和食品工业。下图是乙酸苯甲酯的一种合成路线(部分反应物、产物和反应条件略去)。
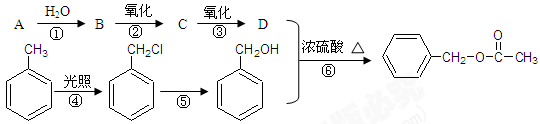
请回答:
(1)运用逆合成分析法推断,C的结构简式为________。
(2)写出A→B的化学方程式为________
(3)与  互为同分异构体的芳香族化合物有________种,其中一种同分
互为同分异构体的芳香族化合物有________种,其中一种同分
异构体的核磁共振氢谱有三种类型氢原子的吸收峰,该同分异构体的结构简式为________ 。
-
(18分)A为常见烃是一种水果催熟剂,乙酸苯甲酯可提高花或果的芳香气味,常用于化妆品工业和食品工业。下图是乙酸苯甲酯的一种合成路线(部分反应物、产物和反应条件略去)。
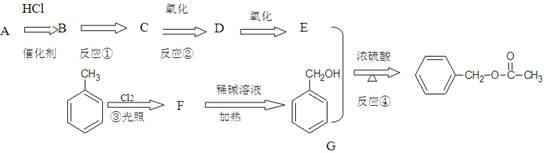
请回答:
(1)E的官能团名称为 ________F的结构简式为________
(2)反应①条件为________,反应④的类型是 ________
(3)反应②的化学方程式为________;反应类型是________
(4)物质D与新制氢氧化铜反应方程式为________
(5)G有多种同分异构体,其中属于芳香族化合物的有 ________种 (不包括G)
写出其中的任意一种同分异构体的结构简式 ________
-
乙酸苯甲酯可提高花或果的芳香气味,常用于化妆 品工业和食品工业,下图是乙酸苯甲酯的一种合成路线(部分反应物、产物和反应条件略去)。已知A是果实的催熟剂。
品工业和食品工业,下图是乙酸苯甲酯的一种合成路线(部分反应物、产物和反应条件略去)。已知A是果实的催熟剂。
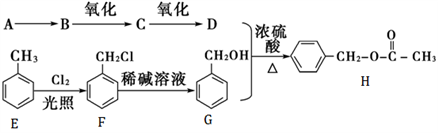
(1)A分子的电子式为________;C的分子式为________;D中官能团结构简式为________。
(2) A→B反应类型为 _____________,反应 F→G反应类型___________。
(3)G的同分异构体有多种,遇FeCl3溶液显紫色的共有_____种;
苯环上一氯代物有2种的物质的结构简式______________。
(4)写出下列反应的化学方程式:
B→C:_____________________;
F→G:______________________;
G→H:___________________;
C的银镜反应方程式为:____________________。
-
工业上电解饱和食盐水能制取多种化工原料,其中部分原料可用于制备多晶硅。
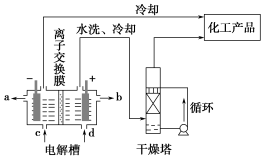
(1)上图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是________;NaOH溶液的出口为________(填字母);精制饱和食盐水的进口为________(填字母);干燥塔中应使用的液体是________。
(2)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用受到广泛关注。
①SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为___________________________________。
②SiCl4可转化为SiHCl3而循环使用,一定条件下,在20 L恒容密闭容器中的反应:
3SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g)
4SiHCl3(g)
达平衡后,H2和SiHCl3物质的量浓度分别为0.140 mol/L和0.020 mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的质量为________kg。
(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0 kg,则生成氢气________m3(标准状况)。
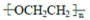 )电解质散剂,常用于肠镜检查前的肠道清洁准备。下图是以具有 芳香气味的有机物A 为原料制取聚乙二醇的过程(部分产物已略去)。烃 C 中碳与氢元素的质量比为 6∶1,是同系物中最简单的物质;E 不能发生银镜反应。
)电解质散剂,常用于肠镜检查前的肠道清洁准备。下图是以具有 芳香气味的有机物A 为原料制取聚乙二醇的过程(部分产物已略去)。烃 C 中碳与氢元素的质量比为 6∶1,是同系物中最简单的物质;E 不能发生银镜反应。











