-
据世界权威刊物《自然》最近报道, 选择碲化锆 (ZrTe5)为材料验证了三维量子霍尔效应, 并发现了金属-绝缘体的转换。Te属于ⅥA元素。回答下列问题:
(1)锆(Zr)的简化电子排布式为[Kr]4d25s2,锆原子中d轨道上的电子数是___,Zr2+的价电子排布图是___。
(2)O、Se、Te的第一电离能由大到小的顺序是___,H2O、H2Se、H2Te的沸点由高到低的顺序是___。
(3)H2Te和CO2 均为三原子分子,但它们的键角差别较大,试用杂化轨道理论解释,理由是___。
(4) [Zr(C2H5O)2]2+是Zr4+形成的一种配离子,其中的配位原子是___(填符号), 1个[Zr(C2H5O)2]2+离子中含共价键的数目是___。
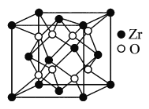
(5)立方氧化锆是一种人工合成的氧化物,其硬度极高,可用于陶瓷和耐火材料,其晶胞结构如图所示。Zr原子的配位数是___。若晶胞中距离最近的两个氧原子间的距离为anm,则立方氧化锆的密度为___ g/cm3。
-
据世界权威刊物《自然》最近报道,我国科学家选择碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应,并发现了金属-绝缘体的转换。回答下列问题:
(1)锌和镉位于同副族,而锌与铜相邻。现有 4 种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10。失去1个电子需要的能量由大到小排序是______(填字母)。
A.④②①③ B.④②③① C.①②④③ D.①④③②
(2)硫和碲位于同主族,H2S的分解温度高于H2Te,其主要原因是_______。在硫的化合物中,H2S、CS2都是三原子分子,但它们的键角(立体构型)差别很大,用价层电子对互斥理论解释:_________;用杂化轨道理论解释:_________。
(3)Cd2+与NH3等配体形成配离子。[Cd(NH3)4]2+中2个NH3被2个Cl-替代只得到1种结构,它的立体构型是___________。1 mol [Cd(NH3)4]2+含___________mol σ键。
(4)砷与卤素形成多种卤化物。AsCl3、AsF3、AsBr3的熔点由高到低的排序为__________。
(5)锆晶胞如图所示,1个晶胞含_______个Zr原子;这种堆积方式称为__________。
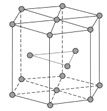
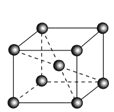
(6)镉晶胞如图所示。已知:NA是阿伏加德罗常数的值,晶体密度为 d g·cm-3。在该晶胞中两个镉原子最近核间距为______nm(用含NA、d的代数式表示),镉晶胞中原子空间利用率为________(用含π的代数式表示)。
-
据世界权威刊物《自然》最近报道,我国科学家选择碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应,并发现了金属-绝缘体的转换。回答下列问题:
(1)锌原子的价电子排布图:____________________________________________
(2)硫和碲位于同主族,H2S的分解温度高于H2Te,其主要原因是________________
(3)Cd2+与NH3等配体形成配离子。1 mol [Cd(NH3)4]2+含___________mol σ键。该配离子中三种元素的电负性大小关系是:_______________________
(4)砷与卤素形成多种卤化物。AsCl3、AsF3、AsBr3的熔点由高到低的排序为________
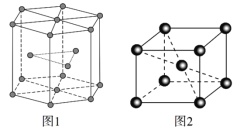
(5)锆晶胞如图1所示,这种堆积方式称为______________________,镉晶胞如图2所示。已知:NA是阿伏加德罗常数的值,晶体密度为d g·cm3。在该晶胞中两个镉原子最近核间距为______nm(用含NA、d的代数式表示),镉晶胞中原子空间利用率为________(用含π的代数式表示)。
-
最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,质量数是85。根据材料完成下列问题:
(1)铷Rb37位于周期表的第__________周期、第__________族。
(2)关于铷的结构和性质判断正确的是( )
①与水反应比钠强烈
②它的原子半径比钠小
③它的氧化物暴露在空气中易吸收CO2
④它的阳离子最外层电子数和镁相同
⑤它是还原剂
A.①③④ B.②③⑤
C.②④ D.①③⑤
(3)氢化铷与水反应可放出氢气,则下列叙述正确的是( )
A.氢化铷溶于水显酸性
B.氢化铷中氢离子被还原为氢气
C.氢化铷与水反应时,水是还原剂
D.氢化铷中氢离子最外层有两个电子
(4)现有铷和另一种碱金属形成的合金50 g,当它与足量水反应时,放出标准状况下的氢气22.4 L,这种碱金属可能是( )
A.Li B.Na C.K D.Cs
-
最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,质量数是85。根据材料完成下列问题:
(1)铷Rb37位于周期表的第__________周期,第__________族。
(2)关于铷的结构和性质判断正确的是( )
①与水反应比钠剧烈
②它的原子半径比钠小
③它的氧化物暴露在空气中易吸收CO2
④它的阳离子最外层电子数和镁相同
⑤它是还原剂
A.①③④ B.②③⑤ C.②④ D.①③⑤
(3)氢化铷与水反应可放出氢气,则下列叙述正确的是( )
A.氢化铷溶于水显酸性
B.氢化铷中氢离子被还原为氢气
C.氢化铷与水反应时,水是还原剂
D.氢化铷中氢离子最外层有两个电子
(4)现有铷和另一种碱金属形成的合金50 g,当它与足量水反应时,放出标准状况下的氢气22.4 L,这种碱金属可能是( )
A.Li B.Na C.K D.Cs
-
据权威刊物报道,1996年科学家在宇宙中发现H3分子。甲、乙、丙、丁四位学生对此报道的认识正确的是 ( )
A.甲认为上述发现绝对不可能,因为H3分子违背了共价键理论
B.乙认为宇宙中还可能存在另一种氢单质,因为氢元素有三种同位素必然有三种阿素异形体
C.丙认为H3屯分子实质上是H2分子与H+以特殊共价键结合的产物,应写成H3+
D.丁认为如上述发现存在,则证明传统的价键理论有一定的局限性有待继续发展
-
据权威刊物报道,1996年科学家在宇宙中发现H3分子。甲、乙、丙、丁四位学生对此报道的认识正确的是 ( )
A.甲认为上述发现绝对不可能,因为H3分子违背了共价键理论
B.乙认为宇宙中还可能存在另一种氢单质,因为氢元素有三种同位素必然有三种阿素异形体
C.丙认为H3屯分子实质上是H2分子与H+以特殊共价键结合的产物,应写成H3+
D.丁认为如上述发现存在,则证明传统的价键理论有一定的局限性有待继续发展
-
金属有机催化体系的发现和发展对有机合成策略的革新起到关键的决定性作用。最近,中国科学家采用新型锰催化体系,选择性实现了简单酮与亚胺的芳环惰性C-H的活化反应。利用该反应制备化合物W的合成路线如下:
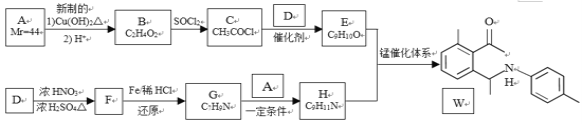
已知:①A为常见的有机物;D为苯的同系物,分子式为C7H8
②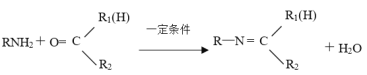
回答下列问题:
(1)B中官能团的名称是__________,F的化学名称是____________。
(2)W的分子式为__________。
(3)D→F,E+H→W的反应类型分别是___________、_____________。
(4)A与银氨溶液加热反应的化学方程式为__________。C和D生成E的化学方程式为_________。
(5)芳香化合物L是E的同分异构体。若L能发生银镜反应,则L可能的结构有______种,其中核磁共振氢谱有四组峰的结构简式为__________(任写一种)。
(6)请以甲苯、丙酮(CH3COCH3)等为原料制备 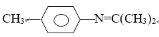 ,写出相应的合成路线流程图(无机试剂任用)_________。
,写出相应的合成路线流程图(无机试剂任用)_________。
-
电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
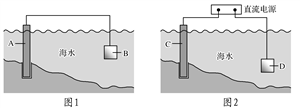
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择________(填字母序号)。
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:___________________________。
(2)图2中,钢闸门C作________极。若用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极反应式为_____________________________________,检测该电极反应产物的方法是_________________________________________。
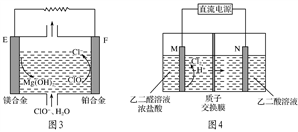
(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的________极(填“正”或“负”)。F电极上的电极反应式为_______________________________________________________________。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因:___________________________________________________。
(4)乙醛酸( )是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
①N电极上的电极反应式为_____________________________________。
②若有2molH+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为________ mol。
-
电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。

(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择__________(填字母序号)
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因_______________。

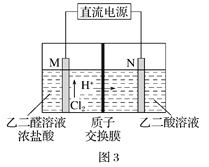
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图2为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的_____________极(填“正”或“负”)。F电极上的电极反应式为_____________。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因____________。
(3)乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图3所示,该装置中阴、阳两极为惰性电极,两级室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
①N电极上的电极反应式为______________。
②若有2molH+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为________________mol。






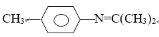 ,写出相应的合成路线流程图(无机试剂任用)_________。
,写出相应的合成路线流程图(无机试剂任用)_________。



