-
如图是元素周期表中的前四周期,①~⑨为相应的元素,请从中选择合适的元素回答问题:
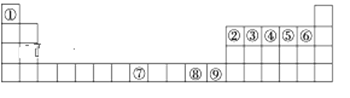
(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,元素⑦位于周期表的___区。
(2)写出元素③与元素⑤形成的稳定化合物的结构式___________。
(3)②、⑥两元素形成的化合物的立体构型为_______,其中心原子的杂化轨道类型为______。
(4)元素⑦与CO可形成X(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断该化合物晶体属于_____晶体(填晶体类型)。
(5)⑧的二价阳离子与过量的④的简单氢化物的水溶液作用的离子方程式_________。
(6)元素⑨的离子的氢氧化物不溶于水,但可溶于氨水中,该离子与NH3间结合的作用力为____。
(7)将①、⑥形成的化合物溶于水,其中可能存在的氢键表示为_______(写一种即可)。
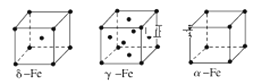
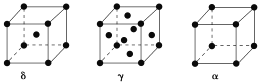
(8)金属⑦有δ、γ、α三种同素异形体,各晶胞如下图,则δ和α中原子的配位数之比为______。
-
如图是元素周期表中的前四周期,①~⑨为相应的元素,请从中选择合适的元素回答问题:
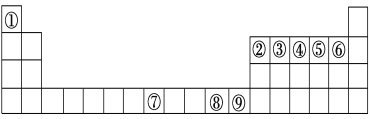
(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,⑨元素位于周期表的________区。
(2)④、⑥两元素形成的化合物的立体构型为________,其中心原子的杂化轨道类型为________。
(3)元素⑧的离子的氢氧化物不溶于水,但可溶于氨水中,该离子与NH3间结合的作用力为________。
(4)在周期表给出的9种元素中,电负性最大的元素基态原子的电子排布式为___________。
(5)在①与④形成的相对分子质量最小的化合物A中,元素④的杂化类型是____,写出与化合物A互为等电子体的一种阳离子______(填离子符号)。
(6)关于元素①与元素⑤形成的1︰1的化合物,下列说法正确的是______(填字母序号)。
A.该化合物中的所有原子都满足最外层8电子稳定结构
B.该化合物分子中σ键和π键数目比为1︰1
C.该化合物是由极性键和非极性键形成的极性分子
D.该化合物分子的空间构型为直线形
(7)元素⑦与CO可形成X(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断该化合物晶体属于________晶体(填晶体类型),化合物中⑦的化合价为:_______。根据等电子体理论,该化合物的配体的结构式为:_______,CaC2中,阴离子的电子式为: ____________________。
-
如图是元素周期表中的前四周期,①~⑨为相应的元素,请从中选择合适的元素回答问题:
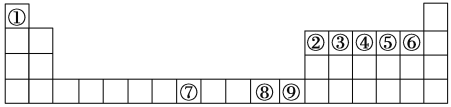
(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,①元素位于周期表的______________区。
(2)②、⑥两元素形成的化合物的空间构型为______________,其中心原子的杂化轨道类型为________。
(3)写出元素③与元素⑤形成的稳定化合物的结构式_______________。
(4)⑧的二价阳离子与过量的④的氢化物的水化物作用的离子方程式为:______。
(5)元素⑦与CO可形成X(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断该化合物晶体属于________晶体(填晶体类型)。
(6)元素⑨的离子的氢氧化物不溶于水,但可溶于氨水中,该离子与NH3间结合的作用力为________。
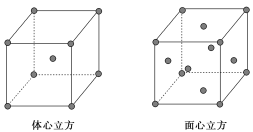
(7)金属⑦的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。则面心立方晶胞和体心立方晶胞中实际含有的原子个数之比为________。
-
过渡元素Ti、Mn、Fe、Cu等可与C、H、O形成多种化合物。请回答下列问题:
(1)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域,其中Mn属于________区。某一次性电池负极材料是Zn,正极材料是Mn的一种常见氧化物,放电后生成MnOOH,电解质是KOH。该电池的正极反应式为__________________________。
(2)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。基态Ti2+中电子占据的最高能层符号为________,该能层具有的原子轨道数为________。BH4-的立体构型是________。
(3)单质Cu的晶体类型为______,晶体中组成微粒通过________作用形成面心立方密堆积,其中Cu原子的配位数为______。在Cu的催化作用下,乙醇可被空气中氧气氧化为乙醛,乙醛分子中碳原子的杂化方式是________,乙醛分子中∠HCO的键角________乙醇分子中∠HCO的键角(填“大于”、“等于”或“小于”)。
(4)单质铁有δ、γ、α三种同素异形体,三种晶胞中Fe原子的配位数之比为________,δ、γ、α三种晶胞的边长之比为________。
-
利用所学化学知识解答问题:
 在高温下CuO 能分解生成
在高温下CuO 能分解生成 ,试从原子结构角度解释其原因: ______
,试从原子结构角度解释其原因: ______  根据元素原子的外围电子排布特征,可将周期表分成五个区域,元素Cu属于 ______ 区
根据元素原子的外围电子排布特征,可将周期表分成五个区域,元素Cu属于 ______ 区
 氰酸
氰酸 是一种链状分子,它与异氰酸
是一种链状分子,它与异氰酸 互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 ______
互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 ______  其中的C的杂化类型为 ______ .
其中的C的杂化类型为 ______ .
 原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物
原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物 与Fe原子或离子形成配合物的分子或离子应具备的结构特征是 ______ .
与Fe原子或离子形成配合物的分子或离子应具备的结构特征是 ______ .
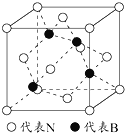
 立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,其晶胞结构与金刚石类似,一个该晶胞中含有 ______ 个氮原子, ______ 个硼原子,设氮原子半径为a pm,硼的原子半径b pm,求该晶胞的空间利用率 ______
立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,其晶胞结构与金刚石类似,一个该晶胞中含有 ______ 个氮原子, ______ 个硼原子,设氮原子半径为a pm,硼的原子半径b pm,求该晶胞的空间利用率 ______  用含a、b的代数式表示
用含a、b的代数式表示
-
根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)A元素次外层电子数是最外层电子数的1/4,外围电子的电子排布图是______。
(2)B是1~36号元素中原子核外电子排布未成对电子数最多的元素,B元素的名称是____,在元素周期表中的位置是____________________。
(3)C元素基态原子的电子排布图是下图中的_______(填序号),另一电子排布图不能作为基态原子的电子排布图是因为它不符合_______(填编号)。
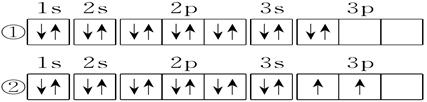
A.能量最低原理 B.泡利原理 C.洪特规则
-
根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)A元素次外层电子数是最外层电子数的 ,其外围电子轨道表示式是__。
,其外围电子轨道表示式是__。
(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是__,在元素周期表中的位置是__,位于周期表___区,写出基态B原子的核外电子排布式___。
(3)C、N、O、F四种元素第一电离能由大到小的顺序为___,电负性由大到小的顺序为___。
(4)基态Fe2+核外电子排布式为__,Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为__。
(5)根据元素As在周期表中的位置预测As的氢化物分子的空间构型为__,其沸点比NH3的__(填“高”或“低”),其判断理由是__。
-
(1)基态Cu2+的核外电子排布式为 ,在高温下CuO 能分解生成Cu2O,试从原子结构角度解释其原因: 。根据元素原子的外围电子排布特征,可将周期表分成五个区域,元素Cu属于 区。
(2)下列叙述不正确的是 。(填字母)
a.HCHO和CO2分子中的中心原子均采用sp杂化
b.因为HCHO与水分子间能形成氢键,所以HCHO易溶于水
c.C6H6分子中含有6个σ键和1个大π键,C2H2是非极性分子
d.CO2晶体的熔点、沸点都比二氧化硅晶体的低,原因是CO2为分子晶体而二氧化硅是原子晶体
(3)氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 。其中的C的杂化类型为 ,写出一种与 CN— 互为等电子体的单质分子式 。
(4)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
① 与Fe原子或离子形成配合物的分子或离子应具备的结构特征是 。
② 六氰合亚铁离子[Fe(CN)6]4 -中不存在 。
a.共价键
b.非极性键
c.配位键
d.σ键
e.π键
(5)立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,其晶胞结构与金刚石类似,一个该晶胞中含有 个氮原子, 个硼原子,设氮原子半径为a pm,硼的原子半径b pm ,求该晶胞的空间利用率 。(用含a、b的代数式表示)
-
按要求回答以下问题:
(1)X、Y、Z 是短周期非金属元素,核电荷数依次增大。X原子外围电子排布为ns2np2,Z是地壳中含量最多的元素。W、Q是第四周期元素,其中Q元素的核电荷数为29。W原子核外未成对电子数在同周期中最多。
①Y元素在周期表中的位置为______________ ;其轨道表示式为_________________。
②X、Y、Z元素的第一电离能由大到小的顺序为_________________(用元素符号作答),X与Z形成三原子分子的电子式为___________(用相关的化学用语作答)。
③Y的氢化物沸点_______Z的氢化物的沸点(填“ >”“<”或 “=”)。
④基态W原子的外围电子排布式为 。
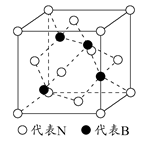
⑤Q的氢化物的晶胞结构如图所示,其化学式是 。
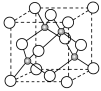
(2)过渡元素在生活、生产和科技等方面有广泛的用途。

①应用于合成氨反应的催化剂(铁)的表面上存在氮原子,上图为氮原子在铁的晶面上的单层附着局部示意图(图中小黑色球代表氮原子,灰色球代表铁原子)。则图示铁颗粒表面上氮原子与铁原子的个数比为________。
②现代污水处理工艺中常利用聚合铁{简称PFS,化学式为[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是______。(填序号)
| 元素 | Mn | Fe |
| 电离能 | | |
| (kJ·mol-1) | | |
| I1 | 717 | 759 |
| I2 | 1 509 | 1561 |
| I3 | 3 248 | 2 957 |
A.PFS中铁显+3价
B.铁原子的价电子排布式是3d64s2
C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程
D.由上表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难
③铂(Pt)单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
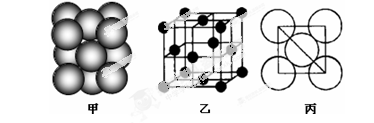
晶胞中铂(Pt)原子的配位数数为为 。
-
X、Y、Z三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如下图转化关系,回答下列问题:

(1)若X基态原子外围电子排布式为3s2,甲是由第二周期两种元素的原子构成的非极性气态分子,Y原子的电子排布图为_________,乙的电子式为________;
(2)若X为非金属,甲是由两种短周期元素的原子构成的A2B型极性分子,且是常见的溶剂,甲的电子式___,乙的化学式为_____;
(3)若X、Y均为金属单质,X基态原子外围电子排布式为3s23p1,甲为具有磁性的黑色固体,则X与甲反应的化学方程式为:___。











