-
随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点。完成下列填空:
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:
CO2(g)+4H2(g)  CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
已知H2的体积分数随温度升高而增加。
若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化。(选填“增大”、“减小”或“不变”)
(2)相同温度,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
| [CO2]/mol·L-1 | [H2]/mol·L-1 | [CH4]/mol·L-1 | [H2O]/mol·L-1 |
| 平衡Ⅰ | a | b | c | d |
| 平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为_________。 (用含有a、b、c、d、m、n、
(用含有a、b、c、d、m、n、 x、y的一个代数式表示)
x、y的一个代数式表示)
(3)碳酸H2CO3,K1=4.3×10-7,K2=5.6×10-11,草酸H2C2O4,K1=5.9×10-2,K2=6.4×10-50.1 mol/L Na2CO3溶液的pH____________0.1 mol/L Na2C2O4溶液的pH。(选填“大于”、“小于”或“等于”)等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是___________。
若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____________。(选填编号)
A.[H+]>[HC2O4-]>[HCO3-]>[CO32-]
B.[HCO3-]>[HC2O4-]>[C2O42-]>[CO32-]
C.[H+]>[HC2O4-]>[C2O42-]>[CO32-]
D.[H2CO3] >[HCO3-]>[HC2O4-]>[CO32-]
(4)人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO3- H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。___________________________
H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。___________________________
-
随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点。
完成下列填空:
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:
CO2(g)+4H2(g) CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
已知H2的体积分数随温度升高而增加。
若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化。(选填“增大”、“减小”或“不变”)
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
| [CO2]/mol·L-1 | [H2]/mol·L-1 | [CH4]/mol·L-1 | [H2O]/mol·L-1 |
| 平衡Ⅰ | a | b | c | d |
| 平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为_________。
(3)碳酸:H2CO3,Ki1=4.3×10-7,Ki2=5.6×10-11
草酸:H2C2O4,Ki1=5.9×10-2,Ki2=6.4×10-5
0.1 mol/L Na2CO3溶液的pH____________0.1 mol/L Na2C2O4溶液的pH。(选填“大于”、“小于”或“等于”)
等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是___________。
若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____。(选填编号)
a.[H+]>[HC2O4-]>[HCO3-]>[CO32-]
B.[HCO3-]>[HC2O4-]>[C2O42-]>[CO32-]
c.[H+]>[HC2O4-]>[C2O42-]>[CO32-]
D.[H2CO3] >[HCO3-]>[HC2O4-]>[CO32-]
(4)人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO3- H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。
H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。
____________________________________________________________________________________
-
随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点。
完成下列填空:
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:
CO2(g)+4H2(g) CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
已知H2的体积分数随温度的升高而增加。
若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化。(选填“增大”、“减小”或“不变”)
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
| [CO2]/mol·L-1 | [H2]/mol·L-1 | [CH4]/mol·L-1 | [H2O]/mol·L-1 |
| 平衡Ⅰ | a | b | c | d |
| 平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为_________。
(3)碳酸:H2CO3,Ki1=4.3×10-7,Ki2=5.6×10-11
草酸:H2C2O4,Ki1=5.9×10-2,Ki2=6.4×10-5
0.1 mol/L Na2CO3溶液的pH____________0.1 mol/L Na2C2O4溶液的pH。(选填“大于”“小于”或“等于”)
等浓度广东草酸溶液和碳酸溶液中,氢离子浓度较大的是___________。
若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____。(选填编号)
a.[H+]>[HC2O4-]>[HCO3-]>[CO32-] b.[HCO3-]>[HC2O4-]>[C2O42-]>[CO32-]
c.[H+]>[HC2O4-]>[C2O42-]>[CO32-] d.[H2CO3] >[HCO3-]>[HC2O4-]>[CO32-]
(4)人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO3- H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。
H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。
________________________________
-
随着科学技术的发展和环保要求不断提高,CO2的捕集利用技术成为研究的重点。
I.工业上使用的捕碳剂有NH3和(NH4)2CO3,它们与CO2可发生如下可逆反应:
NH3(l)+H2O(l)+CO2(g)  NH4HCO3(aq) ΔH1
NH4HCO3(aq) ΔH1
2NH3(l)+H2O(l)+CO2(g)  (NH4)2CO3(aq) ΔH2
(NH4)2CO3(aq) ΔH2
(NH4)2CO3(aq)+H2O(l)+CO2(g)  2NH4HCO3(aq) ΔH3
2NH4HCO3(aq) ΔH3
则ΔH3 =______(用含ΔH1 、ΔH2 的代表式表示)。
II.目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的化学反应方程式为:CO2 (g)+4H2(g)  CH4(g)+2H2O(g),已知:H2的体积分数随温度的升高而增加。
CH4(g)+2H2O(g),已知:H2的体积分数随温度的升高而增加。
(1)该反应的ΔS_____0(填“>”、“=”、“<”),该反应的ΔH____0(填“>”、“<”)。
(2)在恒容密闭容器中通入等物质的量的CO2和H2并发生上述反应,温度T下,CO2物质的量浓度c(CO2)随时间t变化的曲线如下图所示。下列能说明反应达到平衡状态的是___。
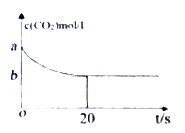
A.体系压强保持不变
B.混合气体密度保持不变
C.甲烷和水蒸气的物质的量之比保持不变
D.H2的质量分数保持不变
(3)温度T下,反应前20秒的平均速率v(H2)= _________(用含a、b的代数式表示)。
(4)温度T下,该反应的平衡常数K=_________(用含a、b的代数式表示)。
(5)若降低温度,反应重新达到平衡,则v(正)_________;CO2转化率_________(填“增大”“减小”或“不变”)。
III.工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如下:
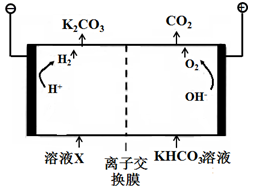
①在阳极区发生的反应包括_________和H++HCO3-=CO2↑+H2O。
②简述CO32-在阴极区再生的原理:_________。
-
随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究新的热点。 完成下列问题:
(1)CO2催化加氢合成CH3OCH3是一种CO2转化方法,其过程中主要发生下列反应:
反应I:
反应Ⅱ: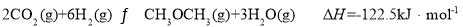
①写出CO和H2合成CH3OCH3的热化学方程式____。
②分别在2L恒温密闭容器甲(恒温恒容)、乙(恒温恒压)中,加入CO2和H2各1 mol的混合气体,假设只发生反应Ⅱ,则两容器中反应达平衡后放出或吸收的热量较多的是____(填“甲”或“乙”)。当反应5 min时,测得甲容器中压强变为原来的一半,则用CO2表示的反应的速率= ___。
③在恒压、CO2和H2的起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图。其中:
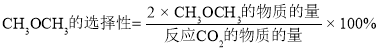
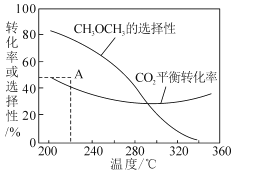
i)温度高于300℃,温度对CO2平衡转化率影响较大的是反应____(填“I”或“Ⅱ”)。
ii)220℃时,在催化剂作用下CO2与H2反应一段时间后,测得CH3OCH3的选择性为48%(图中A点)。不改变反应时间和温度,一定能提高CH3OCH3选择性的措施可以是____(任答一条)。
(2)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为____(写离子符号);若所得溶液c(HCO3-):c(CO32-)=1:5,溶液pH= ___。(室温下,H2CO3的 )
)
-
随着科学技术的发展和环保要求的不断提高, 废气的处理已成为研究的热点,图1是以
废气的处理已成为研究的热点,图1是以 为主要原料的化工产品的生产过程。
为主要原料的化工产品的生产过程。

(1)关于侯氏制碱法,回答下列问题:
①写出 的电子式______。
的电子式______。
②实验室制取 的化学方程式______。
的化学方程式______。
③由侯氏制碱法获得 分为两步:
分为两步:
I.
II.______。
(2)尿素是重要的氮肥,请写出由 生产尿素的化学方程式______。
生产尿素的化学方程式______。
(3) 催化加氢制取汽油过程中发生如下反应:
催化加氢制取汽油过程中发生如下反应:




已知:在一定温度下,10L的密闭容器中,通入
 和
和
 ,反应过程如图2所示,回答下列问题:
,反应过程如图2所示,回答下列问题:
①计算该温度下反应的平衡常数 ______。
______。
②下列可以判断该反应达到平衡状态的是______。
 单位时间内,
单位时间内, 的减少量等于CO的生成量
的减少量等于CO的生成量
 反应容器内的压强不发生变化
反应容器内的压强不发生变化
 混合气体中
混合气体中 的浓度不再发生改变
的浓度不再发生改变
-
捕集CO2的技术对解决全球温室效应意义重大。目前国际空间站处理CO2的一个重要方法是将CO2还原,涉及的化学反应如下:CO2(g)+4H2(g)  CH4(g)+2H2O(g)+Q(Q>0)
CH4(g)+2H2O(g)+Q(Q>0)
完成下列填空:
(1)该反应的平衡常数表达式为________________________________。如果改变某种条件,平衡向正反应方向移动,则平衡常数________(填写编号)。
a、一定增大 b、一定减小 c、可能增大 d、可能减小 e、可能不变
(2)为了提高CO2的捕获百分率,可采取的措施是____________________。(任写一条)
(3)向2L某密闭容器充入1mol CO2和4mol H2,一定条件下发生上述反应。5min末测得气体的物质的量减少了20%,则0~5min内CO2的平均反应速率为_______________。CO2还可应用于纯碱工业。工业生产纯碱的过程中,向饱和的氨化食盐水中通入足量CO2的生产环节又被称为“碳酸化”。
(4)碳酸化时产生的现象是____________________________。碳酸化过程中,溶液中c(CO32-)的变化情况为____________________。
(5)碳酸化后过滤,留在滤液中的阳离子主要有_______________(填写化学式)。简述检验滤液中Cl- 离子的实验操作。________________________________
-
捕集CO2的技术对解决全球室效应意又重大。目前国际空间站处理CO2的一个重要方法是将CO2还原,涉及的化学反应如:CO2(g)+4H2(g) CH4(g)+2H2O(g)+Q(Q>0),完成下列填空:
CH4(g)+2H2O(g)+Q(Q>0),完成下列填空:
(1)该反应的平衡常数表达式为_______________________________。如果改变某种条件,平衡向正反应方向移动。则平衡常数K值___________(填写编号)。
a.一定增大 b.一定减小 c.可能增大 d.可能减小 e.可能不变
(2)为了提高CO2的捕获百分率又能加快反应速率的措施是___________________(任写一条)。
(3)向2L某密闭容器充入1mol CO2和4mol H2,一定条件下发生上述反应,5min末测得气体的物质的量减少了20%,则0-5min内CO2的平均反应速率为_________________。CO2还可应用于纯碱工业,工业生产纯碱的过程中,向饱和的氨化食盐水中通入足量CO2的生产环节又被称为“碳酸化”。
(4)碳酸化时产生的现象是______________________________________________________。碳酸化过程中,溶液中c(CO32-)的变化情况为_____________________________________。
(5)碳酸化后过滤,留在滤液中的阳离子主要有_______________(填写化学式)。简述检验滤液中Cl-离子的实验操作:________________________________________________________。
-
(6分)随着我国工业化水平的不断发展,研究空气污染、废水处理等问题成为重要课题。
(1)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
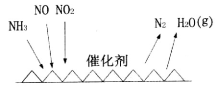
①SCR技术中的氧化剂为____________
②当NO2与NO的物质的量之比为1:l时,与足量氨气在一定条件下发生反应。该反应的化学方程式为_______。当有3 mol电子发生转移时,则参与反应的NO的物质的量为________。
(2)电镀废水中常含有毒的NaCN、HCN等。NaCN水溶液显碱性的原因是_____________(用离子方程式表示);HCN的Ka=6.17×10-10,用NaOH溶液调节含CN-的废水至pH=9,此时废水中c(CN-)_______c(HCN)(填“>”、“<”或“=”)。
(3)室温下有如下数据:草酸(H2C2O4)的K1=5.4×10-2,K2=5.4×10-5;醋酸的电离平衡常数K=1.75×10-5;碳酸的电离平衡常数K1=4.2×10-7,K2=4.5×10-11;Ksp(CaC2O4)=5.0×10-9;Ksp (CaCO3)=2.5×10-9
①用醋酸溶液鉴别CaC2O4和CaCO3两种白色固体的实验现象是___________;
②向0.6 mol·L-1的Na2CO3溶液中加入足量CaC2O4粉末后(忽略溶液体积变化),充分搅拌,发生反应:CO32-(aq)+ CaC2O4 (s) CaCO3 (s)+ C2O42-(aq),静置后沉淀转化达到平衡,此时溶液中的c(C2O42-)(不考虑其他诸如水解之类副反应)为_____________。
CaCO3 (s)+ C2O42-(aq),静置后沉淀转化达到平衡,此时溶液中的c(C2O42-)(不考虑其他诸如水解之类副反应)为_____________。
-
随着现代工业的发展,二氧化碳污染的处理成为科学研究的重点,回答下列问题:
I.有人提出利用H2还原CO2使其转化为有机化工的主要原料乙烯。
(1)查阅资料:H2的燃烧热为285.8kJ/mol,C2H4的燃烧热为l41lkJ/mol,lmolH2O(1)转化为H2O(g)需吸收44kJ的热量。则反应6H2(g)+2CO2(g)  C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
△H=___________kJ/mol。
(2)下图是探究不同温度对CO2的转化率和催化剂的催化效率影响的示意图。
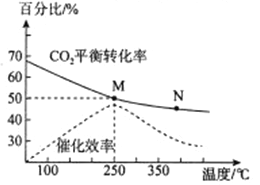
①生产中通常选用的温度最好是___________,理由是___________。
②图中表示的化学平衡常数:M___________N(填>、=、<)
③250℃时,在2L密闭容器中分别充入6molH2和2 molCO2,到达平衡时体系中C2H4的体积分数为___________。
Ⅱ.CO在一定条件下,能与H2合成二甲醚:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)。
CH3OCH3(g)+3H2O(g)。
(1)在1L的密闭容器中分别充入2.5molH2与 bmol CO2发生反应,在不同温度下达到平衡状态时测得实验数据如下表:
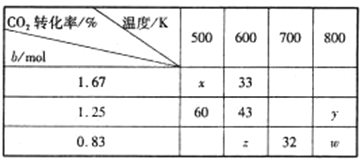
①到达平衡时若升高温度,则上述平衡___________方向移动(填“正反应”或“逆反应”)。
②转化率:x___________y(填>、=、<)
(2)新型高效的二甲醚燃料电池工作时总反应式:CH3OCH3+3O2=2CO2+3H2O。
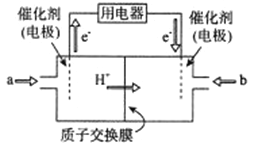
①该电池的负极是___________(填a或b),负极电极反应式为___________;
②利用该电池冶铝,若制得金属铝54g理论上消耗二甲醚___________g。
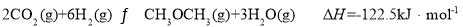
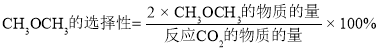

)






