-
在工业废气和汽车尾气中含有多种氮氧化物,氮氧化物能破坏臭氧层,产生光化学烟雾,是造成大气污染的来源之一。
(1)处理 NO 尾气通常是将 NO 与 O2 混合通入碱液中吸收。已知一定条件下有下列反应:
Ⅰ:2N2O5(g)  4NO2(g)+O2(g) △H1
4NO2(g)+O2(g) △H1
Ⅱ:2NO2(g) 2NO(g)+O2(g) △H2
2NO(g)+O2(g) △H2
Ⅲ:2NaOH(aq)+N2O5(g)=2NaNO3(aq)+H2O(1) △H3
写出 NO 和O2 的混合物溶于NaOH 溶液生成硝酸盐的热化学方程式______。
(2)常温下,NO 极易被 O2 氧化为 NO2,温度高于 423K 时,NO2 发生分解:2NO2(g)  2NO(g)+O2(g)△H=114kJ·mol -1,实验测得:
2NO(g)+O2(g)△H=114kJ·mol -1,实验测得:
υ正=υ(NO2)消耗=k 正C2(NO2), υ逆=υ(NO)消耗=2υ(O2) 消耗=k 逆c2(NO)·c( O2),k 正、k 逆 为速率常数,受温度影响。不同温度下,将 NO2 置于体积为 VL 的密闭容器中,NO2 的物质的量的浓度与反应时间的关系如图所示:
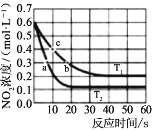
①T1 温度下 0-10s 内,O2 的反应速率υ(O2)=______、平衡常数 KT1=___________。
②T1 温度下,要减少 NO2 的分解率,并缩短达到平衡的时间,可采取的单一措施有______
③平衡常数KT1 ______ KT2 填“大于”“小于”或“等于”,下同);反应速率υa_______υb。
④计算 c 处υ正/υ逆=______。
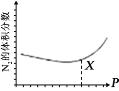
(3)NO 也 可 通 过 如 下 反 应 处 理 :6NO(g)+4NH3(g) =5N2(g) +6H2O(g);一定条件下,平衡时 N2 的体积分数与压强的关系如图所示。N2 的体积分数先减小后增大的原因是______。
-
工业废气和汽车尾气含有多种氮氧化物,以NOx表示,NOx能破坏臭氧层,产生光化学烟雾,是造成大气污染的来源之一。按要求回答下列问题:
(1)NO2与N2O4存在以下转化关系:2NO2(g) N2O4(g)。
N2O4(g)。
①已知:标准状况(25℃、101kPa)下,由最稳定的单质生成1mol化合物的焓变(或反应热),称为该化合物的标准摩尔生成焓。几种氧化物的标准摩尔生成焓如表所示:
| 物质 | NO(g) | NO2(g) | N2O4(g) | CO(g) |
| 标准摩尔生成焓/(kJ·mol-1) | 90.25 | 33.18 | 9.16 | -110.53 |
则NO2转化成N2O4的热化学方程式为__。
②将一定量N2O4投入固定容积的恒温容器中,下述现象能说明反应达到平衡状态的是__(填标号)。
A.v(N2O4)=2v(NO2) B.气体的密度不变
C. 不变 D.气体的平均相对分子质量不变
不变 D.气体的平均相对分子质量不变
③达到平衡后,保持温度不变,将气体体积压缩到原来的一半,再次达到平衡时,混合气体颜色____填“变深”“变浅”或“不变”),判断理由是___。
(2)在容积均为2L的甲、乙两个恒容密闭容器中,分别充入等量NO2,发生反应:2NO2(g) 2NO(g)+O2(g)。保持温度分别为T1、T2,测得
2NO(g)+O2(g)。保持温度分别为T1、T2,测得 n(NO2)与n(O2)随时间的变化如图所示:
n(NO2)与n(O2)随时间的变化如图所示:
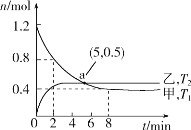
①T1时,反应从开始到第2min,平均速率v(O2)=__,该温度下平衡常数K=__。
②实验测得:v正=k正c2(NO2),v逆=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响,下列有关说法正确的是__(填标号)。
A.反应正向放热
B.a点处,v逆(甲)<v逆(乙)
C.k正(T2)>k正(T1)
D.温度改变,k正与k逆的比值不变
(3)硫代硫酸钠(Na2S2O3)在碱性溶液中是较强的还原剂,可用于净化氧化度较高的NOx废气,使之转化为无毒、无污染的N2。请写出NO2与硫代硫酸钠碱性溶液反应的离子方程式:__。
-
硝酸工业尾气中的NO、NO2进入大气后,会形成光化学烟雾、破坏臭氧层等。可用氢氧化钠溶液对含氮氧化物的尾气进行处理,反应的化学方程式如下:NO2+NO+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO2+NaNO3+H2O。氨气也可以用来处理氮氧化物。例如,氨气与一氧化氮可发生如下反应:4NH3+6NO=5N2+6H2O。将一定量NO和NO2的混合气体通入300mL5mol/LNaOH溶液中,恰好被完全吸收。下列说法不正确的是
A.在用氨气处理氮氧化物时,氮氧化物发生还原反应
B.所得溶液中NaNO3和NaNO2的物质的量之比可能为2:1
C.若用氨气处理,所需氨气在标准状况下的体积可能为39.2L
D.原混合气体中NO在标准状况下的体积可能为16.8L
-
以下非金属氧化物与其引起的环境问题及主要来源对应正确的是 ( )
| 氧化物 | 环境问题 | 主要来源 |
| A | CO2 | 酸雨 | 化石燃料的燃烧 |
| B | SO2 | 光化学烟雾 | 汽车尾气的排放 |
| C | NO2 | 温室效应 | 工厂废气的排放 |
| D | CO | CO中毒 | 燃料的不完全燃烧 |
-
以下非金属氧化物与其引起的环境问题及主要来源对应正确的是( )
| 氧化物 | 环境问题 | 主要来源 |
| A | CO2 | 酸雨 | 化石燃料的燃烧 |
| B | SO2 | 光化学烟雾 | 汽车尾气的排放 |
| C | NO2 | 温室效应 | 工厂废气的排放 |
| D | CO | CO中毒 | 汽车尾气和化石燃料的不完全燃烧 |
-
以下非金属氧化物与其引起的环境问题及主要来源对应正确的是
| 氧化物 | 环境问题 | 主要来源 |
| A | CO | 煤气中毒 | 含碳燃料的不完全燃烧 |
| B | SO2 | 光化学烟雾 | 汽车尾气的排放 |
| C | NO2 | 温室效应 | 工厂废气的排放 |
| D | CO2 | 酸雨 | 化石燃料的燃烧 |
-
以下非金属氧化物与其引起的环境问题及主要来源对应正确的是
| 氧化物 | 环境问题 | 主要来源 |
| A | CO2 | 酸雨 | 化石燃料的燃烧 |
| B | SO2 | 光化学烟雾 | 汽车尾气的排放 |
| C | NO2 | 温室效应 | 工厂废气的排放 |
| D | CO | CO中毒 | 燃料的不完全燃烧 |
-
以下非金属氧化物与其引起的环境问题及主要来源对应正确的是
| 氧化物 | 环境问题 | 主要来源 |
| A | CO2 | 酸雨 | 化石燃料的燃烧 |
| B | SO2 | 光化学烟雾 | 汽车尾气的排放 |
| C | NO2 | 温室效应 | 工厂废气的排放 |
| D | CO | CO中毒 | 燃料的不完全燃烧 |
-
以下非金属氧化物与其引起的环境问题及主要来源对应正确的是
| 氧化物 | 环境问题 | 主要来源 |
| A | CO2 | 酸雨 | 化石燃料的燃烧 |
| B | SO2 | 光化学烟雾 | 汽车尾气的排放 |
| C | NO2 | 温室效应 | 工厂废气的排放 |
| D | CO | CO中毒 | 燃料的不完全燃烧 |
-
以下非金属氧化物与其引起的环境问题及主要来源对应正确的是( )
| 选项 | 氧化物 | 环境问题 | 主要来源 |
| A | CO | 破坏臭氧层 | 汽车尾气和化石燃料的不完全燃烧 |
| B | SO2 | 温室效应 | 汽车尾气的排放 |
| C | NO2 | 光化学烟雾 | 工厂废气的排放及汽车尾气 |
| D | CO2 | 酸雨 | 化石燃料的燃烧 |
A.A B.B C.C D.D
4NO2(g)+O2(g) △H1
2NO(g)+O2(g) △H2
2NO(g)+O2(g)△H=114kJ·mol -1,实验测得:


