-
钙钛矿太阳能电池具有转化效率高、低成本等优点,是未来太阳能电池的研究方向。回答下列问题:
(1)下列状态的钙中,电离最外层一个电子所需能量最大的是__________(填字母标号)。
A.[Ar]4s1 B.[Ar]4s2 C.[Ar]4s14p1 D.[Ar]4p1
(2)基态钛原子的核外价电子轨道表达式为____________。
(3)一种有机金属卤化钙钛矿中含有NH2-CH=NH2+,该离子中氮原子的杂化类型为___________,其对应分子NH2-CH=NH的熔沸点高于CH3CH2CH=CH2的熔沸点的原因为__________。
(4)一种无机钙钛矿CaxTiyOz的晶体结构如图所示,则这种钙钛矿化学式为___________,已知Ca和O离子之间的最短距离为a pm,设阿伏加德罗常数的值为NA,则这种钙钛矿的密度是___________g·cm-3(列出计算表达式)。
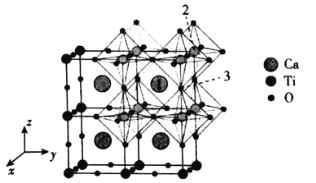
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中原子1的坐标为( ,
, ,
, ),则原子2和3的坐标分别为__________、__________。
),则原子2和3的坐标分别为__________、__________。
-
新型钙钛矿太阳能电池是近几年来的研究热点,具备更加清洁、便于应用、制造成本低和效率高等显著优点,其中一种钙钛矿太阳能电池材料的晶胞如图。回答下列问题:
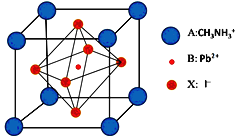
(1)铅或铅盐的焰色反应为绿色,下列有关原理分析的叙述正确的是_________(填字母)。
a.电子从基态跃迁到较高的激发态 b.电子从较高的激发态跃迁到基态
c.焰色反应的光谱属于吸收光谱 d.焰色反应的光谱属于发射光谱
(2)碳原子价层电子的轨道表达式(电子排布图)为_________。基态Pb原子核外电子排布,最后占据能级的电子云轮廓图形状为___________。
(3)CH3NH3+中含有化学键的类型有________(填字母序号),N原子的杂化形式为______,与CH3NH3+互为等电子体的分子为_________
a.极性键 b. 非极性键 c.配位键 d. 离子键 e.σ键 f.π键
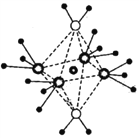
(4)NH4+中H—N—H的键角比NH3中H -N-H的键角大的原因是__________;NH3和水分子与铜离子形成的化合物中阳离子呈轴向狭长的八面体结构(如右图),该化合物加热时首先失去水,请从原子结构角度加以分析:__________。
(5)与I- 紧邻的I- 个数为__________。X射线衍射实验测得晶胞参数:密度为a g·cm-3,则晶胞的边长为____________pm(该物质的相对原子质量为M,NA表示阿伏加德罗常数的值)。
-
新型钙钛矿太阳能电池具备更加清洁、便于应用、制造成本低和效率高等显著优点。 一种钙钛矿太阳能电池材料的晶胞如图所示。
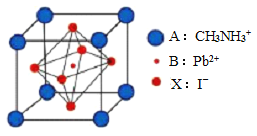
请按要求回答下列有关问题:
(1)构成 CH3NH3 的三种元素中电负性最小的是_____________; 写出碳原子的电子排布式为__________。
(2)Pb 与 C 同主族,比 C 的周期序数大 4,写出 Pb 原子最外层电子的轨道表示式(即电子排布图)__________________。
(3)有关 NH3 的结构与性质探究
① NH3 分子中所含化学键是____________(从“极性键”、“非极性键”、“配位键”、 “离子键”、“σ键”或“ π键”中选填符合的名称);N 原子的杂化形式为__________。
② NH3 分子的 VSEPR 模型名称为_________,分子的空间结构(即立体构型) 为______。
③如图所示,探究 NH3 的性质时,打开止水夹,挤压胶头滴管,可以观察到烧瓶中迅速产生红色喷泉。请用必要的分子结构 与性质的知识和化学用语解释产生该现象的原因:_________、________。

(4)该钙钛矿太阳能电池材料的化学式为________________;该晶胞中,与 I- 紧邻的 I- 个数为_____________; 测定其晶体结构特征最可靠的方法是____________实验。
-
Na3OCl是一种良好的离子导体,具有反钙钛矿晶体结构。回答下列问题:
(1)Ca小于Ti的是_______(填标号)。
A.最外层电子数 B.未成对电子数 C.原子半径 D.第三电离能
(2)由O、Cl元素可组成不同的单质和化合物,其中Cl2O2能破坏臭氧层。
① Cl2O2的沸点比H2O2低,原因是___________________________________。
② O3分子中心原子杂化类型为_______;O3是极性分子,理由是___________________。
(3)Na3OCl可由以下两种方法制得:
方法Ⅰ Na2O + NaCl Na3OCl
Na3OCl
方法II 2Na + 2NaOH + 2NaCl 2Na3OCl + H2↑
2Na3OCl + H2↑
① Na2O的电子式为____________。
② 在方法Ⅱ的反应中,形成的化学键有_______(填标号)。
A.金属键 B.离子键 C.配位键 D.极性键 E.非极性键
(4)Na3OCl晶体属于立方晶系,其晶胞结构如右所示。已知:晶胞参数为a nm,密度为d g·cm-3。
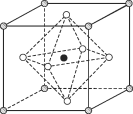
①Na3OCl晶胞中,Cl位于各顶点位置,Na位于_________位置,两个Na之间的最短距离为________nm。
②用a、d表示阿伏加德罗常数的值NA=__________________(列计算式)。
-
Na3OCl是一种良好的离子导体,具有反钙钛矿晶体结构。回答下列问题:
(1)Ca小于Ti的是_______(填标号)。
A.最外层电子数 B.未成对电子数 C.原子半径 D.第三电离能
(2)由O、Cl元素可组成不同的单质和化合物,其中Cl2O2能破坏臭氧层。
① Cl2O2的沸点比H2O2低,原因是___________________________________。
② O3分子中心原子杂化类型为_______;O3是极性分子,理由是___________________。
(3)Na3OCl可由以下两种方法制得:
方法Ⅰ Na2O + NaCl Na3OCl
Na3OCl
方法II 2Na + 2NaOH + 2NaCl 2Na3OCl + H2↑
2Na3OCl + H2↑
① Na2O的电子式为____________。
② 在方法Ⅱ的反应中,形成的化学键有_______(填标号)。
A.金属键 B.离子键 C.配位键 D.极性键 E.非极性键
(4)Na3OCl晶体属于立方晶系,其晶胞结构如右所示。已知:晶胞参数为a nm,密度为d g·cm-3。
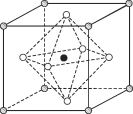
①Na3OCl晶胞中,Cl位于各顶点位置,Na位于_________位置,两个Na之间的最短距离为________nm。
②用a、d表示阿伏加德罗常数的值NA=__________________(列计算式)。
-
Na3OCl是一种良好的离子导体,具有反钙钛矿晶体结构。回答下列问题:
(1)Ca小于Ti的是_______(填标号)。
A.最外层电子数 B.未成对电子数 C.原子半径 D.第三电离能
(2)由O、Cl元素可组成不同的单质和化合物,其中Cl2O2能破坏臭氧层。
① Cl2O2的沸点比H2O2低,原因是___________________________________。
② O3分子中心原子杂化类型为_______;O3是极性分子,理由是___________________。
(3)Na3OCl可由以下两种方法制得:
方法Ⅰ Na2O + NaCl Na3OCl
Na3OCl
方法II 2Na + 2NaOH + 2NaCl 2Na3OCl + H2↑
2Na3OCl + H2↑
① Na2O的电子式为____________。
② 在方法Ⅱ的反应中,形成的化学键有_______(填标号)。
A.金属键 B.离子键 C.配位键 D.极性键 E.非极性键
(4)Na3OCl晶体属于立方晶系,其晶胞结构如右所示。已知:晶胞参数为a nm,密度为d g·cm-3。

①Na3OCl晶胞中,Cl位于各顶点位置,Na位于_________位置,两个Na之间的最短距离为________nm。
②用a、d表示阿伏加德罗常数的值NA=__________________(列计算式)。
-
一种新型钙钛矿太阳能电池具有较高的能量转化率,其组成有多种,主要由 、
、 、
、 、
、 ,
, 、
、 、
、 等离子中的某几种组成。
等离子中的某几种组成。
 中运动在能量最高的能级上的电子自旋方向有_____种;氮与左右相邻的两种元素第一电离能由大到小的顺序为_______。
中运动在能量最高的能级上的电子自旋方向有_____种;氮与左右相邻的两种元素第一电离能由大到小的顺序为_______。
 基态铁原子的核外电子排布式为________,铅元素的电子由________
基态铁原子的核外电子排布式为________,铅元素的电子由________ 填“激发态”或“基态”
填“激发态”或“基态” 跃迁到另一状态时会产生绿色的焰色反应。
跃迁到另一状态时会产生绿色的焰色反应。
 中碳原子的杂化轨道类型为_______,以N原子为中心的几个微粒的空间构型为_________,该离子中
中碳原子的杂化轨道类型为_______,以N原子为中心的几个微粒的空间构型为_________,该离子中 键之间的键角________
键之间的键角________ 中
中 间键角
间键角 填“
填“ ”或“
”或“ ”
” 。
。
 常温下,
常温下, 、
、 、
、 分别为气体、液体、固体。则
分别为气体、液体、固体。则 的晶体类型为_________,从结构角度解释上述三种物质状态的变化:___________________________。
的晶体类型为_________,从结构角度解释上述三种物质状态的变化:___________________________。
 某钙钛矿太阳能电池材料的晶胞如图所示,其晶胞参数为
某钙钛矿太阳能电池材料的晶胞如图所示,其晶胞参数为 、密度为
、密度为 。
。
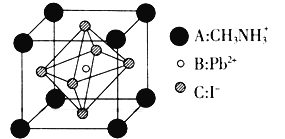
则该晶体中 _________,该晶体的摩尔质量
_________,该晶体的摩尔质量 _____
_____ 用含d、
用含d、 等符号的式子表示,用
等符号的式子表示,用 表示阿伏加德罗常数的值
表示阿伏加德罗常数的值 。
。
-
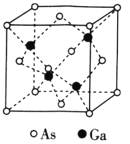
钙钛矿(主要成分是CaTiO3)太阳能薄膜电池制备工艺简单、成本低、效率高,引起了科研工作者的广泛关注,科学家认为钙钛矿太阳能电池将取代硅基太阳能电池的统治地位。
(1)基态Ti原子的价电子排布式为__,能量最高的能级有__个空轨道;Si、P、S第一电离能由小到大顺序是__。
(2)碳和硅的有关化学键键能如表所示:
| 化学键 | C−C | C−H | C−O | Si−Si | Si−H | Si−O |
| 键能/kJ▪mol-1 | 356 | 413 | 336 | 226 | 318 | 452 |
硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是___。
(3)一种新型熔融盐燃料电池以Li2CO3和Na2CO3的熔融盐混合物作电解质,则CO32-的空间构型为___。
(4)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图:
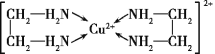
该配离子中含有的化学键类型有__(填字母)。
a.配位键 b.极性键 c.离子键 d.非极性键
一个乙二胺分子中共有__个σ键,C原子的杂化方式为__。
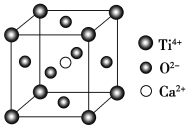
(5)CaTiO3的晶胞为立方晶胞,结构如图所示(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶角)Ca2+的配位数为__,与Ti4+距离最近且相等的O2-有__个;晶体的密度为ρg/cm3,最近的Ti4+和O2-之间的距离为__nm(填计算式)。(CaTiO3的摩尔质量为136g/mol,NA为阿伏加德罗常数)。
-
钙钛矿(主要成分是CaTiO3)太阳能薄膜电池制备工艺简单、成本低、效率高,引起了科研工作者的广泛关注,科学家认为钙钛矿太阳能电池将取代硅基太阳能电池的统治地位。
(1)基态钛原子的电子排布式为______,若钙原子核外有7种能量状态的电子,则钙原子处于____(填“基”或“激发”)态,氧元素所在周期第一电离能由小到大的前三种元素依次是_______。
(2)硅能形成一系列硅氢化合物,如硅烷系列:SiH4、Si2H6;硅烯系列:Si2H4、Si3H6等,其中硅烷广泛应用于微电子、制造太阳能电池。
①上述分子中硅原子存在sp2杂化的是____,属于正四面体的是_____。
②硅烷链长度远小于烷烃,最可能的原因是______,硅烷同系物熔、沸点的变化规律可能是________.
(3) CaTiO3的晶胞为立方晶胞,结构如下图所示:

则与A距离最近且相等的X有___个,M的坐标是_____;若晶胞参数是r pm, NA为阿伏加德罗常数的值,则该晶体的密度是_____g/cm3。
-
钠离子电池具有成本低、能量转换效率高、寿命长等优点。一种钠离子电池用碳基材料(NamCn)作负极,利用钠离子在正负极之间嵌脱过程实现充放电,该钠离子电池的工作原理为Na1-mCoO2+NamCn NaCoO2+Cn。下列说法不正确的是( )
NaCoO2+Cn。下列说法不正确的是( )
A. 放电时,Na+向正极移动
B. 放电时,负极的电极反应式为NamCn-me-=mNa++Cn
C. 充电时,阴极质量减小
D. 充电时,阳极的电极反应式为NaCoO2-me-=Na1-mCoO2+mNa+

,
,
),则原子2和3的坐标分别为__________、__________。











