下列叙述正确的是
①干冰晶体气化时需破坏分子间作用力
②HClO 分子的结构式:H—Cl—O
③NH4Cl 的电子式 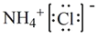
④H2O2分子中既含极性共价键,又含非极性共价键
⑤由于 H—F 键比 H—Cl 键强,所以 HF 的沸点比 HCl 的沸点高
⑥NaHSO4 在溶于水时发生电离,破坏了离子键和共价键
⑦用电子式表示溴化氢的形成过程为:
A.①②⑤ B.②④⑥ C.③⑤⑦ D.①④⑥
高一化学单选题中等难度题
下列叙述正确的是
①干冰晶体气化时需破坏分子间作用力
②HClO 分子的结构式:H—Cl—O
③NH4Cl 的电子式 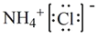
④H2O2分子中既含极性共价键,又含非极性共价键
⑤由于 H—F 键比 H—Cl 键强,所以 HF 的沸点比 HCl 的沸点高
⑥NaHSO4 在溶于水时发生电离,破坏了离子键和共价键
⑦用电子式表示溴化氢的形成过程为:
A.①②⑤ B.②④⑥ C.③⑤⑦ D.①④⑥
高一化学单选题中等难度题
下列叙述正确的是
①干冰晶体气化时需破坏分子间作用力
②HClO 分子的结构式:H—Cl—O
③NH4Cl 的电子式 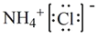
④H2O2分子中既含极性共价键,又含非极性共价键
⑤由于 H—F 键比 H—Cl 键强,所以 HF 的沸点比 HCl 的沸点高
⑥NaHSO4 在溶于水时发生电离,破坏了离子键和共价键
⑦用电子式表示溴化氢的形成过程为:
A.①②⑤ B.②④⑥ C.③⑤⑦ D.①④⑥
高一化学单选题中等难度题查看答案及解析
下列说法错误的是( )
A.HCl、NaCl溶于水,破坏的化学键类型不同
B.氢氧化钠在熔融状态下离子键被削弱,形成自由移动的离子,具有导电性
C.干冰是分子晶体,其气化过程中只需克服分子间作用力
D.常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构
高一化学单选题简单题查看答案及解析
下列说法正确的是( )
A.干冰升华和液氯气化时要破坏不同的微粒间作用力
B.CO2和SiO2具有相同的化学键类型和晶体类型
C.水结成冰体积膨胀、密度变小,这一事实与水中存在氢键有关
D.盐酸能电离出氢离子和氯离子,所以HCl存在离子键
高一化学选择题简单题查看答案及解析
下列叙述正确的是( )
A.固态Na2O2和熔融态NaHSO4中的阴、阳离子个数比不同
B.每个水分子内含有两个氢键
C.碘晶体受热转变成碘蒸气,破坏了共价键
D.干冰溶于水生成碳酸的过程只需克服分子间作用力
高一化学单选题简单题查看答案及解析
下列叙述不正确的是: ( )
A. 干冰变为二氧化碳气体,需吸收能量,是因为分子间作用力被破坏
B. 碳酸氢铵是典型离子化合物,其受热分解产生氨气不仅破坏离子键还破坏了共价键
C. H2O比H2S更稳定,是因为H2O分子间形成了氢键
D. 共价化合物中一定只含共价键
高一化学选择题中等难度题查看答案及解析
下列说法正确的是
A.H2O2中既有离子键又有共价键
B.HCl溶于水能电离出H+和Cl−,所以HCl是离子化合物
C.干冰熔化破坏共价键和分子间作用力
D.PCl3分子中每个原子的最外层都具有8电子的稳定结构
高一化学单选题中等难度题查看答案及解析
下列说法正确的是( )
A.Mg3N2晶体中的化学键是共价键
B.某物质含有离子键,则该物质在任何条件下均能导电
C.干冰是分子晶体,其气化过程中只需克服分子间作用力
D.常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构
高一化学选择题中等难度题查看答案及解析
下列说法不正确的是( )
A. 干冰升华和液氯气化时,都只需克服分子间作用力
B. 氯化氢气体溶于水产生H+和Cl-,所以HCl是离子化合物
C. 硫酸氢钠晶体溶于水,需要克服离子键和共价键
D. 加热氯化铵固体使其分解,需克服离子键和共价键
高一化学单选题简单题查看答案及解析
下列说法不正确的是( )
A.氢氧化钠晶体熔化时只破坏了离子键
B.HCl、HBr、HI均是强酸
C.BF3分子中所有原子的最外层都达到8电子稳定结构
D.碘升华只克服了分子间作用力
高一化学单选题简单题查看答案及解析
以下说法正确的是
A.C60与金刚石互为同素异形体,它们都属于原子晶体
B.干冰升华既克服了分子间作用力,也破坏了共价键
C.金属元素和非金属元素形成的化合物在熔融状态下一定能导电
D.NaCl晶体溶于水破坏了Na+和Cl-之间的离子键
高一化学选择题中等难度题查看答案及解析