-
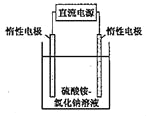
氨氮废水是生活中常见污染物之一,可用电解法加以去除。实验室用石墨电极电解一定浓度的(NH4)2SO4与NaCl混合溶液来模拟该过程。
(1)电解处理氨氮废水电解过程中,溶液初始Cl-浓度和pH对氨氮去除速率与能耗(处理一定量氨氮消耗的电能)的影响关系如图1和图2所示:
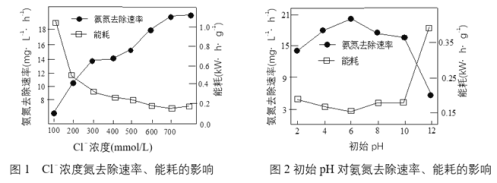
①根据图中数据,处理废水合适的条件是_______________。
②实验中发现阳极会持续产生细小气泡,气泡上浮过程中又迅速消失。结合图1,用电极反应式和离子方程式解释Cl-去除氨氮的原因_______________。
③图1中当Cl-浓度较低时、图2中当初始pH达到12时,均出现氨氮去除速率低而能耗高的现象,共同原因是_______________。
(2)氨的定量测定使用下图装置检测废水中的氨氮总量是否合格。
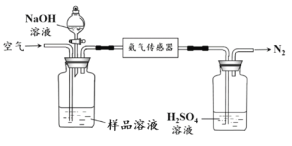
①利用平衡原理分析含氨氮水样中加入NaOH溶液的作用:_______________。
②若利用氨气传感器将1 L水样中的氨氮完全转化为N2时,转移电子的物质的量为6×10-4 mol,则样品混合液中氨氮(以氨气计)含量为_______________mg·L-1。
-
在实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程(如图),乙醛在两电极分别转化为乙醇和乙酸。下列对电解过程的分析正确的是
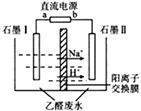
A.以铅蓄电池为电源,则a极为Pb电极
B.石墨Ⅱ电极附近的pH逐渐减小
C.阳极反应为CH3CHO+H2O-2e-=CH3COOH+2H+
D.每处理含8.8g乙醛的废水,转移电子的数目为0.4NA
-
高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
| c(NaOH) | 阴极现象 | 阳极现象 |
| 1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
| 10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
| 15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
下列说法不正确的是
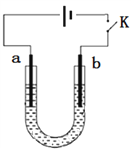
A. a为铁钉,b为石墨
B. 阴极主要发生反应:2H2O + 2e-=== H2↑+ 2OH-
C. 高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-=== FeO42-+ 4H2O
D. 制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
-
高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
| c(NaOH) | 阴极现象 | 阳极现象 |
| 1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
| 10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
| 15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
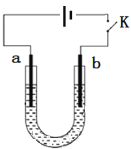
下列说法不正确的是
A. a为铁钉,b为石墨
B. 阴极主要发生反应:2H2O + 2e-=== H2↑+ 2OH-
C. 高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-=== FeO42-+ 4H2O
D. 制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
-
高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
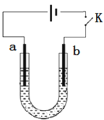
| c(NaOH) | 阴极现象 | 阳极现象 |
| 1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
| 10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
| 15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
下列说法正确的是( )
A.a为石墨,b为铁钉
B.阴极主要发生反应 4OH--4e-== O2↑+ 2H2O
C.高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-== FeO42-+ 4H2O
D.制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
-
高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
| c(NaOH) | 阴极现象 | 阳极现象 |
| 1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
| 10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
| 15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
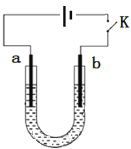
下列说法不正确的是
A. a为铁钉,b为石墨
B. 阴极主要发生反应:2H2O + 2e-=== H2↑+ 2OH-
C. 高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-=== FeO42-+ 4H2O
D. 制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
-
高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
| c(NaOH) | 阴极现象 | 阳极现象 |
| 1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
| 10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
| 15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
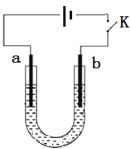
下列说法不正确的是
A. a为铁钉,b为石墨
B. 阴极主要发生反应:2H2O + 2e-=== H2↑+ 2OH-
C. 高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-=== FeO42-+ 4H2O
D. 制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
-
高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
| c(NaOH) | 阴极现象 | 阳极现象 |
| 1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
| 10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
| 15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
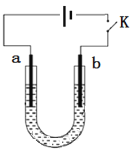
下列说法不正确的是
A. a为铁钉,b为石墨
B. 阴极主要发生反应:2H2O + 2e-=== H2↑+ 2OH-
C. 高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-=== FeO42-+ 4H2O
D. 制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
-
生活污水中的氮和磷主要以铵盐和磷酸盐形式存在,可用铁、石墨作电极,用电解法从溶液中去除。电解时:如图1原理所示可进行除氮,有Cl-存在时,主要依靠有效氯(HClO、ClO-)将NH4+或NH3氧化为N2;翻转电源正负极,可进行除磷,原理是利用Fe2+将PO43-转化为Fe3(PO4)2沉淀。图2为某含Cl-污水在氮磷联合脱除过程中溶液pH的变化。下列说法正确的是( )
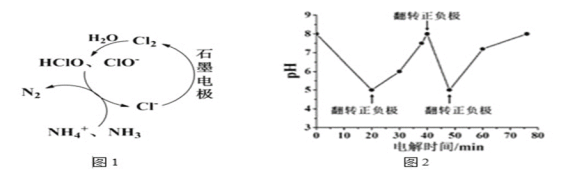
A.电解法除氮有效氯HClO氧化NH4+的离子方程式为3HClO+2NH4+=3Cl-+N2↑+3H2O+5H+
B.溶液pH越小有效氯浓度越大,氮的去除率越高
C.图2中20~40min脱除的元素是磷元素,此时阴极电极反应式为2H++2e-=H2↑
D.图2中0~20min脱除的元素是氮元素,此时铁作阳极
-
实验室模拟“间接电化学氧化法”处理氨氮废水。以硫酸铵和去离子水配制成初始的模拟废水,并以NaCl调剂溶液中氯离子浓度,如图所示进行模拟实验。
(1)阳极反应式为___。
(2)去除NH4+的离子反应方程式为___。