-
(12分)[化学---化学与技术]工业上利用氨氧化获得的高浓度NOx气体(含NO、NO2)制备NaNO2、NaNO3,工艺流程如下: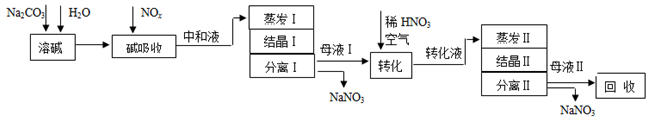
已知:Na2CO3+NO+NO2=2NaNO2+CO2
(1)中和液所含溶质除NaNO2及少量Na2CO3外,还有__________(填化学式)。
(2)中和液进行蒸发Ⅰ操作时,应控制水的蒸发量,避免浓度过大,目的是_______。蒸发Ⅰ产生的蒸气中含有少量的NaNO2等有毒物质,不能直接排放,将其冷凝后用于流程中的_______(填操作名称)最合理。
(3)母液Ⅰ进行转化时加入稀HNO3的目的是_______。母液Ⅱ需回收利用,下列处理方法合理的是________。
a.转入中和液 b.转入结晶Ⅰ操作
c.转入转化液 d.转入结晶Ⅱ操作
(4)若将NaNO2、NaNO3两种产品的物质的量之比设为2:1,则生产1.38吨NaNO2时,Na2CO3的理论用量为______吨(假定Na2CO3恰好完全反应)。
-
工业上利用氨氧化获得的高浓度NOx气体(含NO、NO2)制备NaNO2、NaNO3,工艺流程如下: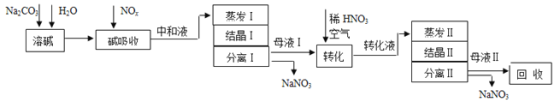
已知:Na2CO3+NO+NO2=2NaNO2+CO2
(1)中和液所含溶质除NaNO2及少量Na2CO3外,还有__________(填化学式)。
(2)中和液进行蒸发Ⅰ操作时,应控制水的蒸发量,避免浓度过大,目的是_______。蒸发Ⅰ产生的蒸气中含有少量的NaNO2等有毒物质,不能直接排放,将其冷凝后用于流程中的_______(填操作名称)最合理。
(3)母液Ⅰ进行转化时加入稀HNO3的目的是_______。母液Ⅱ需回收利用,下列处理方法合理的是________。
a.转入中和液 b.转入结晶Ⅰ操作
c.转入转化液 d.转入结晶Ⅱ操作
(4)若将NaNO2、NaNO3两种产品的物质的量之比设为2:1,则生产1.38吨NaNO2时,Na2CO3的理论用量为______吨(假定Na2CO3恰好完全反应)。
-
工业上利用氨氧化获得的高浓度NOx气体(含NO、NO2)制备NaNO2、NaNO3,工艺流程如下:
已知:Na2CO3+NO+NO2=2NaNO2+CO2
(1)中和液所含溶质除NaNO2及少量Na2CO3外,还有__________(填化学式)。
(2)中和液进行蒸发Ⅰ操作时,应控制水的蒸发量,避免浓度过大,目的是_______。蒸发Ⅰ产生的蒸气中含有少量的NaNO2等有毒物质,不能直接排放,将其冷凝后用于流程中的_______(填操作名称)最合理。
(3)母液Ⅰ进行转化时加入稀HNO3的目的是_______。母液Ⅱ需回收利用,下列处理方法合理的是________。
a.转入中和液 b.转入结晶Ⅰ操作
c.转入转化液 d.转入结晶Ⅱ操作
(4)若将NaNO2、NaNO3两种产品的物质的量之比设为2:1,则生产1.38吨NaNO2时,Na2CO3的理论用量为______吨(假定Na2CO3恰好完全反应)。
-
利用硝酸厂尾气中较高浓度NOx气体(含NO、NO2)制备NaNO2、NaNO3,流程如下:
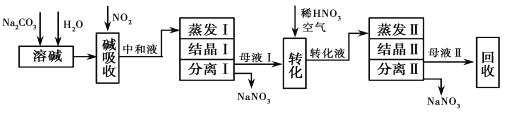
已知:NaOH+NO+NO2═2NaNO2+H2O
(1)写出Na2CO3溶液和NO、NO2反应的化学方程式_______________________________。
(2)中和液所含溶质除NaNO2及少量Na2CO3 外,还有少量___________和___________(填化学式)。
(3)中和液进行蒸发Ⅰ操作时,应控制水的蒸发量,避免浓度过大,目的是____________________;蒸发Ⅰ产生的蒸气中含有少量的NaNO2等有毒物质,不能直接排放,将其冷凝后用于流程中的______________(填操作名称)最合理。
(4)母液Ⅱ需 回收利用,下列处理方法合理的是________________________。
a.转入中和液 b.转入结晶Ⅰ操作 c.转入转化液 d.转入结晶Ⅱ操作
(5)NaNO2能与N2H4反应生成NaN3,该反应中NaNO2_____(填“被氧化”或“被还原”)
N2H4 的电子式是____________________,NaN3 中含有的化学键类型是______________________。
(6)若将NaNO2、NaNO3两种产品的物质的量之比设为2∶1,则生产1.38吨NaNO2时,Na2CO3的理论用量为________________吨(假定Na2CO3恰好完全反应)。
-
亚硝酸钠在食品工业常用作肉类的发色剂,一种模拟工业用纯碱溶液吸收氮氧化物制备NaNO2
的实验装置如下:

已知:N2O3为酸性氧化物,2NO2+2NaOH==NaNO2+NaNO3+H2O,NO与碱不反应,NO+NO2==N2O3。回答下列问题:
(1)装置A中导管不直接插入溶液中而是连接玻璃球泡,其目的是____________;若当NO与NO2的物质的量之比为1 : 1时,A中发生反应的化学方程式为________________。
(2)装置B的作用是__________;装置C中通入O2的目的是______________。
(3)反应后A中溶液经蒸发浓缩、结晶及干燥得到产品。
①甲同学取少量的产品溶于水并用稀盐酸酸化,用湿润的KI淀粉试纸检验,试纸变蓝,得出产品为NaNO2。乙同学认为结论不可靠,其理由是________________。
②将一定量的产品溶于适量的水配成饱和溶液,再加入NH4Cl饱和溶液并加热,可观察到无色气泡逸出,该气体是空气的主要成分之一,写出有关反应的离子方程式:________________。
-
氮的氧化物处理和利用是环境科学研究的热点。
Ⅰ.碱吸法。用烧碱溶液吸收NO、NO2制备亚硝酸盐:2NaOH+NO2+NO=2NaNO2+H2O,2NO2+2NaOH= NaNO3+NaNO2+H2O。已知:298K时,Ka(HNO2)=5×10-4。
(1)298K时,NaNO2的水解常数约为______________。
Ⅱ.电解法。工业上以石墨为电极,用硝酸铵稀溶液作电解质溶液电解NO获得氮肥(在电解后溶液中通入适量氨气),其原理为8NO+7H2O+2NH3 5NH4NO3。
5NH4NO3。
(2)阴极的电极反应式为_______________。
(3)阳极区电解质溶液的pH________(填“增大”“减小”或“不变”)。
Ⅲ.化合法。亚硝酸酰氯(NOCl)是有机合成中的重要试剂,可用NO和Cl2反应得到,化学方程式为2NO(g)+Cl2(g) 2NOCl(g)。
2NOCl(g)。
(4)氮氧化物与悬浮大气中的海盐粒子相互作用会生成NOCl,涉及的相关反应有:
| 热化学方程式 | 平衡常数 |
| ① | 2NO2(g)+NaCl(s) NaNO3(s)+NOCl(g) △H1 NaNO3(s)+NOCl(g) △H1 | K1 |
| ② | 4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) △H2 2NaNO3(s)+2NO(g)+Cl2(g) △H2 | K2 |
| ③ | 2NO(g)+Cl2(g) 2NOCl(g) △H3 2NOCl(g) △H3 | K3 |
△H1、△H2、△H3之间的关系为_____________;K3=________(用含K1、K2的关系式表示)。
(5)在2L恒容容器中充入4molNO(g)和2molCl2(g),在不同温度下测得c(NOCl)与时间(t)的关系如图所示。

①T2时反应0~10min内NOCl的平均反应速率v(NOCl)=______mol·L-1·min-1。
②T2时反应的平衡常数K为__________;NO的平衡转化率α(NO)为_________。
③T2时向上述平衡体系中再加入1molNO(g)、1molCl2(g)、2molNOCl(g),则平衡______(填“向左”“向右”或“不”)移动。
(6)在密闭容器中充入NO(g)和Cl2(g),改变外界条件,Cl2的转化率变化如图所示。则该条件可能为____(填字母)。
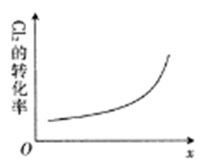
A.升高温度 B.增大压强 C.增大起始投料比 D.增大催化剂接触面
D.增大催化剂接触面
-
硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为:
2NO2 + Na2CO3 → NaNO2 + NaNO3 + CO2↑ ①
NO + NO2 + Na2CO3 → 2NaNO2 + CO2↑ ②
⑴ 根据反应①,每产生22.4L(标准状况下)CO2,吸收液质量将增加___________g。
⑵配制1000g 质量分数为21.2%的纯碱吸收液,需Na2CO3·10H2O________g。
⑶ 现有1000g 质量分数为21.2%的纯碱吸收液,吸收硝酸工业尾气,每产生22.4L(标准状况下)CO2时,吸收液质量就增加44g。
①吸收液中NaNO2 和NaNO3 的物质的量之比________
② 1000g 质量分数为21.2%的纯碱在20℃经充分吸收硝酸工业尾气后,蒸发掉688g水,冷却到0℃,最多可析出NaNO2________克(0℃时,NaNO2的溶解度为71.2g/100g水)
-
大量排放氮的氧化物会产生酸雨、光化学烟雾等环境问题。工业上处理氮的氧化物途径有多种:
Ⅰ.碱吸祛。利用纯碱溶液吸收NO、NO2,发生的反应有:
2NO2+Na2CO3=NaNO3+NaNO2+CO2,NO+NO2+Na2CO3=2NaNO2+CO2
用一定量纯碱溶被吸收NO、NO2恰好完全反应得到吸收溶液。
(1)向吸收溶液中滴加酸性高锰酸钾溶液,溶液褪色,氧化产物为NO3-,写出离子方程式__________
Ⅱ.天然气还原法。
CH4催化还原NO、NO2的热化学方程式如下:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574k]/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160kJ/mol
(2)4NO(g)=N2(g)+2NO2(g) ΔH=_________
(3)上述物质NaNO2、NO、CO2中含有共同的化学键的类型是_______
Ⅲ.活性炭还原法。
在VL恒容密闭容器中加入足量的活性炭和一定量NO,恒温(T1)条件下发生反应生成Q、P(均为无污染物质)。测得物质的量与时间关系如表所示:
| n/mol t/min | NO | Q | P |
| 0 | 0.200 | 0 | 0 |
| 10 | 0.116 | 0.042 | 0.042 |
| 20 | 0.080 | 0.060 | 0.060 |
| 30 | 0.080 | 0.060 | 0.060 |
(4)在T1温度下,NO的平衡转化率为_______;平衡常数K为_________(用分数表示)。
(5)30min后,将温度升高至T2达到平衡时,容器中NO、Q、P的浓度之比为3:1:1,则该反应的正反应ΔH_____0(填“>”“<”或“=”)。在T2温度达到平衡之后,再向容器中充入少量NO,则NO的平衡转化率将_____________“变大”“不变”“变小”)。
-
某实验小组设计如下流程,模拟将汽车尾气中的氮氧化物(主要为NO和NO2的混合物)转化为工业用盐亚硝酸钠(NaNO2),并对亚硝酸钠进行多角度探究:
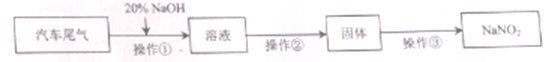
已知:NO2+NO+2NaOH=2NaNO2+H2O
2NO2+2NaOH=NaNO2+NaNO3+H2O
2NaNO3 2NaNO2+O2↑
2NaNO2+O2↑
Ⅰ.(1)配制20%NaOH溶液,除烧杯、玻璃棒外,还需要的玻璃仪器有___________(填仪器名称)。
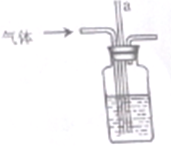
(2)操作中,实验小组同学将气体通入盛有NaOH溶液的烧杯,部分同学认为存在缺陷,改用下图装置,玻璃管a的作用是__________________。
(3)操作③中会用到下列____________仪器(填序号),

Ⅱ.NaNO2的性质
(4)设计一个实验验证酸性条件下NaNO2具有氧化性。____________________________。
供选用的试剂:NaNO2溶液、FeSO4溶液、KI溶液、稀硫酸、淀粉溶液、KSCN溶液。
(5)酸性条件下NaNO2也具有还原性。取1.50g样品,配成100mL溶液。分别取出25.00mL,用0.1000mol·L-1KMnO4酸性标准溶液滴定三次,测得平均消耗20.00mL KMnO4溶液。写出该反应的离子方程式____________________。滴定终点时的现象是______________________。NaNO2的纯度为_____________。
-
工业废气中氮氧化物是主要的大气污染源之一,已知:
2NO2+2NaOH====NaNO3+NaNO2+H2O
NO2+NO+2NaOH====2NaNO2+H2O
现有amol NO2和bmol NO的混合气体,若用足量的NaOH溶液将其完全吸收,则a和b必须满足的关系是
A.a=3b B.a=b
C.a≥b D.任意比例









