-
(本题共15分)
有4种质量比可能相同或不同的镁铝合金样品①、②、③、④。甲、乙、丙、丁4位同学各取1种样品,进行下列实验,测定合金中镁的质量分数。
52.甲同学取样品①m1 g和过量的氢氧化钠溶液反应,然后过滤;再往滤液中通入过量的二氧化碳气体,将所得沉淀过滤、洗涤、烘干、灼烧,得到固体质量仍为m1 g。则样品①合金中镁的质量分数为_____________。
53.乙同学取样品②m2 g和足量的盐酸反应,然后滴加过量的氢氧化钠溶液,将沉淀过滤、洗涤、烘干、灼烧,得到固体质量仍为m2 g。则样品②合金中镁的质量分数为____________。
54.丙同学取样品③m3 g和足量的稀硫酸反应,发现固体完全溶解,标准状况下得到气体体积为V L,则样品③中m3的取值范围是___________________________________________。
丁同学取不同质量的样品④分别和30 mL同浓度的盐酸反应,所取合金质量与产生气体体积(已转化为标准状况)如下:
实验序号
a
b
c
合金质量/mg
510
765
918
气体体积/mL
560
672
672
55.通过计算求该盐酸的物质的量浓度。
56.通过计算求样品④中合金中镁的质量分数。
57.在c组实验后,还需向容器中加入1.0 mol·L-1的氢氧化钠溶液多少毫升才能使剩余合金中的铝恰好完全溶解?
高三化学计算题中等难度题查看答案及解析
-
有三种镁铝合金样品(组分比例不一定相同)①、②、③。小奉、小贤、小红三同学各取一种样品,对合金中镁的质量分数进行下列实验探究:
(1)小奉取样品①m1 g和过量的氢氧化钠溶液反应,然后过滤;再往滤液中通入过量的二氧化碳气体,将所得沉淀过滤、洗涤、烘干、灼烧,得到固体质量仍为m1 g。则合金中镁的质量分数为___________。(保留小数点后面2位)
(2)小贤取样品②m2 g和足量的稀硫酸反应,发现固体完全溶解,标准状况下得到气体体积为VL,则m2的取值范围是_________。(结果转化为最简分数)
(3)小红取不同质量的样品③分别和30 mL同浓度的盐酸反应,所取合金质量与产生气体的体积(标准状况下测定)如下所示:
实验序号
a
b
c
合金质量(g)
0.51
0.765
0.918
气体体积(mL)
560
672
672
求:I.盐酸的物质的量浓度_______
II.合金中镁的质量分数_______
III.要使c组实验后剩余合金中的铝恰好完全溶解,还需向容器中加入1.0 mol/L的氢氧化钠溶液多少mL_______?
高三化学计算题中等难度题查看答案及解析
-
某同学取不同质量的镁铝合金样品分别与30 mL同浓度的盐酸反应,所取合金质量与产生气体体积(已转化为标准状况)如下:
实验序号
a
b
c
合金质量/mg
510
765
918
气体体积/mL
560
672
672
通过计算求:
(1)该盐酸的物质的量浓度。
(2)合金中镁的质量分数。
(3)在c组实验后,还需向容器中加入多少毫升同浓度的盐酸才能使剩余合金恰好完全溶解?
高三化学计算题困难题查看答案及解析
-
(8分)标准状况下,进行甲、乙、丙三组实验,各取30.0 mL相同浓度的盐酸,然后分别慢慢地加入不同质量的同一种镁铝合金粉末,得下列有关数据(假设反应前后溶液的体积不发生变化):
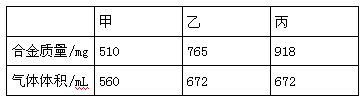
根据实验数据,计算:
(1)盐酸中HCl的物质的量浓度为_____________。
(2)合金中镁的质量分数(计算结果保留至0.1%,有必要的计算步骤和语言叙述,只写答案不得分,下同)。
(3)甲组实验后,还需向容器中加入lmol·L-1的NaOH溶液多少毫升恰好使铝元素以[Al(OH)4]-存在,并使Mg2+刚好沉淀完全?
高三化学填空题中等难度题查看答案及解析
-
为测定某镁铝合金样品中铝的含量,进行下列实验:取一定量合金,加人1OOmLO.3mol • L1稀硫酸,合金完全溶解,产生的气体在标况下为560mL;再加人
NaOH溶液至沉淀质量不再变化,用去350mLNaOH溶液。则所取样品中铝的物质的量为 ( )
A. 0. 005 mol B 0. Olmol C. 0.025mol D. 0. 03 mol
高三化学选择题中等难度题查看答案及解析
-
为测某镁铝合金样品中铝的含量,进行下列实验:取一定量合金,加入100mL0.3mol·L—1稀硫酸,合金完全溶解,产生的气体在标准状况下体积为560mL;再加0.2mol·L—1NaOH溶液至沉淀质量恰好在此时不再变化,用去350mL NaOH溶液。则所取样品中铝的物质的量为
A.0.005mol B.0.01mol C.0.025mol D.0.03mol
高三化学选择题中等难度题查看答案及解析
-
为测定某镁铝合金样品中铝的含量,进行下列实验:取一定量合金,加入100mL0.3mol·L-1稀硫酸,合金完全溶解,产生的气体在标况下为.560mL;再加入0.2mol·L-1NaOH溶液至沉淀质量不再变化,用去350mLNaOH溶液。则所取样品中铝的物质的量为
A.0.005 mol B.0.01mol C.0.025mol D.0.03 mol
高三化学选择题简单题查看答案及解析
-
为测定某镁铝合金样品中铝的含量,某同学进行了如下实验:取一定量合金,加入100 mL 0.3 mol•L-1稀硫酸,合金完全溶解,产生的气体在标准状况下的体积为560 mL;再加入0.2 mol·L-1 NaOH溶液至沉淀质量恰好不再变化,用去350 mL NaOH溶液。则所取样品中铝的物质的量为( )
A. 0.005 mol B. 0.01 mol C. 0.02 mol D. 0.03 mol
高三化学单选题中等难度题查看答案及解析
-
为测定镁铝合金(不含其它元素)中铝的质量分数,甲乙两个学习小组设计了下列二种不同的实验方案进行探究。请回答下列问题:(15分)
(一)甲组:实验方案:镁铝合金
测定剩余固体质量
实验步骤:
①称量:托盘天平称量2.7g镁铝合金粉末
②溶【解析】
将①中药品加入烧杯中,用量筒量取至少 mL 1mol/L NaOH 溶液加入烧杯中,不断搅拌,充分反应③过滤:
④洗涤:若未对过滤所得固体进行洗涤,测得铝的质量分数将 (填“偏高”、“偏低”或“不变”),证明固体已洗涤干净的方法为
⑤干燥、称量剩余固体
(二)乙组:

实验装置如图,实验步骤如下:

①按图连接好装置
②称取两份质量均为0.3g 的镁铝合金样品粉末,分别放入A装置左右两个管中,向B装置中加入一定量的水,把装置A.B的胶塞塞好,然后调节C的高度使B和C中的液面相平,记录下此时的体积为112 mL
③通过注射器的针头向装置A左侧管中注入足量的稀盐酸,等不再有气泡产生时,调节装置C的高度,使B和C中的液面相平时记录下此时的体积为448mL
④通过另一针头向装置A右侧管中加入足量的稀NaOH溶液,等不再有气泡产生时,调节装置C的高度,使B和C中的液面相平时记录下此时的体积为672mL。
问题和讨论:
(1)上述实验步骤①和②之间必须加一步 的操作,具体方法为 。
(2)为使气体体积测定结果不至于引起很大偏差,除了应注意使B和C中的液面相平外,在反应完全后至读数之前,还需要注意的关键问题是(有几点写几点) 。
(3)计算合金中铝的质量分数时,是否需要将气体体积折算为标准状况的体积 ,试根据题中数据计算出合金中铝的质量分数为 。
高三化学实验题极难题查看答案及解析
-
为测定镁铝合金(不含其它元素)中铝的质量分数,甲乙两个学习小组设计了下列二种不同的实验方案进行探究。请回答下列问题:
(一)甲组:实验方案:镁铝合金
 测定剩余固体质量
测定剩余固体质量实验步骤:
①称量:托盘天平称量2.7g镁铝合金粉末
②溶【解析】
将①中药品加入烧杯中,用量筒量取至少_____mL 1mol/L NaOH 溶液加入烧杯中,不断搅拌,充分反应③过滤:
④洗涤:若未对过滤所得固体进行洗涤,测得铝的质量分数将_____(填“偏高”、“偏低”或“不变”),证明固体已洗涤干净的方法为_________________________
⑤干燥、称量剩余固体
(二)乙组:

实验装置如图,实验步骤如下:

①按图连接好装置;
②称取两份质量均为0.3g 的镁铝合金样品粉末,分别放入A装置左右两个管中,向B装置中加入一定量的水,把装置A、B的胶塞塞好,然后调节C的高度使B和C中的液面相平,记录下此时的体积为112 mL;
③通过注射器的针头向装置A左侧管中注入足量的稀盐酸,等不再有气泡产生时,调节装置C的高度,使B和C中的液面相平时记录下此时的体积为448mL;
④通过另一针头向装置A右侧管中加入足量的稀NaOH溶液,等不再有气泡产生时,调节装置C的高度,使B和C中的液面相平时记录下此时的体积为672mL。
问题和讨论:
(1)上述实验步骤①和②之间必须加一步________的操作,具体方法为________________________。
(2)为使气体体积测定结果不至于引起很大偏差,除了应注意使B和C中的液面相平外,在反应完全后至读数之前,还需要注意的关键问题是(有几点写几点)_______。
(3)计算合金中铝的质量分数时,是否需要将气体体积折算为标准状况的体积____,试根据题中数据计算出合金中铝的质量分数为______。
高三化学实验题中等难度题查看答案及解析