-
硫酸亚铁晶体(FeSO4•7H2O)在医药上作补血剂。工业上由废铁生产FeSO4•7H2O的一种流程如图:
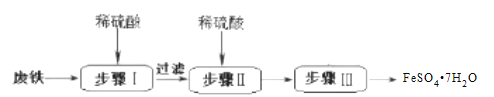
(1)步骤Ⅰ的操作前往往需要热碱溶液冲洗,其目的是_____。
(2)步骤Ⅰ加入稀硫酸的量不能过量的原因是_____。步骤Ⅱ加入稀硫酸的目的是_____。
(3)步骤Ⅲ从硫酸亚铁溶液中获得碱酸亚铁晶体(FeSO4•7H2O) 的实验操作为_____、_____、_____。烘干操作需在低温条件下进行,原因是_____。
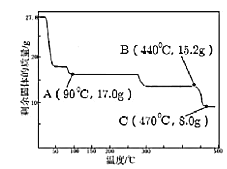
(4)取27.8g FeSO4•7H2O加热至不同温度,剩余固体的质量变化如上图所示。分析数据,90℃残留物的化学式是_____。440℃~470℃时固体物质发生反应的化学方程式是_____,做出这一判断的依据是_____。
-
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。为测定补血剂中铁元素的含量,某化学兴趣小组设计了如下实验方案,操作流程如下:
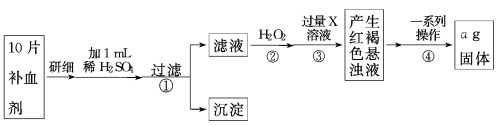
(1)写出步骤②中H2O2氧化Fe2+ 的离子方程式 。步骤②中除用H2O2外还可以使用的物质是 ;若步骤③中X溶液是氨水,写出该反应的离子方程式 。
(2)步骤④一系列操作依次是:过滤、洗涤、 、冷却、称量。
(3)假设实验无损耗,则每片补血剂含铁元素的质量 g(用含a的代数式表示)。
-
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
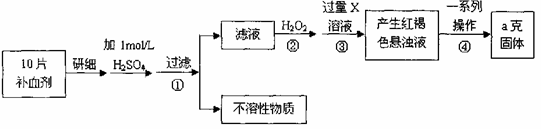
请回答下列问题:
(1)步骤②加入过量H2O2的目的:
(2)步骤③中反应的离子方程式:
(3)步骤④中一系列处理的操作步骤:过滤、________、灼烧、________、称量。
(4)若实验无损耗,则每片补血剂含铁元素的质量________ g(用含a的代数式表示,不用化简)。
(5)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5Fe2+ + MnO4— + 8H+ = 5Fe3+ + Mn2+ + 4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需
要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需__________________。
②上述实验中的KMnO4溶液需要酸化,用于酸化的酸是____________。
a.稀硝酸 b.稀硫酸 c.稀盐酸 d.浓硝酸
-
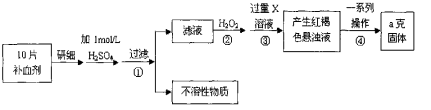
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
请回答下列问题:
(1) 步骤①滤液中滴加KSCN溶液后滤液变为红色,则该溶液中含有 (填离子符号),检验滤液中还存在Fe2+的方法为 (注明试剂、现象)。
(2) 步骤②加入过量H2O2的目的是 。
(3) 步骤③中反应的离子方程式为 。
(4) 步骤④中一系列处理的操作步骤包括:过滤、 、灼烧、 、称量。
(5) 若实验无损耗,则每片补血剂含铁元素的质量为 g。
-
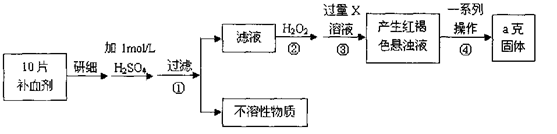
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
请回答下列问题:
(1)步骤①滤液中滴加KSCN溶液后滤液变为红色,则该溶液中含有________(填离子符号),检验滤液中还存在Fe2+的方法为________
________(注明试剂、现象)。
(2)步骤②加入过量H2O2的目的是。
(3)步骤③中反应的离子方程式为________。
(4)步骤④中一系列处理的操作步骤包括:过滤、、灼烧、、称量。
(5)若实验无损耗,则每片补血剂含铁元素的质量为________g。
-
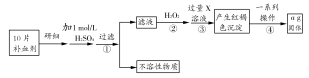
硫酸亚铁晶体(FeSO4·7H2O)在医药上可作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
请回答下列问题:
(1)步骤②加入过量H2O2的目的是 。
(2)步骤③中反应的离子方程式为 。
(3)步骤④中的一系列操作依次为:过滤、 、灼烧、 、称量。
(4)若实验无损耗,则每片补血剂含铁元素的质量为 g(用含a的代数式表示,不用化简)。
(5)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。反应原理为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需要的玻璃仪器为 ;
②上述实验中的KMnO4溶液需要酸化,可用于酸化的酸是 。
a.稀硝酸 b.稀硫酸 c.稀盐酸 d.浓硝酸
-
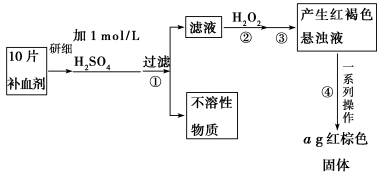
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中
铁元素的含量。实验步骤如下:
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是:取样,先滴加KSCN溶液,再滴加________,该过程的现象为________。
(2)步骤②加入过量H2O2的目的是:______________________________________。
(3)步骤③中反应的离子方程式是:_______________________________________。
(4)步骤④中一系列处理的操作步骤:过滤、________、灼烧、________、称量。
(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为________g。
-
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如下:
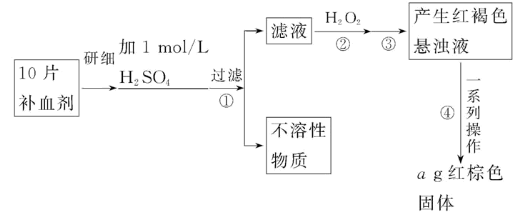
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是:取样,先滴加KSCN溶液,再滴加_______,该过程的现象为:__________________________________________。
(2)步骤②加入过量H2O2的目的是:____________________________________。
(3)步骤③中反应的离子方程式是:_____________________________________。
(4)步骤④中一系列处理的操作步骤:过滤、_______、灼烧、_______、称量。
(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为_______g。
-
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如下:
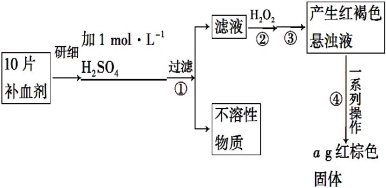
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是:取样,先滴加KSCN溶液,再滴加 ,该过程的现象为______________________。
(2)步骤②加入过量H2O2的目的是 _______________________。
(3)步骤④中反应的化学方程式是 _______________________。
(4)步骤④中一系列处理的操作步骤:过滤、________、灼烧、 、称量。
-
硫酸亚铁晶体(FeSO4·7H2O)是医药上补血剂的有效成分。某课外小组测定该补血剂中铁元素含量的流程如下(已知其它成分在测定过程中不参与反应),回答下列问题。
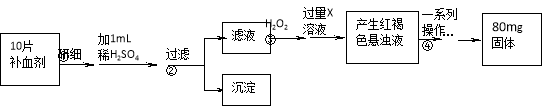
(1)写出铁原子的原子结构示意图 。
(2)步骤①研细的目的是 。
(3)证明步骤②滤液中含有Fe2+的方法是 。
(4)步骤③加入H2O2的目的是 ,发生反应的离子方程式是 。
(5)步骤④中一系列操作依次是 、洗涤、 、冷却、称量。
(6)假设实验无损耗,正常人每天应补充16.8mg左右的铁,如果全部通过服用上述测定的补血剂片来补充,则正常人每天需服用上述补血剂 片。










