-
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”,进行了如下实验:2KMnO4+5H2C2O4 +3H2SO4 =2MnSO4 +K2SO4 +10CO2↑ +8H2O
编号
0.01mol•L-1
酸性KMnO4溶液
0.1mol•L-1
H2C2O4溶液
水
某种物质
反应温度/℃
反应时间
(min)
Ⅰ
2mL
2mL
0
0
20
2.1
Ⅱ
V1mL
2mL
1mL
0
20
5.5
Ⅲ
V2 mL
2mL
0
0
50
0.5
Ⅳ
2mL
2mL
0
少量
20
0.2
请回答:
(1)实验计时方法是从溶液混合开始记时,至____时记时结束;
(2)V1=___,V2=___;设计实验Ⅰ、Ⅲ的目的是______;
(3)利用实验Ⅲ中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)=___;
(4)有同学在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。某同学认为是放热导致溶液温度升高所致,重做Ⅰ号实验,测定过程中溶液不同时间的温度,结果温度没有明显变化。由此你得出的结论是:
①____不是反应速率突然加快的原因;
②可能是反应产物有催化作用。Ⅳ号实验是为验证你的猜测,实验中要加入的少量某种物质是____(填化学式)
高一化学实验题中等难度题查看答案及解析
-
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”,进行了如下实验:2KMnO4 + 5H2C2O4 +3H2SO4 =2MnSO4 + K2SO4 +10CO2↑ +8H2O
编号
0.01mol•L—1
酸性KMnO4溶液
0.1mol•L—1
H2C2O4溶液
水
某种物质
反应温度/℃
反应时间(min)
Ⅰ
2mL
2mL
0
0
20
2.1
Ⅱ
V1mL
2mL
1mL
0
20
5.5
Ⅲ
V2 mL
2mL
0
0
50
0.5
Ⅳ
2mL
2mL
0
少量
20
0.2
请回答:
(1)实验计时方法是从溶液混合开始记时,至____________时记时结束;
(2)V1=_____,V2=_____;设计实验Ⅰ、Ⅲ的目的是__________________;
(3)利用实验Ⅲ中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)=____;
(4)有同学在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。某同学认为是放热导致溶液温度升高所致,重做Ⅰ号实验,测定过程中溶液不同时间的温度,结果温度没有明显变化。由此你得出的结论是:
①________不是反应速率突然加快的原因;
②可能是反应产物有催化作用。Ⅳ号实验是为验证你的猜测,实验中要加入的少量某种物质是___________。
高一化学实验题中等难度题查看答案及解析
-
某小组利用H2C2O4溶液和硫酸酸化的KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性KMnO4溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:KMnO4+H2C2O4+H2SO4→K2SO4+MnSO4+CO2↑+H2O (未配平)。
0.1mol·L-1KMnO4酸性溶液的体积/mL
0. 6mol·L-1
H2C2O4溶液的体积/mL
H2O的积/mL
实验温度/℃
溶液褪色时所需时间/min
实验1
10
V1
35
25
实验2
10
10
30
25
实验3
10
10
V2
50
(1)表中V1=___________mL , V2=___________mL。
(2)探究温度对化学反应速率影响的实验编号是________(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是____________。
(3)实验①测得KMnO4溶液的褪色时间为2 min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=________________。
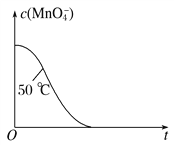
(4)已知50 ℃时c(MnO
)~反应时间t的变化曲线如图。若保持其他条件不变,请在坐标图中,画出25 ℃时c(MnO
)~t的变化曲线示意图________。
高一化学综合题困难题查看答案及解析
-
某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下,下列说法错误的是( )
实验
序号
实验温度T/K
参加反应的物质
溶液颜色褪至无色时所需时间t/s
KMnO4溶液(含硫酸)
H2C2O4溶液
H2O
V/mL
c/mol·L-1
V/mL
c/mol·L-1
V/mL
A
293
4
0.02
6
0.1
0
6
B
293
4
0.02
4
0.1
V1
8
C
T1
4
0.02
6
0.1
0
5
A.时间t的意义是,从溶液混合到KMnO4颜色褪去的时间
B.实验C中5s内平均反应速率v(KMnO4)=1.6×10-3mol•L-1•s-1
C.实验A和B是探究H2C2O4浓度对反应速率的影响,则V1=0
D.实验A和C是探究温度对反应速率的影响,则T1>293
高一化学单选题中等难度题查看答案及解析
-
某研究性学习小组的同学为了探究影响化学反应速率的外界条件,选择酸性KMnO4溶液和H2C2O4溶液的反应为研究对象。
已知①2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O;
②该反应的催化剂是Mn2+。
同学们设计的方案见下表。
C(KMnO4)/mol·L-1
V(KMnO4溶液)/mL
V(H2C2O4溶液)/mL
C(H2C2O4溶液)/mol·L-1
温度/℃
催化剂(MnSO4)
实验A
0.05
2
4
0.2
室温
无
实验B
0.05
2
4
0.1
室温
无
实验C
0.05
2
4
0.1
热水
无
实验D
0.05
2
4
0.1
室温
有
(1)选择KMnO4和H2C2O4溶液的反应为研究对象,理由是__________,该反应中还原剂为__________,表现氧化性的物质是__________,每消耗1molKMnO4转移电子的物质的量为____________________。
(2)研究某一因素 影响时要设计对比实验,本实验中的对比实验是__________(填字母)。
(3)为探究温度对反应速率的影响,应选择实验__________(填字母)。
(4)实验中同学们发现实验A和实验B中酸性KMnO4溶液紫色消失先慢后快,请你推测导致该现象可能的原因______________________________。
高一化学简答题困难题查看答案及解析
-
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过褪色所需时间来判断反应的快慢。该小组设计了如下方案:
实验编号
H2C2O4溶液
酸性KMnO4
温度
浓度(mol/L)
体积(mL)
浓度(mol/L)
体积(mL)
0.10
2.0
0.010
4.0
25
0.20
2.0
0.010
4.0
25
0.20
2.0
0.010
4.0
50
(1)已知反应后H2C2O4转化为CO2逸出,KMnO4转化为MnSO4,为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为n(H2C2O4):n(KMnO4)≥__。
(2)试验编号②和③探究的内容是____。
(3)实验①测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时同内平均反应速率v(KMnO4)=___mol·L-1·min-1。
高一化学实验题中等难度题查看答案及解析
-
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案。
编号
H2C2O4溶液
酸性KMnO4溶液
浓度/mol·L-1
体积/mL
浓度/mol·L-1
体积/mL
温度℃
①
0.10
2.0
0.010
4.0
20
②
0.20
2.0
0.010
4.0
20
③
0.20
2.0
0.010
4.0
40
(1)写出该反应的化学方程式 。
(2)
探究温度对化学反应速率影响的实验编号是________(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是____________。
(3)实验①测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=_____________mol·L-1·min-1。
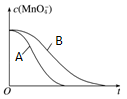
(4) 若保持其他条件不变,下图两条曲线分别表示20℃和40℃时c(MnO)~反应时间t的变化曲线。40℃时c(MnO)~t的变化曲线为 。(填写A或B)
高一化学实验题困难题查看答案及解析
-
某化学实验小组用酸性 KMnO4 溶液和草酸(H2C2O4)溶液反应,研究外界条件对反应速率的影响,实验操作及现象如下:
编号
实验操作
实验现象
向一支试管中先加入 1mL 0.01 mol/L 酸性KMnO4 溶液,再加入 1 滴 3mol/L 硫酸和 9 滴蒸馏水,最后加入1mL 0.1mol/L 草酸溶液
前 10min 内溶液紫色无明显变化,后颜色逐渐变浅, 30 min 后几乎变为无色
Ⅱ
向另一支试管中先加入 1mL 0.01mol/L 酸性KMnO4 溶液,再加入 10 滴 3mol/L 硫酸,最后加入 1mL 0.1mol/L 草酸溶液
80s 内溶液紫色无明显变化,后颜色迅速变浅,约150s 后几乎变为无色
(1)将高锰酸钾与草酸反应的离子方程式补充完整__________:
□MnO
+□H2C2O4 + □ = □Mn2+ +□ +□H2O
(2)由实验 I、Ⅱ可得出的结论是_____。
(3)关于实验Ⅱ中 80s 后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的 Mn2+ 对反应有催化作用。设计实验 Ⅲ,验证猜想。
① 补全实验Ⅲ的操作:
向试管中先加入 1mL 0.01mol/L 酸性 KMnO4 溶液,_____,最后加入 1mL 0.1mol/L 草酸溶液。
②若猜想成立,应观察到的实验现象是________。
高一化学实验题简单题查看答案及解析
-
某化学小组选用酸性高锰酸钾溶液和草酸(H2C2O4)溶液,探究外界条件对化学反应速率的影响,进行了如下三组实验:[实验内容及记录]
已知:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
实验
编号
室温下,试管中所加试剂及其用量/mL
室温下溶液颜色褪至无色所需时间/min
_mol·L-1H2C2O4溶液
H2O
0.05 mol·L-1KMnO4溶液
3 mol·L-1稀硫酸
1
3.0
1.0
4.0
2.0
4.0
2
2.0
2.0
4.0
2.0
5.2
3
1.0
3.0
4.0
2.0
6.4
请回答:
(1)[实验原理]_____________(写离子方程式)。
(2)为完成实验目的,H2C2O4溶液的物质的量浓度不低于________。
(3)根据上表中的实验数据,可以得到的结论是_________。
(4)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示,但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设。并继续进行实验探究。
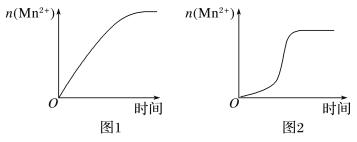
①该小组同学提出的假设是__________。
②请你帮助该小组同学完成实验方案。
实验
编号
室温下,试管中所加试剂及其用量/mL
再向试管中加入少量MnSO4
室温下溶液颜色褪至无色所需时间/min
__mol·L-1
H2C2O4溶液
H2O
0.05 mol·L-1
KMnO4溶液
3 mol·L-1
稀硫酸
4
3.0
1.0
4.0
2.0
0.1 g
t
若该小组同学提出的假设成立,应观察到的现象_____________。
高一化学实验题中等难度题查看答案及解析
-
某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.010 mol·L-1、0.0010 mol·L-1, 催化剂的用量可选择0.5 g、0 g,实验温度可选择298 K、323 K。每次实验KMnO4酸性溶液的用量均为4 mL、H2C2O4溶液(0.10 mol·L-1)的用量均为2 mL。
⑴ 请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
实验
编号
T/K
催化剂的用量 / g
酸性KMnO4溶液的浓度/mol·L-1
实验目的
①
298
0.5
0.010
a. 实验①和②探究酸性KMnO4溶液的浓度对该反应速率的影响;
b. 实验①和________探究温度对该反应速率的影响;
c. 实验①和________探究催化剂对该反应速率的影响。
②
③
④
⑵ 某同学对实验①和②分别进行了三次实验,测得以下实验数据(从混合振荡均匀开始计时):
实验编号
溶液褪色所需时间 t / min
第1次
第2次
第3次
①
14.0
13.0
11.0
②
6.0
7.0
7.0
① 实验②中用KMnO4的浓度变化来表示的平均反应速率为________(忽略混合前后溶液的体积变化)。
② 该同学分析上述数据后得出“当其他条件相同的情况下,酸性KMnO4溶液的浓度越小,所需要的时间就越短,亦即其反应速率越快”的结论,你认为是否正确________(填“是”或“否”)。他认为不用经过计算,直接根据表中褪色时间的长短就可以判断浓度大小与反应速率的关系,你认为是否可行________(填“是”或“否”),若不可行(若认为可行则不填),请设计可以直接通过观察褪色时间的长短来判断的改进方法:________。
高一化学实验题简单题查看答案及解析