-
在通风橱中进行下列实验:
| 步骤 | 
| 
|
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色 气泡后,迅速停止 | Fe、Cu接触后,其表面 均产生红棕色气泡 |
下列说法中,不正确的是( )
A.Ⅰ中气体由无色变红棕色的化学方程式为:2NO+O2=2NO2
B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否持续被氧化
-
在通风厨中进行下列实验:下列说法不正确的是( )
| 步骤 | 
| 
|
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
| | | |
A. Ⅰ中气体由无色变为红棕色的化学方程式:2NO+O2===2NO2
B. Ⅱ中的现象说明Fe表面形成致密的氧化膜,阻止Fe进一步反应
C. 对比Ⅰ、Ⅱ中的现象,说明稀HNO3的氧化性强于浓HNO3
D. 针对Ⅲ中的现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
-
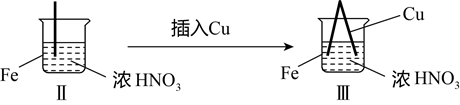
在通风橱中进行下列实验:
| 步骤 | 
| 
|
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
| | | |
下列说法不正确的是( )
A. Ⅰ中气体由无色变红棕色的化学方程式为:2NO+O2=NO2
B. Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C. 对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D. 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
-
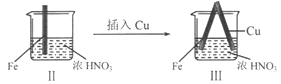
在通风橱中进行下列实验:
| 步骤 | 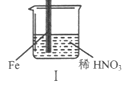
| 
|
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
下列说法不正确的是
A.I中气体由无色变红棕色的化学方程式:2NO+O2=2NO2
B.II中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比I、II中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
-
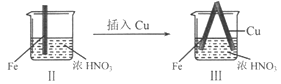
在通风橱中进行下列实验:
| 步骤 | 
| 
|
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
下列说法不正确的是
A.I中气体由无色变红棕色的化学方程式:2NO+O2=2NO2
B.II中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比I、II中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
-
在通风橱中进行的关于铁的性质的下列实验:
步骤 

现象依次为ⅠFe表面产生大量无色气泡,液面上方变为红棕色
ⅡFe表面产生少量红棕色气泡后,迅速停止
ⅢFe、Cu接触后,其表面均产生红棕色气泡
下列说法中不正确的是( )
A.Ⅰ中气体由无色变红棕色的化学方程式为:2NO+O2═2NO2
B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
-
在通风橱中进行下列实验:
| 实验 步骤 | 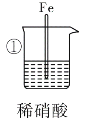
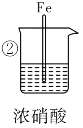
| 
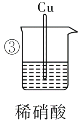
| 
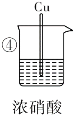
| 
|
| 现象 | Fe表面产生大量 无色气体,在液面 上方变红棕色 | Fe表面无明 显变化 | 常温下有无色气泡,加热后,Cu表面产生无色气体,在液面上方变红棕色 | Cu表面产生红 棕色气体 |
请回答下列问题:
(1)①中气体由无色变为红棕色,红棕色气体是__________________(填分子式)。
(2)②中的现象说明Fe发生了______现象,产生的原因是________________________。
(3)对比①②中的现象,______(填“能”或“不能”)说明稀硝酸的氧化性强于浓硝酸。
(4)对比③④中的现象,说明氧化性:稀硝酸______(填“>”或“<”)浓硝酸。
(5)③中在加热时的化学反应方程式为________________________,此反应中稀硝酸除表现出氧化性外,还表现出____________。
-
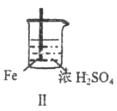
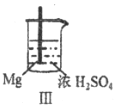
Fe和Mg与H2SO4反应的实验记录如下:
| 实验 | 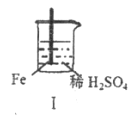
| 
| 
| 
|
| 现象 | Fe表面产生大量无色气泡 | Fe表面产生少量气泡后迅速停止 | Mg表面迅速产生大量气泡 | Fe表面有大量气泡,Mg表面有少量气泡 |
关于上述实验说法不合理的是
A. Ⅰ中产生气体的原因是:Fe+2H+=Fe2++H2↑
B. 取出Ⅱ中的铁棒放入CuSO4溶液立即析出亮红色固体
C. Ⅲ中现象说明Mg在浓H2SO4中没被钝化
D. Ⅳ中现象说明Mg的金属性比Fe强
-
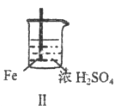
Fe和Mg与H2SO4反应的实验记录如下:
| 实验 | 
| 
| 
| 
|
| 现象 | Fe表面产生大量无色气泡 | Fe表面产生少量气泡后迅速停止 | Mg表面迅速产生大量气泡 | Fe表面有大量气泡,Mg表面有少量气泡 |
关于上述实验说法不合理的是
A. Ⅰ中产生气体的原因是:Fe+2H+=Fe2++H2↑
B. 取出Ⅱ中的铁棒放入CuSO4溶液立即析出亮红色固体
C. Ⅲ中现象说明Mg在浓H2SO4中没被钝化
D. Ⅳ中现象说明Mg的金属性比Fe强
-
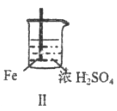
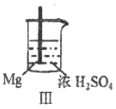
Fe和Mg与H2SO4反应的实验记录如下:
| 实验 | 
| 
| 
| 
|
| 现象 | Fe表面产生大量无色气泡 | Fe表面产生少量气泡后迅速停止 | Mg表面迅速产生大量气泡 | Fe表面有大量气泡,Mg表面有少量气泡 |
关于上述实验说法不合理的是
A. Ⅰ中产生气体的原因是:Fe+2H+=Fe2++H2↑
B. 取出Ⅱ中的铁棒放入CuSO4溶液立即析出亮红色固体
C. Ⅲ中现象说明Mg在浓H2SO4中没被钝化
D. Ⅳ中现象说明Mg的金属性比Fe强



























