-
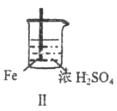
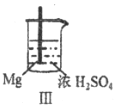
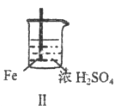
Fe和Mg与H2SO4反应的实验记录如下:
| 实验 | 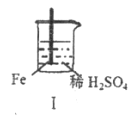
| 
| 
| 
|
| 现象 | Fe表面产生大量无色气泡 | Fe表面产生少量气泡后迅速停止 | Mg表面迅速产生大量气泡 | Fe表面有大量气泡,Mg表面有少量气泡 |
关于上述实验说法不合理的是
A. Ⅰ中产生气体的原因是:Fe+2H+=Fe2++H2↑
B. 取出Ⅱ中的铁棒放入CuSO4溶液立即析出亮红色固体
C. Ⅲ中现象说明Mg在浓H2SO4中没被钝化
D. Ⅳ中现象说明Mg的金属性比Fe强
-
Fe和Mg与H2SO4反应的实验记录如下:
| 实验 | 
| 
| 
| 
|
| 现象 | Fe表面产生大量无色气泡 | Fe表面产生少量气泡后迅速停止 | Mg表面迅速产生大量气泡 | Fe表面有大量气泡,Mg表面有少量气泡 |
关于上述实验说法不合理的是
A. Ⅰ中产生气体的原因是:Fe+2H+=Fe2++H2↑
B. 取出Ⅱ中的铁棒放入CuSO4溶液立即析出亮红色固体
C. Ⅲ中现象说明Mg在浓H2SO4中没被钝化
D. Ⅳ中现象说明Mg的金属性比Fe强
-
Fe和Mg与H2SO4反应的实验记录如下:
| 实验 | 
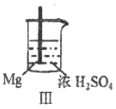
| 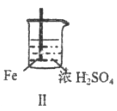
| 
| 
|
| 现象 | Fe表面产生大量无色气泡 | Fe表面产生少量气泡后迅速停止 | Mg表面迅速产生大量气泡 | Fe表面有大量气泡,Mg表面有少量气泡 |
关于上述实验说法不合理的是
A. Ⅰ中产生气体的原因是:Fe+2H+=Fe2++H2↑
B. 取出Ⅱ中的铁棒放入CuSO4溶液立即析出亮红色固体
C. Ⅲ中现象说明Mg在浓H2SO4中没被钝化
D. Ⅳ中现象说明Mg的金属性比Fe强
-
在通风橱中进行下列实验:
| 步骤 | 
| 
|
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色 气泡后,迅速停止 | Fe、Cu接触后,其表面 均产生红棕色气泡 |
下列说法中,不正确的是( )
A.Ⅰ中气体由无色变红棕色的化学方程式为:2NO+O2=2NO2
B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否持续被氧化
-
在通风厨中进行下列实验:下列说法不正确的是( )
| 步骤 | 
| 
|
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
| | | |
A. Ⅰ中气体由无色变为红棕色的化学方程式:2NO+O2===2NO2
B. Ⅱ中的现象说明Fe表面形成致密的氧化膜,阻止Fe进一步反应
C. 对比Ⅰ、Ⅱ中的现象,说明稀HNO3的氧化性强于浓HNO3
D. 针对Ⅲ中的现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
-
在通风橱中进行下列实验:
| 步骤 | 
| 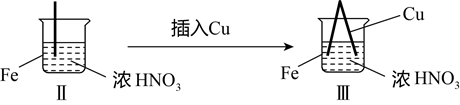
|
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
| | | |
下列说法不正确的是( )
A. Ⅰ中气体由无色变红棕色的化学方程式为:2NO+O2=NO2
B. Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C. 对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D. 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
-
在通风橱中进行下列实验:
| 步骤 | 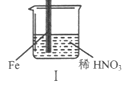
| 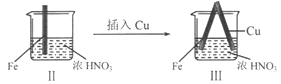
|
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
下列说法不正确的是
A.I中气体由无色变红棕色的化学方程式:2NO+O2=2NO2
B.II中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比I、II中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
-
在通风橱中进行下列实验:
| 步骤 | 
| 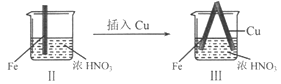
|
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
下列说法不正确的是
A.I中气体由无色变红棕色的化学方程式:2NO+O2=2NO2
B.II中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比I、II中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
-
在通风橱中进行的关于铁的性质的下列实验:
步骤 

现象依次为ⅠFe表面产生大量无色气泡,液面上方变为红棕色
ⅡFe表面产生少量红棕色气泡后,迅速停止
ⅢFe、Cu接触后,其表面均产生红棕色气泡
下列说法中不正确的是( )
A.Ⅰ中气体由无色变红棕色的化学方程式为:2NO+O2═2NO2
B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
-
某兴趣小组在研究性学习中设计了如下实验来探究Fe和H2SO4反应的过程,装置如下图所示.
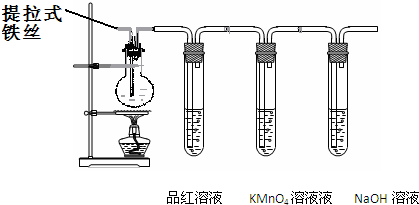
①在烧瓶中加入浓硫酸.
②将提拉式铁丝插入溶液中,观察到有少量气泡,后停止的现象.
③加热烧瓶至有大量气体产生时停止加热,品红溶液颜色褪去,烧瓶中溶液变为棕黄色.
④一段时间后KMnO4溶液颜色不再变浅,但NaOH 溶液中仍有气体放出,在导管口处可点燃此气体,烧瓶中液体变为浅绿色
根据以上实验回答:
(1)由步骤②的现象可得出的结论是:______
(2)在步骤③中,品红溶液褪色的原因是______
(3)写出步骤④中,使溶液变为浅绿色的可能的原因是(用离子方程式表示)____________
(4)若1g氢气燃烧生成液态水放出142.9KJ热量,则氢气的燃烧热的热化学方程式是:______
(5)若在反应中铁丝质量减少a克,并收集到bL可燃性气体(标准状况下假设无体积损失),则在反应过程中产生的使品红溶液褪色的气体的质量是______(用含a、b数学表达式表示)
























