-
实验室用氨气还原氧化铜的方法测定铜的近似相对原子质量,反应的化学方程式为
2NH3+3CuO N2+3Cu+3H2O,试回答:
N2+3Cu+3H2O,试回答:
(1)如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)]时,请用下列仪器设计一个简单的试验方案。
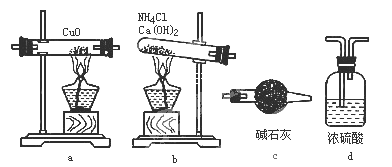
① 仪器连接的顺序(用字母编号表示,仪器可重复使用 )__________;d中浓硫酸的作用是___________,___________________;实验完毕时观察到a中的现象是_____________________;
②列出计算Cu的相对原子质量的表达式__________________;
③下列情况将使测定结果偏大的是_____________。(以下选择填空不限1个正确答案,均用字母标号填写)
A.CuO未全部还原为Cu B.CuO受潮 C.CuO中混有Cu
(2)如果仍采用上述仪器装置,其他方案可选用测定的物理量有___________。
A.m (Cu)和m(CuO) B. m (N2)和m (H2O)
C.m (Cu)和m(H2O) D.m(NH3)和m (H2O)
-
实验室用氨气还原氧化铜的方法测定铜的近似相对原子质量,反应的化学方程式为
2NH3+3CuO N2+3Cu+3H2O,试回答:
N2+3Cu+3H2O,试回答:
(1)如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)]时,请用下列仪器设计一个简单的试验方案。
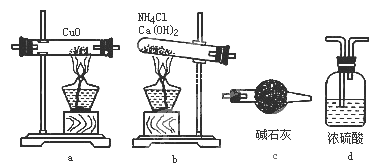
① 仪器连接的顺序(用字母编号表示,仪器可重复使用 )__________;d中浓硫酸的作用是___________,___________________;实验完毕时观察到a中的现象是_____________________;
②列出计算Cu的相对原子质量的表达式__________________;
③下列情况将使测定结果偏大的是_____________。(以下选择填空不限1个正确答案,均用字母标号填写)
A.CuO未全部还原为Cu B.CuO受潮 C.CuO中混有Cu
(2)如果仍采用上述仪器装置,其他方案可选用测定的物理量有___________。
A.m (Cu)和m(CuO) B. m (N2)和m (H2O)
C.m (Cu)和m(H2O) D.m(NH3)和m (H2O)
-
实验室用氨气还原氧化铜的方法测定铜的近似相对原子质量,反应的化学方程式为:2NH3+3CuO N2+3Cu+3H2O,试回答:
N2+3Cu+3H2O,试回答:
(1)如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)] 时,请用下图所列仪器设计一个简单的实验方案。
(2)①请写出用下图装置制备氨气的化学反应方程式___________________。
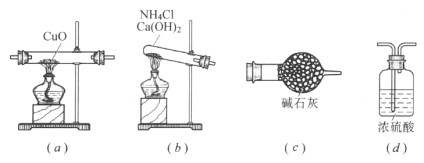
②仪器连接的顺序为(用字母编号表示,仪器可重复使用) ______________________,(d)中浓硫酸的作用是___________,实验完毕时观察到(a)中的现象是______________________。
③列出计算Cu的相对原子质量的表达式:______________________。
(2)有同学认为NH3与CuO反应生成的红色物质中可能含有Cu2O。已知Cu2O是红色粉末,在酸性溶液中,Cu+能自身发生氧化还原反应生成Cu2+和Cu。
①若CuO未完全分解,则所测定的Cu的相对原子质量会______________(偏大或偏小)。
②请设计一个简单的实验检验该红色物质中是否含有Cu2O________________。
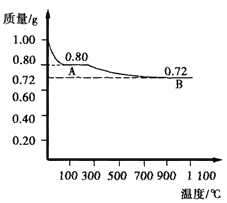
(3)在解决了问题(2)后,又有同学提出:Cu2O与CuO的热稳定性哪个更强?于是他们进行了如下实验:取0.98 g Cu(OH)2固体,加热到80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末B。如下图所示:
据此可推得A为__________,且AB段发生的反应为_________________,
由此得到的热稳定性的结论是____________________。
-
(6分)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,反应方程式为2NH3+3CuO  N2+3H2O+3Cu,用示意图中的装置制出氨气并在C中实现该反应。回答下列问题:
N2+3H2O+3Cu,用示意图中的装置制出氨气并在C中实现该反应。回答下列问题:
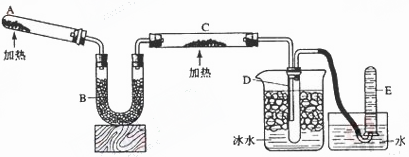
(1)A是实验室制氨气,发生反应的化学方程式是_________________
(2)实验检验氨气的方法是_______________________________ 。
(3)实验时C中反应,氨的作用是_____剂。(4)E中收集到的气体是______。
-
一定条件下氨气和氧化铜可以发生如下反应:2NH3+3CuO △ 3Cu+N2+3H2O,对此反应的分析合理的是
A.该反应属置换反应
B.NH3被氧化为N2
C.反应体现了金属铜的还原性
D.每生成1mol H2O 就伴随着1mol电子转移
-
一定条件下氨气和氧化铜可以发生如下反应:2NH3+3CuO △ 3Cu+N2+3H2O,对此反应的分析合理的是
A.该反应属置换反应
B.NH3被氧化为N2
C.反应体现了金属铜的还原性
D.每生成1mol H2O 就伴随着1mol电子转移
-
下列反应说明氨气既有还原性,又有碱性的是
A.4NH3+5O2=4NO+6H2O B.3Cl2+8NH3=N2+6NH4Cl
C.3CuO+2NH3=3Cu+ N2+3H2O D.NH3+HNO3=NH4NO3
-
一定条件下,NH3和CuO可发生反应:2NH3+3CuO=3Cu+N2+3H2O,对此反应的分析合理的是( )
A.该反应是置换反应
B.NH3被还原为N2
C.反应中氧化剂和氧化产物的物质的量之比为3:1
D.若反应中生成1moH2O,则转移电子的物质的量为lmol
-
下列反应中说明氨气具有还原性和碱性的是( )
A. 2NH3+3CuO=3Cu+N2+3H2O
B. 8NH3+3Cl3=6NH4Cl+N2
C. 4NH3+6NO 5N2+6H2O
5N2+6H2O
D. NH3+HCl=NH4Cl
-
下列反应说明氨气既有还原性,又有碱性的是( )
A.4NH3+5O2=4NO+6H2O
B.3Cl2+8NH3=N2+6NH4Cl
C.3CuO+2NH3=3Cu+N2+3H2O
D.NH3+HNO3=NH4NO3
N2+3Cu+3H2O,试回答:




