工业上电解NaHSO4溶液制备Na2S2O8(过二硫酸钠)。电解时,阴极材料为Pb;阳极(铂电极)电极反应式为2-2e-=
+2H+。下列说法正确的是
A.Na2S2O8水溶液呈弱碱性
B.Na2S2O8可水解生成H2O2,同时生成NaHSO4可循环利用
C.H2S2O8可完全电离,故稳定性与硫酸相当
D.Na2S2O8具有强氧化性,故不能使酸性高锰酸钾溶液褪色
高三化学单选题中等难度题
工业上电解NaHSO4溶液制备Na2S2O8(过二硫酸钠)。电解时,阴极材料为Pb;阳极(铂电极)电极反应式为2-2e-=
+2H+。下列说法正确的是
A.Na2S2O8水溶液呈弱碱性
B.Na2S2O8可水解生成H2O2,同时生成NaHSO4可循环利用
C.H2S2O8可完全电离,故稳定性与硫酸相当
D.Na2S2O8具有强氧化性,故不能使酸性高锰酸钾溶液褪色
高三化学单选题中等难度题
工业上电解NaHSO4溶液制备Na2S2O8(过二硫酸钠)。电解时,阴极材料为Pb;阳极(铂电极)电极反应式为2-2e-=
+2H+。下列说法正确的是
A.Na2S2O8水溶液呈弱碱性
B.Na2S2O8可水解生成H2O2,同时生成NaHSO4可循环利用
C.H2S2O8可完全电离,故稳定性与硫酸相当
D.Na2S2O8具有强氧化性,故不能使酸性高锰酸钾溶液褪色
高三化学单选题中等难度题查看答案及解析
工业上电解NaHSO4溶液制备Na2S2O8。电解时,阴极材料为Pb;阳极(铂电极)电极反应式为2HSO4-- 2e-=S2O82-+2H+。下列说法正确的是( )
A. 阴极电极反应式为Pb+HSO4-- 2e-=PbSO4+H+
B. 阳极反应中S的化合价升高
C. S2O82-中既存在非极性键又存在极性键
D. 可以用铜电极作阳极
高三化学单选题简单题查看答案及解析
工业上电解 NaHSO4 溶液制备 Na2S2O8(其中阴离子结构为 )。其中阴极材料为 Pb;阳极材料为铂。下列说法不正确的是
)。其中阴极材料为 Pb;阳极材料为铂。下列说法不正确的是
A.SO42-向阳极迁移
B.阳极可换为铜电极
C.阳极反应中 S 的化合价不变
D.阴极电极反应式:2H++2e-=H2↑。
高三化学单选题困难题查看答案及解析
Na2S2O8具有强氧化性,在石油行业中有重要用途,工业上可利用电解法制备它,工作原理如图(电极材料是石墨)所示,且电子由外电路流入C2,下列说法正确的是
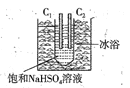
A. 阴极上的电极反应式为:2SO42--2e-=S2O82-
B. C1电极接电源负极,发生还原反应
C. 电解一段时间后,溶液的pH减小
D. 刚开始电解时,两电极上放电离子的物质的量相等
高三化学选择题中等难度题查看答案及解析
实验室模拟工业制备高纯铁。用惰性电极电解FeSO4溶液制备高纯铁的原理如图所示:
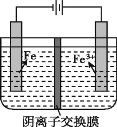
下列说法不正确的是( )
A.阴极主要发生反应:Fe2++2e-=Fe
B.向阳极附近滴加 KSCN 溶液,溶液变红
C.电解一段时间后,阴极附近pH减小
D.电解法制备高纯铁总反应:3Fe2+ Fe+2Fe3+
高三化学单选题中等难度题查看答案及解析
电解硫酸钠溶液生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为l∶2,下列有关说法正确的是( )
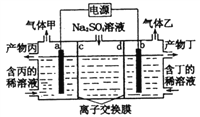
A. a电极反应式为:2H++2e-= H2↑
B. 产物丙为硫酸溶液
C. 离子交换膜d 为阴离子交换膜
D. 每转移0.1mol电子,产生1.12 L的气体乙
高三化学单选题困难题查看答案及解析
电解硫酸钠溶液生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为l∶2,下列有关说法正确的是( )
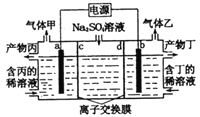
A. a电极反应式为:2H++2e-= H2↑
B. 产物丙为硫酸溶液
C. 离子交换膜d 为阴离子交换膜
D. 每转移0.1mol电子,产生1.12 L的气体乙
高三化学单选题困难题查看答案及解析
工业上联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极。 实验过程中取样测丙溶液的 pH 值,pH 试纸显红色。下列有关说法正确的是

A.a 电极的电极反应式为:2H+ + 2e- = H2↑
B.联合生产过程中需添加补充 Na2SO4
C.离子交换膜 d 为阴离子交换膜
D.每转移 0.1 mol 电子,产生 1.12 L 的气体乙
高三化学单选题中等难度题查看答案及解析
MnO2是常见的氧化剂、催化剂和活性电极材料。
(1)工业上,以惰性材料为电极,电解MnSO4溶液(含少量稀硫酸)制备MnO2。写出阳极的电极反应式:___________。
(2)已知如下热化学方程式(K代表平衡常数):
①MnCO3(s)MnO(s)+CO2(g) △H1 K1
②2MnO(s)+O2(g)2MnO2(s) △H2 K2
③2MnCO3(s)+O2(g)2MnO2(s)+2CO2(g) △H3 K3
△H3=______(用△H1、△H2表示) K3=_______(用K1、K2表示)。
(3)反应②在低温条件下能自发进行,则△H2______0(填“>”“<”或“=”)。
(4)在密闭容器中投入足量的MnCO3,—定条件下发生反应:MnCO3(s)MnO(s)+CO2(g)
△H>0。在一定温度下,达到平衡状态时p(CO2)=2a MPa。
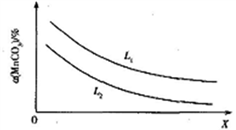
① 温度、压强对MnCO3分解率的影响如图所示:比较:L1____L2(填“>”“<”或“=”)。
② 保持温度不变,将容器体积扩大至原来的2倍,则p(CO2)的变化范围是______。
③ 保持温度不变,将容器体积压缩至原来的一半,达到新平衡时下列物理量-定不变的是__(填代号)。
A.平衡常数K B.c(CO2) C.n(CO2) D.m(MnCO3)
(5)—定温度下,在容积为2L的恒容密闭容器中加人足量的MnCO3(s)和5molO2,发生反应:2MnCO(s)+O2(g)2MnO2(s)+2CO2(g),CO2以平均速率0.1mol• L-1·min-1经过10min达到平衡状态。该条件下该反应的平衡常数K为_______。
高三化学简答题中等难度题查看答案及解析
Cu2O广泛用作颜料和化工生产的催化剂。
Ⅰ.制备Cu2O
(1)电解法:工业上用铜作阳极,钛片为阴极,电解一定浓度的NaOH 溶液可制备氧化亚铜,写出阳极的电极反应式为_____________________
(2)微乳液-还原法:在 100℃ Cu(NO3)2 的水溶液中加入一定体积的 NaOH 水溶液,并搅拌使之混合均匀, 再逐滴加入水合肼的水溶液,直至产生红色沉淀,经抽滤、洗涤和真空干燥,得到Cu2O 粉末。
已知: N2H4(l)+O2(g)=N2(g)+2H2O(l)△H= -akJ/mol
Cu(OH)2(s)=CuO(s)+H2O(l)△H= +bkJ/mol
4CuO(s)=2Cu2O(s)+O2(g)△H= +ckJ/mol
则由N2H4 和Cu(OH)2 反应制备 Cu2O 的热化学方程式为 ________________________。
Ⅱ.工业上用Cu2O 与 ZnO 组成的催化剂可用于工业上合成甲醇: CO(g)+2H2(g) CH3OH(g) △H = -90.8 kJ/mol,回答下列问题:
(1)能说明反应CO(g)+2H2(g)CH3OH(g)已达平衡状态的是(_______)
A.当反应的热效应△H = -90.8 kJ/mol 时反应达到平衡状态
B.在恒温恒压的容器中,混合气体的密度保持不变
C.在绝热恒容的容器中,反应的平衡常数不再变化
D.在恒温恒容的容器中,气体的平均摩尔质量不再变化
(2)在 T1℃时,体积为 2 L 的恒容容器中充入物质的量之和为 3mol 的 H2 和CO,当起始 n(H2)/n(CO)= 2 时,经过 5min 达到平衡,CO 的转化率为 0.6,则0~5min 内平均反应速率 v (H2)=___;该温度下的平衡常数为__________________ ;若此时再向容器中加入CO(g) 和 CH3OH(g)各 0.4mol,达新平衡时 H2 的转化率将 ______(填“增大”、 “减小”或“不变”);
(3)工业实际合成 CH3OH 生产中,采用下图M点而不是N点对应的反应条件,运用化学反应速率和化学平衡知识,同时考虑生产实际,说明选择该反应条件的理由:________。

高三化学综合题中等难度题查看答案及解析