对水样中M的分解速率的影响因素进行研究。在相同温度下,M的物质的量浓度 [c(M)]随时间(t) 变化的有关实验数据如下图所示,下列说法不正确的是( )

A.水样的PH越小,M的分解速率越快
B.水样中添加Cu2+,能加快M的分解速率
C.由②③得,反应物浓度越大,M的分解速率越快
D.在0~20min内,②中M的平均分解速率为0.015mol·L-1·min-1
高一化学单选题中等难度题
对水样中M的分解速率的影响因素进行研究。在相同温度下,M的物质的量浓度 [c(M)]随时间(t) 变化的有关实验数据如下图所示,下列说法不正确的是( )

A.水样的PH越小,M的分解速率越快
B.水样中添加Cu2+,能加快M的分解速率
C.由②③得,反应物浓度越大,M的分解速率越快
D.在0~20min内,②中M的平均分解速率为0.015mol·L-1·min-1
高一化学单选题中等难度题
对水样中M的分解速率的影响因素进行研究。在相同温度下,M的物质的量浓度 [c(M)]随时间(t) 变化的有关实验数据如下图所示,下列说法不正确的是( )

A.水样的PH越小,M的分解速率越快
B.水样中添加Cu2+,能加快M的分解速率
C.由②③得,反应物浓度越大,M的分解速率越快
D.在0~20min内,②中M的平均分解速率为0.015mol·L-1·min-1
高一化学单选题中等难度题查看答案及解析
对水样中溶质M的分解速率影响因素进行研究。在相同温度下,M的物质的量浓度(mol·L-1)随时间(min)变化的有关实验数据见下表。
| 时间 水样 | 0 | 5 | 10 | 15 | 20 | 25 |
| I (pH=2) | 0.40 | 0.28 | 0.19 | 0.13 | 0.10 | 0.09 |
| II(pH=4) | 0.40 | 0.31 | 0.24 | 0.20 | 0.18 | 0.16 |
| Ⅲ(pH=4) | 0.20 | 0.15 | 0.12 | 0.09 | 0.07 | 0.05 |
| IV(pH=4,含 Cu2+) | 0.20 | 0.09 | 0.05 | 0.03 | 0.01 | 0 |
下列说法不正确的是
A. 在0~20 min内,I中M的平均分解速率为0.015mol·L-1·min-1
B. 其它条件相同时,水样酸性越强,M的分解速率越快
C. 在0~25 min内,Ⅲ中M的分解百分率比II大
D. 由于Cu2+存在,IV中M的分解速率比I快
高一化学选择题中等难度题查看答案及解析
对水样中溶质M的分解速率影响因素进行研究。在相同温度下,M的物质的量浓度(mol·L-1)随时间(min)变化的有关实验数据见下表。
| 时间 水样 | 0 | 5 | 10 | 15 | 20 | 25 |
| I (pH=2) | 0.40 | 0.28 | 0.19 | 0.13 | 0.10 | 0.09 |
| II(pH=4) | 0.40 | 0.31 | 0.24 | 0.20 | 0.18 | 0.16 |
| Ⅲ(pH=4) | 0.20 | 0.15 | 0.12 | 0.09 | 0.07 | 0.05 |
| IV(pH=4,含 Cu2+) | 0.20 | 0.09 | 0.05 | 0.03 | 0.01 | 0 |
下列说法不正确的是( )
A. 在0~20 min内,I中M的平均分解速率为0.015mol·L-1·min-1
B. 其它条件相同时,水样酸性越强,M的分解速率越快
C. 在0~25 min内,Ⅲ中M的分解百分率比II大
D. 由于Cu2+存在,IV 中M的分解速率比I快
高一化学单选题困难题查看答案及解析
对水样中溶质M的分解速率影响因素进行研究。在相同温度下,M的物质的量浓度(mol·L-1)随时间(min)变化的有关实验数据见下表。
| 时间 水样 | 0 | 5 | 10 | 15 | 20 | 25 |
| I (pH=2) | 0.40 | 0.28 | 0.19 | 0.13 | 0.10 | 0.09 |
| II(pH=4) | 0.40 | 0.31 | 0.24 | 0.20 | 0.18 | 0.16 |
| Ⅲ(pH=4) | 0.20 | 0.15 | 0.12 | 0.09 | 0.07 | 0.05 |
| IV(pH=4,含Cu2+) | 0.20 | 0.09 | 0.05 | 0.03 | 0.01 | 0 |
下列说法不正确的是( )
A.在0~20 min内,I中M的平均分解速率为0.015mol·L-1·min-1
B.其它条件相同时,水样酸性越强,M的分解速率越快
C.在0~25 min内,Ⅲ中M的分解百分率比II大
D.由于Cu2+存在,IV 中M的分解速率比I快
高一化学单选题中等难度题查看答案及解析
对水样中M的分解速率的影响因素进行研究。 在相同温度下,M的物质的量浓度[c(M)]随时间(t)的变化如下图所示。下列说法错误的是
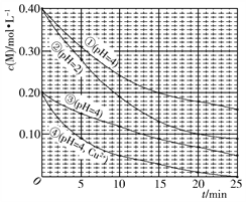
A. 水样酸性越强,M的分解速率越快
B. 水样中添加Cu2+,能加快M的分解速率
C. 由②③得,反应物浓度越大,M的分解速率越快
D. 在0~20 min内,②中M的分解速率为0.015 mol·L−1·min−1
高一化学单选题中等难度题查看答案及解析
某探究性学习小组拟通过锌与盐酸的反应研究影响反应速率的因素。
该探究性学习小组用相同质量的锌和相同浓度的足量的稀盐酸反应得到实验数据如下表所示:
| 实验编号 | 锌的状态 | 反应温度/℃ | 收集100mL氢气所需时间/s |
| Ⅰ | 薄片 | 15 | 200 |
| Ⅱ | 薄片 | 25 | 90 |
| Ⅲ | 粉末 | 25 | 10 |
(1)该实验的目的是探究 、 对锌和稀盐酸反应速率的影响;
(2)实验Ⅰ和Ⅱ表明 ,化学反应速率越大;
(3)能表明固体的表面积对反应速率有影响的实验编号是 和 ,实验结论是 ;
(4)请设计一个实验方案证明盐酸的浓度对该反应的速率的影响:
。
高一化学实验题中等难度题查看答案及解析
H2O2分解速率受多种因素影响。实验测得70℃时不同条件下H2O2浓度随时间的变化如下图所示。下列说法正确的是
A.  图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B. 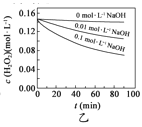 图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C.  图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快
图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快
D. 
 图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
高一化学单选题中等难度题查看答案及解析
H2O2分解速率受多种因素影响。实验测得70℃时不同条件下H2O2浓度随时间的变化如下图所示。下列说法正确的是
A. 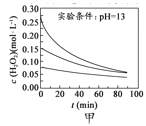 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B. 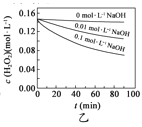 图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C.  图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快
图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快
D. 
 图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
高一化学单选题中等难度题查看答案及解析
I.为了探究化学反应速率及其影响因素,某研究小组以盐酸和碳酸钙反应进行了如下实验。实验方案与数据如下表,t表示收集a mLCO2所需的时间。
| 序号 | 反应温度/℃ | C(HCl)/ mol·L-1 | V(HCl)/ mL | 10g碳酸钙的形状 | t/min |
| 1 | 20 | 2 | 10 | 块状 | t1 |
| 2 | 20 | 2 | 10 | 粉末 | t2 |
| 3 | 20 | 4 | 10 | 粉末 | t3 |
| 4 | 40 | 2 | 10 | 粉末 | t4 |
(1)设计实验1和实验2的目的是研究 _________________对化学反应速率的影响。
(2)为研究温度对对化学反应速率的影响,可以将实验_____和实验____(填序号)作对比。
(3)将实验2和实验3作对比,可知t2___________t3(填“﹥”、“﹤”或“﹦”)。
II.在一体积为10L密闭容器中,通入一定量的CO和H2O,在 850℃时发生如下反应:
CO(g)+H2O(g) CO2(g)+H2(g),CO浓度变化如图,
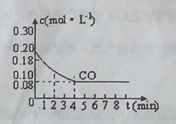
(1)则0~4 min的平均反应速率v(CO)=_____________mol·L-1·min -1。
(2)该反应达到最大限度所需的时间为____________,此时CO的转化率为_____________。
高一化学实验题中等难度题查看答案及解析
为了探究化学反应速率和化学反应限度的有关问题,某研究小组进行了以下实验:
Ⅰ.以H2O2的分解反应为研究对象,实验方案与数据记录如下表,t表示收集a mL O2所需的时间。
| 序号 | 反应 | c(H2O2)/ | V(H2O2) | m(MnO2) | t/min |
| 1 | 20 | 2 | 10 | 0 | t1 |
| 2 | 20 | 2 | 10 | 0.1 | t2 |
| 3 | 20 | 4 | 10 | 0.1 | t3 |
| 4 | 40 | 2 | 10 | 0.1 | t4 |
(1)设计实验2和实验3的目的是研究____________对化学反应速率的影响。
(2)为研究温度对化学反应速率的影响,可以将实验________和实验________作对比(填序号)。
(3)将实验1和实验2作对比,t1________t2(填“>”、“<”或“=”)。
Ⅱ.以KI和FeCl3反应为例(2Fe3++2I-2Fe2++I2)设计实验,探究此反应存在一定的限度。可选试剂:
①0.1 mol·L-1KI溶液 ②0.1 mol·L-1FeCl3溶液 ③0.1 mol·L-1FeCl2溶液 ④0.1 mol·L-1盐酸 ⑤0.1 mol·L-1KSCN溶液 ⑥CCl4
实验步骤:(1)取5 mL 0.1 mol·L-1KI溶液,再滴加几滴0.1 mol·L-1FeCl3溶液;
(2)充分反应后,将溶液分成三份;
(3)取其中一份,加试剂⑥,振荡,CCl4层显紫色,说明反应生成碘;
(4)另取一份,加试剂________(填序号),现象______________,说明此反应存在一定的限度。
Ⅲ.N2O4可分解为NO2。在100 mL密闭容器中投入0.01 mol N2O4,利用现代化学实验技术跟踪测量c(NO2)。c(NO2)随时间变化的数据记录如下图所示。
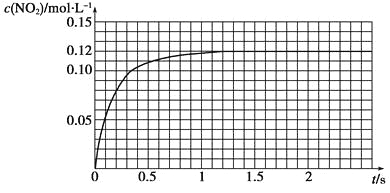
(1)反应容器中最后剩余的物质有______________,其中N2O4的物质的量为________mol。
(2)c(NO2)随时间变化的曲线表明,实验测得的化学反应速率在逐渐减小,最后________。
高一化学填空题简单题查看答案及解析