硼氢化钠(NaBH4)具有强还原性,在工业生产上广泛用于非金属及金属材料的化学镀膜、贵金属回收、工业废水处理等。工业上采用的Bayer法制备NaBH4通常分两步(如图)。下列说法错误的是
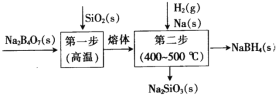
A.用B2O3代替Na2B4O7也可制得NaBH4
B.两步的总反应中氧化剂与还原剂的物质的量之比为2:1
C.将SiO2粉碎能增大得到熔体的速率
D.由图可知该工艺过程中无污染性物质产生,符合绿色化学理念
高三化学单选题中等难度题
硼氢化钠(NaBH4)具有强还原性,在工业生产上广泛用于非金属及金属材料的化学镀膜、贵金属回收、工业废水处理等。工业上采用的Bayer法制备NaBH4通常分两步(如图)。下列说法错误的是

A.用B2O3代替Na2B4O7也可制得NaBH4
B.两步的总反应中氧化剂与还原剂的物质的量之比为2:1
C.将SiO2粉碎能增大得到熔体的速率
D.由图可知该工艺过程中无污染性物质产生,符合绿色化学理念
高三化学单选题中等难度题
硼氢化钠(NaBH4)具有强还原性,在工业生产上广泛用于非金属及金属材料的化学镀膜、贵金属回收、工业废水处理等。工业上采用的Bayer法制备NaBH4通常分两步(如图)。下列说法错误的是

A.用B2O3代替Na2B4O7也可制得NaBH4
B.两步的总反应中氧化剂与还原剂的物质的量之比为2:1
C.将SiO2粉碎能增大得到熔体的速率
D.由图可知该工艺过程中无污染性物质产生,符合绿色化学理念
高三化学单选题中等难度题查看答案及解析
铜的电解实现了铜与杂质的分离,也造成了一部分资重金属进入阳极泥中,通过对阳极泥的综合处理可以回收可观的宝贵金属。稀散元素硒和碲广泛用于治金工业、 电子工业、国防工业、 医学和农业等领域,需求量越来越大。电解精炼铜的阳极泥主要成分为Cu2Se、Cu2Te和少量金属单质Au等, 工业上从其中同收碲、硒的一种工艺流程如图:

已知: TeO2是两性氧化物,Se和TeO2的物理性质如下表:
| 物理性质 | 熔点 | 沸点 | 水溶性 |
| Se | 221℃ | 685℃ | 难溶于水 |
| TeO2 | 733℃ | 1260℃ | 微溶于水 |
(1)“焙烧”时所加的硫酸浓度最好为_____(填序号)。
a.10% b.50% c.70% d.98%
(2)加硫酸焙烧过程中Cu2Se参与反应的化学方程式为_________,氧化产物和还原产物的物质的量之比是_______。
(3)滤渣的主要成分是_______ (填化学式)。
(4)“酸溶”后,将TeO2先溶于盐酸得到四氯化碲,然后再通入二氧化硫得到碲单质,后者发生反应的化学方程式为______________ 。
(5)“沉碲”时控制溶液的pH为4.5-5.0,生成TeO2沉淀。如果H2SO4过量,溶液酸度过大,将导致“沉碲”不完全,原因是______________ 。
(6)过滤所得粗硒中含有Ni、Fe、Cu等杂质,可采用真空蒸馏的方法进行提纯,获得纯硒。真空蒸馏的挥发物中硒含量与温度的关系如图所示。蒸馏操作中控制的最佳温度是_____ (填序号)
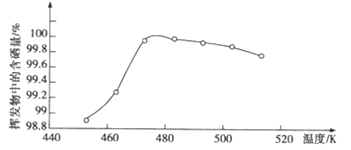
a. 455℃ b. 462℃ c.475℃ d. 515℃
(7)工业上还可以通过电解铜阳极泥碱浸,过滤后的滤液得到单质碲。己知电解时的电极均为石墨,则阴极的电极反应式为___________。
高三化学综合题困难题查看答案及解析
亚硝酸钠(有毒性,市场上很易与食盐混淆)是一种常见的工业用盐,广泛用于物质合成、金属表面处理等,物理性质与NaCl极为相似。相关化学性质如下图所示,下列说法不正确的是

A.该图示中涉及到的氧化还原反应共4个
B.NaNO2与N2 H4反应中,氧化产物与还原产物的物质的量之比为2:1
C.可用KI-淀粉试纸和食醋鉴别NaNO2和NaCl
D.分解NaN3盐每产生1 mol N2转移6 mol e-
高三化学选择题中等难度题查看答案及解析
化学与生产、生活密切相关。下列说法不正确的是
A.维生素C具有还原性,应密封保存
B.用Na2S处理工业废水中的Cu2+、Hg2+等重金属离子
C.75%的酒精能使蛋白质变性,可用于医用消毒
D.酸性洁厕灵与碱性“84消毒液”共用,可提高清洁效果
高三化学单选题简单题查看答案及解析
在有机化学工业中常用的一种钠盐是NaBH4,即硼氢化钠。它具有很强的还原性,也是一种高贮氢密度材料,是最有可能作为氢燃料电池的即时供应氢源。但它不能与水和酸共存。
⑴将其投入水中可生成偏硼酸钠(NaBO2)和氢气,写出该反应的化学方程式,反应中的还原剂是________,每摩NaBH4反应时电子转移数为________mol。
⑵若将NaBH4投入酸溶液中其反应速率与其放入水中相比,应快还是慢________,理由是。
⑶NaBH4还用于将含Au3+的碱性废液中回收黄金,其离子方程式为:
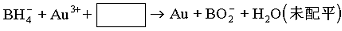
请写出配平的离子方程式。
高三化学填空题中等难度题查看答案及解析
(6分)在有机化学工业中常用的一种钠盐是NaBH4,即硼氢化钠。它具有很强的还原性,也是一种高贮氢密度材料,是最有可能作为氢燃料电池的即时供应氢源。但它不能与水和酸共存。⑴将其投入水中可生成偏硼酸钠(NaBO2)和氢气,写出该反应的化学方程式________,反应中的还原剂是________,每摩NaBH4反应时电子转移数为________mol。
⑵NaBH4还用于将含Au3+的碱性废液中回收黄金,其离子方程式为:
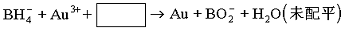
请写出配平的离子方程式。
高三化学填空题中等难度题查看答案及解析
亚硝酸钠(有毒性,市场上很易与食盐混淆)是一种常见的工业用盐,广泛用于物质合成、金属表面处理等,它的性质或用途,其物理性质与NaCl极为相似.相关化学性质如图所示,下列说法不正确的是( )
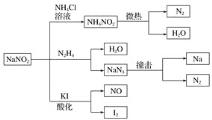
A. NaNO2稳定性大于NH4NO2 B. NaNO2与N2H4反应中,NaNO2是氧化剂
C. 可用KI淀粉和食醋鉴别NaNO2和NaCl D. 分解NaN3盐每产生1mol N2转移6mole-
高三化学单选题困难题查看答案及解析
亚硝酸钠(有毒性,市场上很易与食盐混淆)是一种常见的工业用盐,广泛用于物质合成、金属表面处理等,它的性质或用途,其物理性质与NaCl极为相似.相关化学性质如图所示,下列说法不正确的是( )

A.NaNO2稳定性大于NH4NO2 B.NaNO2与N2H4反应中,NaNO2是氧化剂
C.可用KI淀粉和食醋鉴别NaNO2和NaCl D.分解NaN3盐每产生1mol N2转移6mole-
高三化学单选题困难题查看答案及解析
亚硝酸钠(有毒性,市场上很易与食盐混淆)是一种常见的工业用盐,广泛用于物质合成、金属表面处理等,它的性质或用途,其物理性质与NaCl极为相似.相关化学性质如图所示,下列说法不正确的是( )
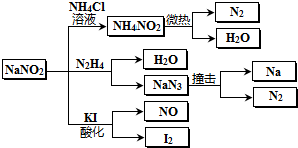
A.NaNO2稳定性大于NH4NO2
B.NaNO2与N2H4反应中,NaNO2是氧化剂
C.可用KI-淀粉和食醋鉴别NaNO2和NaCl
D.分解NaN3盐每产生1molN2 转移6mol e-
高三化学选择题简单题查看答案及解析
钠及其化合物具有广泛的用途.
(1)工业上制备金属钠的常用方法是 .试写出制备金属钠的化学方程式 .金属钠可用于 (写出Na在熔点低方面的一种用途).
(2)用Na2CO3熔融盐作电解质,CO、O2、CO2为原料可组成新型电池.该电池的结构如图所示:

①正极的电极反应式为 ,电池工作时物质A可循环使用,A物质的化学式为 .
②请写出检验Na2CO3中钠元素的方法 .
(3)常温下,浓度均为0.1mol•L﹣1的下列五种钠盐溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaCO | NaCN |
| pH | 8.8 | 9.7 | 6 | 0.3 |
上述盐溶液的阴离子中,结合H+能力最强的是 ,根据表中数据,浓度均为0.01mol•L﹣1的下列四种酸的溶液分别稀释100倍,pH变化最大的是 (填序号).
a.HCN b.HClO c.CH3COOH d.H2CO3
(4)实验室中常用NaOH来进行尾气处理、洗气和提纯.
①常温下,当300mL 1mol•L﹣1的NaOH溶液吸收4.48L(折算成标准状况)SO2时,所得溶液pH>7,则溶液中各离子浓度由大到小的顺序为 .
②已知几种离子开始沉淀时的pH如下表:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加某浓度的NaOH溶液时, (填离子符号)先沉淀,Ksp[Fe(OH)2] Ksp[Mg(OH)2](填“>”、“=”或“<”).
高三化学填空题困难题查看答案及解析