-
甲、乙两同学用下图所示装置进行实验,探究硝酸与铁反应的产物。
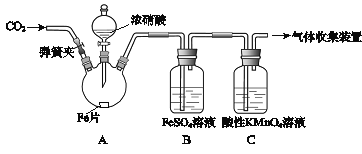
文献记载:
I.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+4、+2、﹣3价等氮的化合物。
II.FeSO4+NO⇌Fe(NO)SO4(棕色) 。
III.NO2和NO都能被KMnO4氧化吸收。
甲的实验操作和现象记录如下:
| 实验操作 | 实验现象 |
| (1)打开弹簧夹,通入一段时间某气体,关闭弹簧夹。 | |
| (2)打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞。 | 无明显现象。 |
| (3)加热烧瓶,反应开始后停止加热。 | ①A中有红棕色气体产生,一段时间后,气体颜色逐渐变浅; B中溶液变棕色; C中溶液紫色变浅。 ②反应停止后,A中有固体剩余。 |
请回答下列问题:
(1)为排除空气对实验的干扰,操作(1)中通入的气体可能是________________。
(2)滴入浓硝酸加热前没有明显现象的原因是__________________________。
(3)试写出加热烧瓶后A中有红棕色气体产生的化学方程式_______________。
(4)甲认为B中溶液变棕色是因为A中有NO生成,你认为甲的观点对吗_________(填正确或错误)?请结合方程式简述原因 ________________________________。
(5)检验是否生成﹣3价氮的化合物,应进行的实验操作是________________________。
-
某同学设计如下实验装置探究硫酸与金属、非金属的反应、验证其产物,并探究随着反应的进行,硫酸性质发生的变化。根据实验要求回答相关问题:
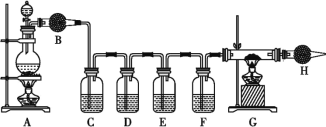
F装置用于检验二氧化碳。供选择的试剂有:只含碳的生铁、18 mol·L-1的硫酸、品红溶液、无水硫酸铜粉未、酸性高锰酸钾溶液、氧化铜、澄清的石灰水、碱石灰。(供选择的试剂可重复使用)
(1)打开分液漏斗的活塞,A装置中发生的反应6H2SO4(浓)+2Fe Fe2(SO4)3+6H2O↑+3SO2↑和(用化学方程式表示)_____,随反应的进行,硫酸的浓度变稀,又发生反应(用化学方程式表示)____
Fe2(SO4)3+6H2O↑+3SO2↑和(用化学方程式表示)_____,随反应的进行,硫酸的浓度变稀,又发生反应(用化学方程式表示)____
(2)B装置中的试剂是__________。
(3)E装置中的试剂是____________作用是______________。
(4)G装置中的试剂是__________,现象是______________。
(5)制备SO2的适宜药品为___________(填代号)。
①Na2SO3固体;②Na2SO3溶液;③20%硫酸;④70%硫酸;⑤铜片
(6)对SO2与氯水的反应进行探究。用注射器吸入一定量的饱和氯水和SO2,振荡,静置,再吸入少量品红溶液,发现品红溶液不褪色,用化学反应方程式解释其原因____________
-
(共14分)某同学设计如下实验装置探究硫酸与金属、非金属的反应、验证其产物,并探究随着反应的进行,硫酸性质发生的变化。根据实验要求回答相关问题:
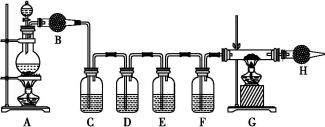
F装置用于检验二氧化碳。供选择的试剂有:只含碳的生铁、18 mol·L-1的硫酸、品红溶液、无水硫酸铜粉未、酸性高锰酸钾溶液、氧化铜、澄清的石灰水、碱石灰。(供选择的试剂可重复使用)
(1)打开分液漏斗的活塞,A装置中发生的反应6H2SO4(浓)+2Fe Fe2(SO4)3+6H2O↑+3SO2↑和 (用化学方程式表示),随反应的进行,硫酸的浓度变稀,又发生反应 (用化学方程式表示)。
Fe2(SO4)3+6H2O↑+3SO2↑和 (用化学方程式表示),随反应的进行,硫酸的浓度变稀,又发生反应 (用化学方程式表示)。
(2)B装置中的试剂是 。
(3)E装置中的作用是 。
(4)G装置中的试剂是 ,现象是 。
(5)从安全角度考虑,应后点燃 的酒精灯(填“A”或“G”)。你认为本实验尾气是否需要处理? (填“是”或“否”),如需处理,具体方案是 。
-
已知2Mg+CO2 2MgO+C,某同学根据金属活动顺序表推测钠与CO2也能反应,为探究反应产物,利用下图装置进行实验。(已知PdCl2能被CO还原为黑色的Pd,饱和NaHCO3溶液可以用于除去CO2 中的HC1气体)
2MgO+C,某同学根据金属活动顺序表推测钠与CO2也能反应,为探究反应产物,利用下图装置进行实验。(已知PdCl2能被CO还原为黑色的Pd,饱和NaHCO3溶液可以用于除去CO2 中的HC1气体)
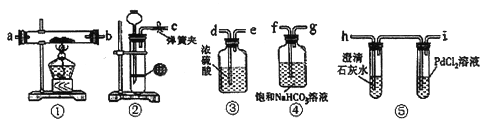
(1)原料中的金属钠通常保存在______中,实验室取用少量金属钠需要用到的实验用品有_____,____,玻璃片和小刀等。
(2)装置②中用稀盐酸与CaCO3反应制备CO2,制备该气体时发生反应的离子方程式是___________。
(3)请将图中各装置按顺序连接(填裝置接口字母): c接____,____接____,____接____,_____接______。
(4)装置③的作用是___________。
(5)检查完装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让CO2充满整个装置,当观察到________时再点燃酒精灯。此步操作的目的是__________。
(6)根据下列实验现象,推测并请写出钠与CO2反应的化学方程式___________。
I.实验过程中若观察到装置⑤PdCl2溶液中有黑色沉淀,且装置①中固体成分只有一种,向固体中加入稀盐酸可产生能使澄清石灰水变浑独的气体。请写出钠与CO2反应的化学方程式____________。
-
下图是铜与稀硝酸反应的两个实验装置图,请回答下列问题:
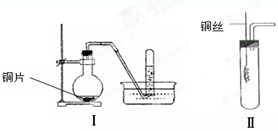
(1)铜与稀硝酸反应的化学方程式_____ _ 。
(2)学生甲用装置Ⅰ探究铜与稀硝酸反应的气体产物。实验过程在烧瓶中观察到有红棕色气体产生,在试管中收集到无色气体。 烧瓶中产生红棕色气体的原因是
(用方程式表示)。
(3)学生乙认为,甲用装置Ⅰ实验,无法说明问题。为了证明并观察到铜与稀硝酸反应的产物为NO,甲设计了如图Ⅱ所示的实验装置,选择下列药品,并按下列实验步骤完成该实验。请你根据他的思路,回答下列问题:
药品:稀硝酸锌粒石灰石固体
步骤:
①检查装置的气密性
②向试管中加入一定量CaCO3固体
③向试管中倒入过量的稀HNO3并迅速盖上带铜丝和导管的橡皮塞
④待反应完全后,将导管插入试管内接近液面
⑤将铜丝插入到溶液中
⑥用注射器的针头穿过橡皮塞并向试管内推入氧气(或空气)
(ⅰ)步骤②目的是 ;
(ⅱ)推入氧气或空气的目的是 ;
(ⅲ)分别将等质量的铜片与等体积均过量的浓硝酸和稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出,这可能是Cu2+的浓度差异引起的,你同意这种看法吗?(填“同意”或“不同意”),原因是 。
-
(12分)下图是铜与稀硝酸反应的两个实验装置图,请回答下列问题:
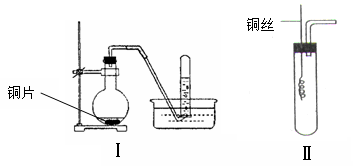
(1)铜与稀硝酸反应的化学方程式______________________。
(2)学生甲用装置Ⅰ探究铜与稀硝酸反应的气体产物。实验过程在烧瓶中观察到有红棕色气体产生,在试管中收集到无色气体。
烧瓶中产生红棕色气体的原因是________(用方程式表示) 。
(3)学生乙认为,甲用装置Ⅰ实验,无法说明问题。为了证明并观察到铜与稀硝酸反应的产物为NO,甲设计了如图Ⅱ所示的实验装置,选择下列药品,并按下列实验步骤完成该实验。请你根据他的思路,回答下列问题:
药品:稀硝酸 锌粒 石灰石固体
步骤:
①检查装置的气密性
②向试管中加入一定量CaCO3固体
③向试管中倒入过量的稀HNO3并迅速盖上带铜丝和导管的橡皮塞
④待反应完全后,将导管插入试管内接近液面
⑤将铜丝插入到溶液中
⑥用注射器的针头穿过橡皮塞并向试管内推入氧气(或空气)
(ⅰ)步骤①②目的是________ ;
(ⅱ)推入氧气或空气的目的是________;
(ⅲ)分别将等质量的铜片与等体积均过量的浓硝酸和稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出,这可能是Cu2+的浓度差异引起的,你同意这种看法吗?________ (填“同意”或“不同意”),原因是________ 。
-
(9分)下图是铜与稀硝酸反应的两个实验装置图,请回答下列问题:
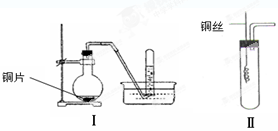
(1)铜与稀硝酸反应的化学方程式______________________。
(2)学生甲用装置Ⅰ探究铜与稀硝酸反应的气体产物。实验过程在烧瓶中观察到有红棕色气体产生,在试管中收集到无色气体。 烧瓶中产生红棕色气体的原因是
________(用方程式表示) 。
(3)学生乙认为,甲用装置Ⅰ实验,无法说明问题。为了证明并观察到铜与稀硝酸反应的产物为NO,甲设计了如图Ⅱ所示的实验装置,选择下列药品,并按下列实验步骤完成该实验。请你根据他的思路,回答下列问题:
药品:稀硝酸 锌粒 石灰石固体
步骤:
①检查装置的气密性
②向试管中加入一定量CaCO3固体
③向试管中倒入过量的稀HNO3并迅速盖上带铜丝和导管的橡皮塞
④待反应完全后,将导管插入试管内接近液面
⑤将铜丝插入到溶液中
⑥用注射器的针头穿过橡皮塞并向试管内推入氧气(或空气)
(ⅰ)步骤②目的是________ ;
(ⅱ)推入氧气或空气的目的是________;
(ⅲ)分别将等质量的铜片与等体积均过量的浓硝酸和稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出,这可能是Cu2+的浓度差异引起的,你同意这种看法吗?(填“同意”或“不同意”),原因是________ 。
-
(10分)不同浓度的硫酸与锌反应时,产物不同。为了验证这一事实,某同学拟用下图装置进行实验(假设实验条件为压强为101 kPa,温度为0℃)。
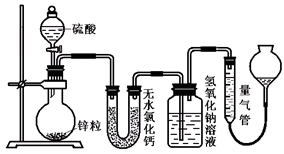
(1)若在烧瓶中放入1.3g锌粒,与c mol/L H2SO4反应,为保证实验结论的可靠,量气管的量程应不小于ml。
(2)若1.3g锌粒完全溶解,氢氧化钠洗气瓶增重l.28g,则圆底烧瓶中发生反应的化学方程式为:________。
(3)若在烧瓶中投入d g锌,加入一定量的c mol/L 浓硫酸V L,充分反应后锌有剩余,测得氢氧化钠洗气瓶增重m g,则整个实验过程产生的气体中,n(H2)+n(SO2)=________mol。(用含字母的代数式表示,需化简)。
(4)反应结束后,为了准确地测量气体体积,量气管在读数时除了视线与液面的最低处相平外,还要注意:
①________②________。
-
HNO3与金属反应后所得还原产物与硝酸的浓度和金属的活泼性有关。10mL 0.5mol·L-1 HNO3与0.048g Mg恰好完全反应。若氮元素只被还原到一种价态,下列说法正确的是
A. HNO3作还原剂 B. HNO3浓度越高,N元素还原价态越低
C. 反应中转移电子数为0.004mol D. 还原产物可能为NH4NO3
-
某兴趣小组的学生根据活泼金属Mg与CO2发生反应,推测活泼金属钠也能与CO2发生反应,因此兴趣小组用下列装置进行“钠与二氧化碳反应”的实验探究(尾气处理装置已略去).已知:常温下,CO能使一些化合物中的金属离子还原,例如:PdCl2+CO+H2O=Pd↓+CO2+2HCl.反应生成黑色的金属钯,此反应也可用来检测微量CO的存在.
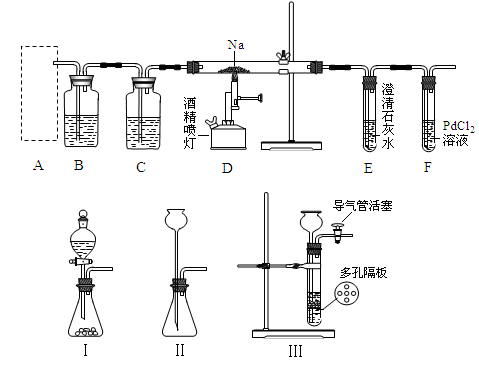
请回答下列问题:
(1)通常实验室制取CO2气体的离子方程式是__________________,为了使制气装置能“随开随用,随关随停”,上图A处应选用的装置是___________(填写“Ⅰ”、“Ⅱ”或“Ⅲ”).若要制取干燥、纯净的CO2,装置B、C中各盛放的试剂分别为______、_________。
(2)装入药品后,在点燃酒精喷灯前,必须进行的操作是___________待装置_______(填写字母)中出现_____________现象时,再点燃酒精喷灯,这步操作的目的是______________。
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是__________________。
②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式(需注明正确的反应条件)是______________________。








