-
某化学小组设计实验,探究“NO2是否能与炽热的铜反应生成氧化铜和氮气”。
已知:①NO和FeSO4溶液反应:NO+FeSO4=FeSO4·NO(棕色)
②酸性KMnO4溶液吸收NO生成NO 和Mn2+
和Mn2+
③Cu2O在酸性条件下能发生反应:Cu2O+2H+=Cu2++Cu+H2O
设计实验所需装置如图所示(每个装置中液态试剂均足量,且不考虑A装置挥发出的硝酸对后续装置的影响)。
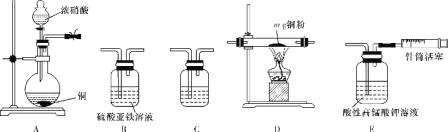
回答下列问题:
(1)该实验装置较复杂,检查气密性时采用分段检查的方法,请写出A装置气密性的检验方法___。
(2)该实验装置的连接顺序为:___(填装置字母代号),C装置中盛装试剂是___(填名称)。
(3)开始实验先引发A中反应,一段时间后再点燃D处酒精灯,这样操作的目的是___。
(4)实验过程中观察到下列现象,请回答:
①B中浅绿色溶液变棕色得出实验结论是___
a.二氧化氮与铜反应的还原产物一定有NO
b.二氧化氮与铜反应的还原产物一定无NO
c.二氧化氮与铜反应的还原产物可能有NO
②E中有明显现象,该现象是___,写出发生反应的离子方程式___。
(5)当D中铜粉完全反应时冷却至室温,停止A中反应,测得反应后D中固体粉末质量为ag,
①当a=___(用含m的代数式表示)时,铜被氧化的产物全部是CuO;
②设计最简单的实验方案,验证反应后D中固体是否含有Cu2O___(试剂选任)
-
资料表明:赤热铜能与NO2反应。某小组设计了如下实验装置进行探究,探究固体产物的成分,气体产物是N2还是NO。已知:酸性KMnO4溶液能氧化NO生成NO3ˉ;NO和FeSO4溶液反应:NO+FeSO4=[Fe(NO)]SO4(棕色);Cu2O+2H+=Cu+Cu2++H2O
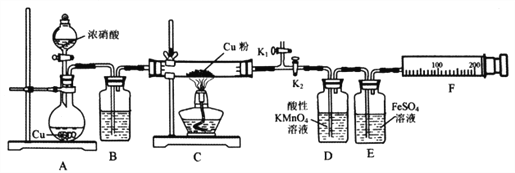
请回答下列问题:
(1)A中反应的化学方程式为________________________。
(2)检查装置气密性,装好药品,然后实验的正确操作顺序是____________
①关闭K1,打开K2 ②打开分液漏斗活塞
③打开K1,关闭K2 ④点燃C处酒精灯
(3)实验过程中,D装置中的现象是____________,能否根据D装置中的现象确认C中有无NO生成? ______,理由是__________。
(4)E装置的作用是____________。
(5)当铜粉完全反应后,实验小组对反应后的固体成分提出以下猜想:①只有CuO;②只有Cu2O;有同学认为可通过简单的定性实验即可判断猜想①是否成立,其实验方法是_____________________。
(6)实验中E装置自始至终未显棕色,小组最后通过定量实验得到如下数据。
| C装置质量 | F装置气体的体积(已折算为标准状况) |
| 玻管质量 | Cu质量 | 反应后(玻管+生成物) |
| mg | 1.92g | (m+2.24)g | 112mL |
据此写出实验时实际发生反应的化学方程式________________________。
-
资料表明:赤热铜能与NO2反应。某小组设计了如下实验装置进行探究,探究固体产物的成分,气体产物是N2还是NO。
已知:酸性KMnO4溶液能氧化NO生成NO3ˉ;
NO和FeSO4溶液反应:NO+FeSO4=[Fe(NO)]SO4(棕色);
Cu2O+2H+=Cu+Cu2++H2O
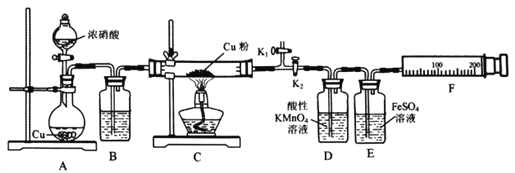
请回答下列问题:
(1)A中反应的化学方程式为________________________。
(2)检查装置气密性,装好药品,然后实验的正确操作顺序是____________
①关闭K1,打开K2 ②打开分液漏斗活塞
③打开K1,关闭K2 ④点燃C处酒精灯
(3)实验过程中,D装置中的现象是____________,能否根据D装置中的现象确认C中有无NO生成? ______,理由是________________________。
(4)E装置的作用是____________。
(5)当铜粉完全反应后,实验小组对反应后的固体成分提出以下猜想:①只有CuO;②只有Cu2O;有同学认为可通过简单的定性实验即可判断猜想①是否成立,其实验方法是_____________________。
(6)实验中E装置自始至终未显棕色,小组最后通过定量实验得到如下数据。
| C装置质量 | F装置气体的体积(已折算为标准状况) |
| 玻管质量 | Cu质量 | 反应后(玻管+生成物) |
| mg | 1.92g | (m+2.24)g | 112mL |
据此写出实验时实际发生反应的化学方程式________________________。
-
资料表明:赤热铜能与NO2反应。某小组设计了如下实验装置进行探究,探究固体产物的成分,气体产物是N2还是NO。
已知:酸性KMnO4溶液能氧化NO生成NO3ˉ;
NO和FeSO4溶液反应:NO+FeSO4=[Fe(NO)]SO4(棕色);
Cu2O+2H+=Cu+Cu2++H2O
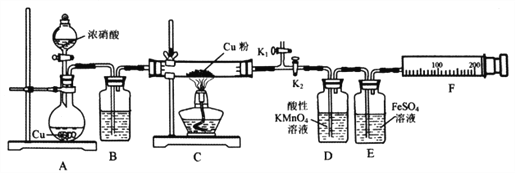
请回答下列问题:
(1)A中反应的化学方程式为________________________。
(2)检查装置气密性,装好药品,然后实验的正确操作顺序是____________
①关闭K1,打开K2 ②打开分液漏斗活塞
③打开K1,关闭K2 ④点燃C处酒精灯
(3)实验过程中,D装置中的现象是____________,能否根据D装置中的现象确认C中有无NO生成? ______,理由是________________________。
(4)E装置的作用是____________。
(5)当铜粉完全反应后,实验小组对反应后的固体成分提出以下猜想:①只有CuO;②只有Cu2O;有同学认为可通过简单的定性实验即可判断猜想①是否成立,其实验方法是_____________________。
(6)实验中E装置自始至终未显棕色,小组最后通过定量实验得到如下数据。
| C装置质量 | F装置气体的体积(已折算为标准状况) |
| 玻管质量 | Cu质量 | 反应后(玻管+生成物) |
| mg | 1.92g | (m+2.24)g | 112mL |
据此写出实验时实际发生反应的化学方程式________________________。
-
某同学做“FeSO4被HNO3氧化”的实验,发现溶液变深棕色。猜想可能是生成的NO2或NO与Fe2+或Fe3+反应,使溶液变为深棕色,设计下列装置探究。下列说法错误的是
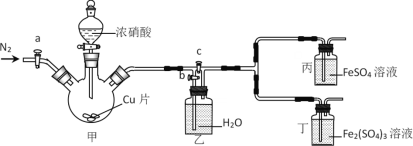
A.先检查装置气密性,加入药品后,关闭c,打开a和b,再通入一段时间N2
B.关闭a、c,打开b及分液漏斗活塞,反应后丙中溶液变为深棕色,丁中溶液无明显变化,证明NO与Fe2+反应
C.甲中反应一段时间后,更新丙、丁中试剂,关闭a和b,打开c,反应后丙中溶液变为深棕色,丁中溶液无明显变化,证明NO2也可与Fe2+反应
D.该实验的缺陷是缺少尾气吸收装置
-
І.为探究铜与稀硝酸反应的气态产物中是否含NO2,进行如下实验。
已知: FeSO4+NO→[Fe(NO)]SO4,该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色。

(1)实验前需检验装置的气密性,简述操作_____________________________________。
(2)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是__________________________________________________________________;铜片和稀硝酸反应的化学方程式为________________________________。
(3)洗气瓶中加入KSCN溶液的目的及原理是______________________________________;本实验只观察到洗气瓶中出现了棕色,写出尾气处理的化学方程式________________。
ІІ.实验室制备的CuSO4·5H2O中常含Cu(NO3)2,用重量法测定CuSO4·5H2O的含量。
(4)实验步骤为:①___________②加水溶解③加氯化钡溶液,沉淀④过滤(其余步骤省略),在过滤前,需要检验是否沉淀完全,其操作是_________________________________。
(5)若1.040 g试样中含CuSO4·5H2O的准确值为1.015 g,而实验测定结果是l.000 g 测定的相对误差为____________。
-
为探究铜与6mol•L-1硝酸反应的气态产物中是否含NO2,进行如下实验。
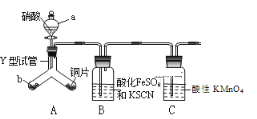
已知:FeSO4+NO  [Fe(NO)]SO4(棕色),该反应较缓慢,待生成一定量2+时突显明显棕色。
[Fe(NO)]SO4(棕色),该反应较缓慢,待生成一定量2+时突显明显棕色。
(1)实验前需检验装置的气密性,简述操作_____________________________________。
(2)仪器a的名称____________
(3)实验开始时先将Y形试管向盛有块状固体b的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是_________;
(4)证明有NO2的实验现象___________________________________
(5)装置C的作用________,反应离子方程式____________。
(6)测定化学试剂绿矾(FeSO4·7H2O)纯度的方法:称取绿矾3.000g置于锥形瓶中,加入100mL蒸馏水,加入10mLH2SO4和5mLH3PO4,用0.1000molL-1KMnO4溶液滴定至终点,消耗KMnO4溶液20.00mL。KMnO4溶液盛放在棕色_____式(填“酸”或“碱”)滴定管中,列式计算绿矾的纯度_______________________。
-
为探究铜与稀硝酸反应的气态产物中是否含NO2,进行如下实验.
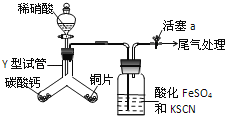
已知:FeSO4+NO→[Fe(NO)]SO4,该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色.
(1)实验前需检验装置的气密性,简述操作__.
(2)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是__;铜片和稀硝酸反应的化学方程式为__.
(3)洗气瓶中加入KSCN溶液的目的及原理是__;本实验只观察到洗气瓶中出现了棕色,写出尾气处理的化学方程式__.
-
为探究铜与6mol•L﹣1硝酸反应的气态产物中是否含NO2,进行如下实验.
已知:FeSO4+NO⇌[Fe(NO)]SO4(棕色),该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色.
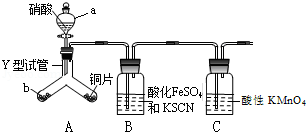
(1)实验前需检验装置的气密性,简述操作 .
(2)仪器a的名称
(3)实验开始时先将Y形试管向盛有块状固体b的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是 ;
(4)证明有NO2的实验现象
(5)装置C的作用 ,反应离子方程式 .
(6)测定化学试剂绿矾(FeSO4•7H2O)纯度的方法:称取绿矾3.000g置于锥形瓶中,加入100mL蒸馏水,加入10mLH2SO4和5mLH3PO4,用0.1000molL﹣1KMnO4溶液滴定至终点,消耗KMnO4溶液20.00mL.KMnO4溶液盛放在棕色 式(填“酸”或“碱”)滴定管中,列式计算绿矾的纯度 .
-
某校化学学习小组拟验证NO能被氨气还原并测定其转化率,设计如下实验:
参考知识:NO气体与FeSO4溶液反应生成可溶性硫酸亚硝基合铁(Ⅱ):NO+FeSO4=Fe(NO)SO4
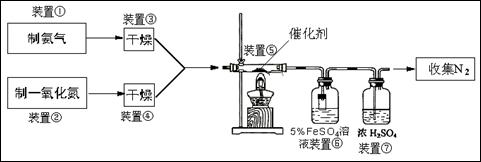
试回答下列问题:

⑴实验室用氯化铵与氢氧化钙固体制备氨气,应选用的装置是________
该反应的化学方程式________
实验室通常用________法收集氨气,检验该气体是否收集满方法________
⑵装置③、④若用同一装置,则该装置中所盛装的药品是________
A.Na2O2 B.浓硫酸 C.P2O5 D.碱石灰
⑶装置⑥中,粗玻璃管X的作用________,装置⑦的作用________
⑷装置⑥的广口瓶中,除生成Fe(NO)SO4外,还有白色沉淀生成,写出生成该沉淀的离子方程式________
⑸若参加反应的NO为2.688L(标准状况,下同),氨气过量,最后收集到2.016LN2,则装置⑤中NO的转化率为________
和Mn2+










