-
为探究铜与6mol•L﹣1硝酸反应的气态产物中是否含NO2,进行如下实验.
已知:FeSO4+NO⇌[Fe(NO)]SO4(棕色),该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色.
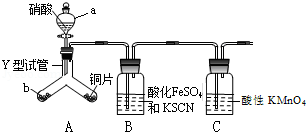
(1)实验前需检验装置的气密性,简述操作 .
(2)仪器a的名称
(3)实验开始时先将Y形试管向盛有块状固体b的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是 ;
(4)证明有NO2的实验现象
(5)装置C的作用 ,反应离子方程式 .
(6)测定化学试剂绿矾(FeSO4•7H2O)纯度的方法:称取绿矾3.000g置于锥形瓶中,加入100mL蒸馏水,加入10mLH2SO4和5mLH3PO4,用0.1000molL﹣1KMnO4溶液滴定至终点,消耗KMnO4溶液20.00mL.KMnO4溶液盛放在棕色 式(填“酸”或“碱”)滴定管中,列式计算绿矾的纯度 .
-
为探究铜与6mol•L-1硝酸反应的气态产物中是否含NO2,进行如下实验。
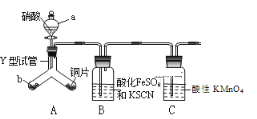
已知:FeSO4+NO  [Fe(NO)]SO4(棕色),该反应较缓慢,待生成一定量2+时突显明显棕色。
[Fe(NO)]SO4(棕色),该反应较缓慢,待生成一定量2+时突显明显棕色。
(1)实验前需检验装置的气密性,简述操作_____________________________________。
(2)仪器a的名称____________
(3)实验开始时先将Y形试管向盛有块状固体b的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是_________;
(4)证明有NO2的实验现象___________________________________
(5)装置C的作用________,反应离子方程式____________。
(6)测定化学试剂绿矾(FeSO4·7H2O)纯度的方法:称取绿矾3.000g置于锥形瓶中,加入100mL蒸馏水,加入10mLH2SO4和5mLH3PO4,用0.1000molL-1KMnO4溶液滴定至终点,消耗KMnO4溶液20.00mL。KMnO4溶液盛放在棕色_____式(填“酸”或“碱”)滴定管中,列式计算绿矾的纯度_______________________。
-
І.为探究铜与稀硝酸反应的气态产物中是否含NO2,进行如下实验。
已知: FeSO4+NO→[Fe(NO)]SO4,该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色。

(1)实验前需检验装置的气密性,简述操作_____________________________________。
(2)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是__________________________________________________________________;铜片和稀硝酸反应的化学方程式为________________________________。
(3)洗气瓶中加入KSCN溶液的目的及原理是______________________________________;本实验只观察到洗气瓶中出现了棕色,写出尾气处理的化学方程式________________。
ІІ.实验室制备的CuSO4·5H2O中常含Cu(NO3)2,用重量法测定CuSO4·5H2O的含量。
(4)实验步骤为:①___________②加水溶解③加氯化钡溶液,沉淀④过滤(其余步骤省略),在过滤前,需要检验是否沉淀完全,其操作是_________________________________。
(5)若1.040 g试样中含CuSO4·5H2O的准确值为1.015 g,而实验测定结果是l.000 g 测定的相对误差为____________。
-
为探究铜与稀硝酸反应的气态产物中是否含NO2,进行如下实验.
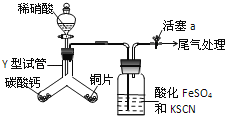
已知:FeSO4+NO→[Fe(NO)]SO4,该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色.
(1)实验前需检验装置的气密性,简述操作__.
(2)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是__;铜片和稀硝酸反应的化学方程式为__.
(3)洗气瓶中加入KSCN溶液的目的及原理是__;本实验只观察到洗气瓶中出现了棕色,写出尾气处理的化学方程式__.
-
(12分)为探究铜与稀硝酸反应的产物及影响反应速率的主要因素,进行如下实验。
实验一 探究铜和稀硝酸反应的产物。
实验装置如图,气密性已检查。
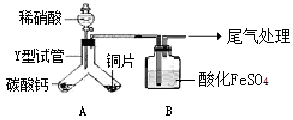
已知:FeSO4+NO=[Fe(NO)]SO4,该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色。
(1)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是 。
(2)铜片和稀硝酸反应的化学方程式为 。
(3)本实验A生成的气体中,若有NO2,B的实验现象为 ;若只有NO生成,B的实验现象是 。
实验二 探究铜和稀硝酸反应速率先慢后快的原因
经过实验一,测得硝酸的浓度<6 mol•L-1,只有NO生成。当铜片与5 mol•L-1硝酸反应时,开始时反应非常缓慢,一段时间后反应速率明显加快。为探究此反应的反应速率先慢后快的原因,进行如下探究:
探究一:研究反应过程的温度变化对反应速率的影响,实验所得曲线和现象记录如下图表。
| 时间/min | 现象 |
| 0~15 | 铜表面出现气泡,但速度很慢 |
| 25 | 溶液有很浅的蓝色,气泡生成速度加快 |
| 30 | 气泡生成速度较快,均匀冒出 |
| 45 | 洗气瓶中可见少量淡棕色的物质 |
| 50 | 溶液中蓝色明显变深,洗气瓶中突显明显棕色 |
(4)获得图2数据所需的测量仪器有________________________________。
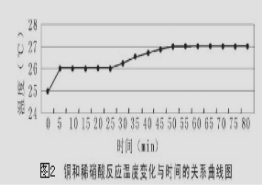
(5)从上述图表分析可得到的结论是 。
| 序号 | 温度 | 铜片/g | 硝酸/mL | 硝酸铜/g |
| 1 | 25℃ | ① | ② | ③ |
| 2 | 25℃ | 5 | 20 | 0.5 |
| 3 | 25℃ | 5 | 20 | 1.0 |
探究二:研究化学反应产物对反应速率的影响
设计了如下实验,利用上图装置测定溶液突显明显棕色的时间。
(6)请将上表中将实验1的实验条件填写完整① ② ③
(7)通过实验发现实验1、2、3的反应速率并无明显变化,为达到实验目的还需要继续进行的实验是 。
-
资料表明:赤热铜能与NO2反应。某小组设计了如下实验装置进行探究,探究固体产物的成分,气体产物是N2还是NO。已知:酸性KMnO4溶液能氧化NO生成NO3ˉ;NO和FeSO4溶液反应:NO+FeSO4=[Fe(NO)]SO4(棕色);Cu2O+2H+=Cu+Cu2++H2O
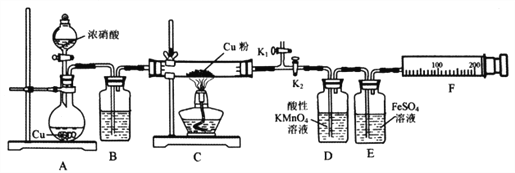
请回答下列问题:
(1)A中反应的化学方程式为________________________。
(2)检查装置气密性,装好药品,然后实验的正确操作顺序是____________
①关闭K1,打开K2 ②打开分液漏斗活塞
③打开K1,关闭K2 ④点燃C处酒精灯
(3)实验过程中,D装置中的现象是____________,能否根据D装置中的现象确认C中有无NO生成? ______,理由是__________。
(4)E装置的作用是____________。
(5)当铜粉完全反应后,实验小组对反应后的固体成分提出以下猜想:①只有CuO;②只有Cu2O;有同学认为可通过简单的定性实验即可判断猜想①是否成立,其实验方法是_____________________。
(6)实验中E装置自始至终未显棕色,小组最后通过定量实验得到如下数据。
| C装置质量 | F装置气体的体积(已折算为标准状况) |
| 玻管质量 | Cu质量 | 反应后(玻管+生成物) |
| mg | 1.92g | (m+2.24)g | 112mL |
据此写出实验时实际发生反应的化学方程式________________________。
-
资料表明:赤热铜能与NO2反应。某小组设计了如下实验装置进行探究,探究固体产物的成分,气体产物是N2还是NO。
已知:酸性KMnO4溶液能氧化NO生成NO3ˉ;
NO和FeSO4溶液反应:NO+FeSO4=[Fe(NO)]SO4(棕色);
Cu2O+2H+=Cu+Cu2++H2O
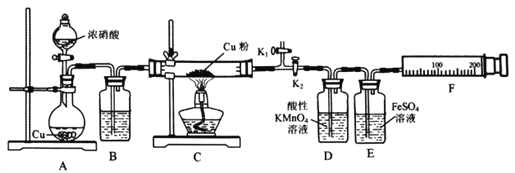
请回答下列问题:
(1)A中反应的化学方程式为________________________。
(2)检查装置气密性,装好药品,然后实验的正确操作顺序是____________
①关闭K1,打开K2 ②打开分液漏斗活塞
③打开K1,关闭K2 ④点燃C处酒精灯
(3)实验过程中,D装置中的现象是____________,能否根据D装置中的现象确认C中有无NO生成? ______,理由是________________________。
(4)E装置的作用是____________。
(5)当铜粉完全反应后,实验小组对反应后的固体成分提出以下猜想:①只有CuO;②只有Cu2O;有同学认为可通过简单的定性实验即可判断猜想①是否成立,其实验方法是_____________________。
(6)实验中E装置自始至终未显棕色,小组最后通过定量实验得到如下数据。
| C装置质量 | F装置气体的体积(已折算为标准状况) |
| 玻管质量 | Cu质量 | 反应后(玻管+生成物) |
| mg | 1.92g | (m+2.24)g | 112mL |
据此写出实验时实际发生反应的化学方程式________________________。
-
资料表明:赤热铜能与NO2反应。某小组设计了如下实验装置进行探究,探究固体产物的成分,气体产物是N2还是NO。
已知:酸性KMnO4溶液能氧化NO生成NO3ˉ;
NO和FeSO4溶液反应:NO+FeSO4=[Fe(NO)]SO4(棕色);
Cu2O+2H+=Cu+Cu2++H2O
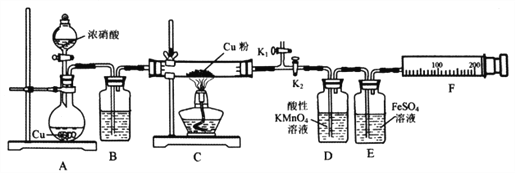
请回答下列问题:
(1)A中反应的化学方程式为________________________。
(2)检查装置气密性,装好药品,然后实验的正确操作顺序是____________
①关闭K1,打开K2 ②打开分液漏斗活塞
③打开K1,关闭K2 ④点燃C处酒精灯
(3)实验过程中,D装置中的现象是____________,能否根据D装置中的现象确认C中有无NO生成? ______,理由是________________________。
(4)E装置的作用是____________。
(5)当铜粉完全反应后,实验小组对反应后的固体成分提出以下猜想:①只有CuO;②只有Cu2O;有同学认为可通过简单的定性实验即可判断猜想①是否成立,其实验方法是_____________________。
(6)实验中E装置自始至终未显棕色,小组最后通过定量实验得到如下数据。
| C装置质量 | F装置气体的体积(已折算为标准状况) |
| 玻管质量 | Cu质量 | 反应后(玻管+生成物) |
| mg | 1.92g | (m+2.24)g | 112mL |
据此写出实验时实际发生反应的化学方程式________________________。
-
甲、乙两同学用下图所示装置进行实验,探究硝酸与铁反应的产物.
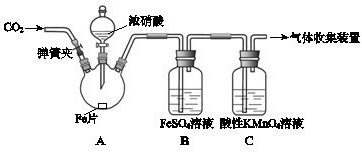
文献记载:I.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+4、+2、-3价等氮的化合物.
II.FeSO4+NO⇌Fe(NO)SO4(棕色)△H<0.
III.NO2和NO都能被KMnO4氧化吸收.
甲的实验操作和现象记录如下:
| 实验操作 | 实验现象 |
| 打开弹簧夹,通入一段时间CO2,关闭弹簧夹. | |
| 打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞. | 无明显现象. |
| 加热烧瓶,反应开始后停止加热. | ①A中有红棕色气体产生,一段时间后,气体颜色逐渐变浅; B中溶液变棕色; C中溶液紫色变浅.
②反应停止后,A中无固体剩余. |
请回答下列问题:
(1)滴入浓硝酸加热前没有明显现象的原因是________.
(2)检验是否生成-3价氮的化合物,应进行的实验操作是________.
(3)甲取少量B中溶液,加热,实验现象是________.请用化学平衡原理解释原因:________.甲依据该现象得出的结论是A中有NO生成.
(4)乙认为甲得出A中有NO生成的证据不足.为获取充足的证据,乙仍采用该装置和操作进行对照实验,乙作出的改变是________,证明有NO生成的实验现象是________.
(5)证明A溶液中是否含有Fe2+和Fe3+,选择的药品是(填序号)________.
a.铁粉 b.溴水 c.鉄氰化钾溶液 d.硫氰化钾溶液.
-
硝酸与金属反应时,浓度不同生成的还原产物也可能不同。某兴趣小组进行了如下实验探究。
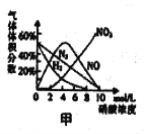
[查阅资料]
a.镁与硝酸反应生成各气体产物成分及含量随HNO3浓度变化曲线如图甲所示:
b.NO2沸点:21℃;NO沸点:-151℃
c.2NO2+2OH-=NO3-+NO2-+H2O,NO+NO2+2OH-=2NO2-+H2O
[实验探究] 该小组拟选用如图A B C D所示装置探究镁与4 mol·L-1硝酸反应的产物。连接装置A→B→C→D→C,检查气密性,按图示加入试剂,D中通入的O2微过量。
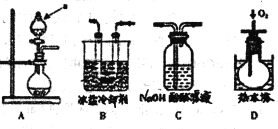
(1)后一个C装置的作用是_______,证明气体产物中有NO生成的实验现象是______。
(2)从第一个C装置中逸出的气体成分是________。
(3)溶液中还可能有一种还原产物,这种还原产物可能是_____,请设计实验验证你的猜想________;并写出生成该还原产物的化学方程式_____________











