25℃时,向20. 00 mL 0.1 mol/L H2X溶液中滴入0.1 mo1/L NaOH溶液,溶液中由水电离出的c水(OH-) 的负对数[一lgc水(OH-)]即pOH水-与所加NaOH溶液体积的关系如图所示。下列说法中正确的是

A.水的电离程度:M>P B.图中P点至Q点对应溶液中逐渐增大
C.N点和Q点溶液的pH相同 D.P点溶液中
高二化学单选题中等难度题
25℃时,向20. 00 mL 0.1 mol/L H2X溶液中滴入0.1 mo1/L NaOH溶液,溶液中由水电离出的c水(OH-) 的负对数[一lgc水(OH-)]即pOH水-与所加NaOH溶液体积的关系如图所示。下列说法中正确的是

A.水的电离程度:M>P B.图中P点至Q点对应溶液中逐渐增大
C.N点和Q点溶液的pH相同 D.P点溶液中
高二化学单选题中等难度题
25℃时,向20. 00 mL 0.1 mol/L H2X溶液中滴入0.1 mo1/L NaOH溶液,溶液中由水电离出的c水(OH-) 的负对数[一lgc水(OH-)]即pOH水-与所加NaOH溶液体积的关系如图所示。下列说法中正确的是

A.水的电离程度:M>P B.图中P点至Q点对应溶液中逐渐增大
C.N点和Q点溶液的pH相同 D.P点溶液中
高二化学单选题中等难度题查看答案及解析
室温下,某一元弱酸HA的电离常数K=1.6×10-6。 向20.00 mL 浓度约为0.1 mol·L-1 HA溶液中逐滴加入0.1000 mol·L-1 的标准NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:(已知lg4=0.6)
(1)a点溶液中pH约为________,此时溶液中H2O电离出的c(H+)为________。
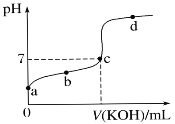
(2)a、b、c、d四点中水的电离程度最大的是________点,滴定过程中宜选用__________作指示剂,滴定终点在________(填“c点以上”或“c点以下”)。
(3)滴定过程中部分操作如下,下列各操作使测量结果偏高的是_________________(填字母序号)。
A.滴定前碱式滴定管未用标准NaOH溶液润洗
B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定
C.滴定过程中,溶液出现变色后,立即停止滴定
D.滴定结束后,仰视液面,读取NaOH溶液体积
(4)若重复三次滴定实验的数据如下表所示,计算滴定所测HA溶液的物质的量浓度为_____mol/L。
| 实验序号 | NaOH溶液体积/mL | 待测HA溶液体积/mL |
| 1 | 21.01 | 20.00 |
| 2 | 20.99 | 20.00 |
| 3 | 21.60 | 20.00 |
高二化学综合题中等难度题查看答案及解析
室温下,将1.000 mol/L盐酸滴入20.00 mL 1.000 mo1/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是( )
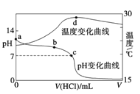
A. a点由水电离出的c(H+) = 1.0 × 10-14 mo1/L
B. b点:c(NH4+) > c(Cl-) > c(OH-) > c(H+)
C. c点:盐酸与氨水恰好完全反应
D. d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热
高二化学单选题困难题查看答案及解析
室温下,将1.000 mol/L盐酸滴入20.00 mL 1.000 mo1/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是( )
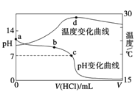
A. a点由水电离出的c(H+) = 1.0 × 10-14 mo1/L
B. b点:c(NH4+) > c(Cl-) > c(OH-) > c(H+)
C. c点:盐酸与氨水恰好完全反应
D. d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热
高二化学单选题困难题查看答案及解析
常温下,向20.00mL0.1mol·L-1KOH溶液中滴加0.1 mol·L -1HA(弱酸)溶液,混合溶液中水电离出的c(OH-)与HA溶液体积之间的关系如图I所示:向20.00mL0.1 mol ·L-1 HA溶液中滴加0. 1mol ·L-1 KOH溶液,混合溶液中水电离出的c(OH-)与KOH溶液体积之间的关系如图II所示。
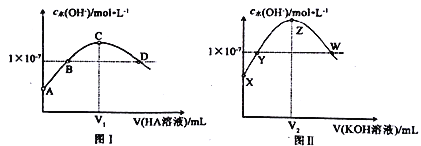
下列有关说法正确的是
A.A点、X点对应溶液中水的电离程度相同
B.B点、Y点对应溶液的pH相等
C.C点、Z点对应溶液中都存在:c(OH-)=c(H+)+c(HA)
D.D点、W点对应溶液中分别都存在:c(K+)=c(A-)
高二化学单选题中等难度题查看答案及解析
某同学用0.1 mol/L 的盐酸滴定20.00 mL NaOH溶液,测定其浓度。下列操作正确的是
A. 需用NaOH溶液润洗锥形瓶
B. 用量筒量取20.00 mL NaOH溶液
C. 滴定前,使酸式滴定管尖嘴部分充满盐酸
D. 充分反应后,滴入酚酞溶液,观察是否到达滴定终点
高二化学单选题简单题查看答案及解析
常温下,向20 mL 0.1 mol·L−1的HA溶液中逐滴加入0.1mol·L−1的NaOH溶液,溶液中水所电离的c水(H+)随加入NaOH溶液体积的变化如图所示,下列说法正确的是
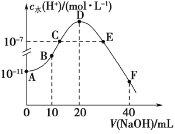
A.HA的电离常数Ka约为1×10−5
B.B点的溶液中粒子浓度满足关系:c(HA)>c(Na+)>c(A−)
C.C、E两点因为对水的电离的抑制作用和促进作用相同,所以溶液均呈中性
D.F点的溶液呈碱性,粒子浓度满足关系c(OH−)=c(HA)+c(A−)+c(H+)
高二化学单选题中等难度题查看答案及解析
室温下向10mL 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA溶液pH的变化曲线如图所示。下列说法不正确的是
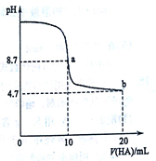
A.在逐滴加入HA溶液至20mL时,NaOH溶液中水的电离程度先增大后减小
B.b点所示溶液中c(A-)>c(HA)
C.pH=7时,c(Na+)=c(A-)+c(HA)
D.该酸是弱酸
高二化学选择题简单题查看答案及解析
25℃时,向 20 mL 0.1 mol/L NaOH 溶液中逐滴加入 0.1 mol/L 醋酸溶液,滴定曲线如图所示。下列说法正确的是
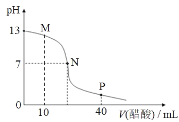
A.该NaOH 溶液中水电离出的 c(OH-)=1×10-12 mol/L
B.M 点时,c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.P 点时,c(CH3COO-)+c(CH3COOH)=2c(Na+)
D.N 点对应的横坐标是 20
高二化学单选题中等难度题查看答案及解析
用0.1mol/LNaOH溶液分别滴定体积均为20.00 mL、浓度均为0.1mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
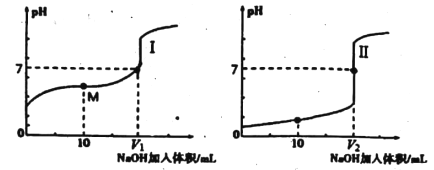
(1)用NaOH溶液滴定醋酸溶液通常所选择的指示剂为________;符合其滴定曲线的是______(填“I”或“Ⅱ”)。
(2)图中V1和V2大小的比较:V1_____V2(填“>”、“<”或“=”)。
(3)滴定前的上述三种溶液中。由水电离出的c(H+)最大的是_____溶液(填化学式)。
(4)若用0.1mol/LNaOH溶液滴定未知浓度的醋酸,滴定前仰视,滴定后平视,则所测结果____(填“偏低”,“偏高”或“不变”)。
高二化学填空题中等难度题查看答案及解析