25℃时,用0.1mol•L-1NaOH溶液滴定某二元弱酸H2A,H2A被滴定分数、pH及物种分布分数δ[δ(X)=]如图所示:
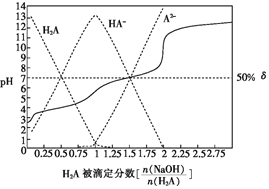
下列说法错误的是( )
A.用NaOH溶液滴定0.1mol•L-1NaHA溶液可用酚酞作指示剂
B.0.1mol•L-1NaHA溶液中:c(Na+)>c(HA-)>c(H2A)>c(A2-)
C.0.1mol•L-1Na2A溶液中:c(Na+)>c(HA-)+2c(A2-)
D.H2A的Ka2=1×10-7
高三化学单选题中等难度题
25℃时,用0.1mol•L-1NaOH溶液滴定某二元弱酸H2A,H2A被滴定分数、pH及物种分布分数δ[δ(X)=]如图所示:

下列说法错误的是( )
A.用NaOH溶液滴定0.1mol•L-1NaHA溶液可用酚酞作指示剂
B.0.1mol•L-1NaHA溶液中:c(Na+)>c(HA-)>c(H2A)>c(A2-)
C.0.1mol•L-1Na2A溶液中:c(Na+)>c(HA-)+2c(A2-)
D.H2A的Ka2=1×10-7
高三化学单选题中等难度题
25 ℃时,用0.1 mol·L-1NaOH溶液滴定某二元弱酸H2A,H2A被滴定分数、pH及物种分布分数δ[δ(X)=]如图所示:
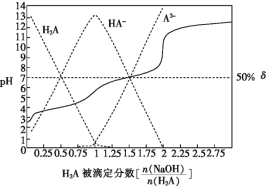
下列说法错误的是
A.用NaOH溶液滴定0.1 mol·L-1NaHA溶液可用酚酞作指示剂
B.0.1 mol·L-1Na2A溶液中:c(Na+)<c(HA-)+2c(A2-)
C.0.1 mol·L-1NaHA溶液中:c(Na+)>c(HA-)>c(H2A)>c(A2-)
D.H2A 的Ka2=1×10-7
高三化学多选题困难题查看答案及解析
25℃时,用0.1mol•L-1NaOH溶液滴定某二元弱酸H2A,H2A被滴定分数、pH及物种分布分数δ[δ(X)=]如图所示:

下列说法错误的是( )
A.用NaOH溶液滴定0.1mol•L-1NaHA溶液可用酚酞作指示剂
B.0.1mol•L-1NaHA溶液中:c(Na+)>c(HA-)>c(H2A)>c(A2-)
C.0.1mol•L-1Na2A溶液中:c(Na+)>c(HA-)+2c(A2-)
D.H2A的Ka2=1×10-7
高三化学单选题中等难度题查看答案及解析
25 ℃时,用0.1 mol/LNaOH溶液滴定某二元弱酸H2A,H2A被滴定分数、pH及物种分布分数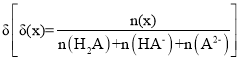 如图所示:
如图所示:
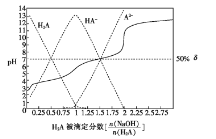
下列说法错误的是
A.用NaOH溶液滴定0.1 mol·L-1NaHA溶液可用酚酞作指示剂
B.0.1 mol·L-1NaA溶液中:
C.0.1 mol·L-1NaHA溶液中:
D.H2A 的K2=1×10-7
高三化学单选题困难题查看答案及解析
25℃时,用0.1 mol·L-1 NaOH溶液滴定某二元弱酸H2A,H2A被滴定分数、pH及物种分布分数δ[δ(X)=]如图所示:
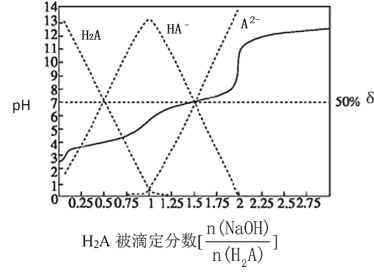
下列说法错误的是
A.用NaOH溶液滴定0.1 mol·L-1 NaHA溶液可用酚酞作指示剂
B.0.1 mol·L-1 NaHA溶液中:c(Na+)>c(HA-)>c(A2-)>c(H2A)
C.0.1 mol·L-1 Na2A溶液中:c(Na+)<c(HA-)+2c(A2-)
D.H2A的K2=1×10-7
高三化学单选题中等难度题查看答案及解析
常温下用0.1mol·L-1NaOH溶液滴定10.00mL二元弱酸H2A溶液,滴定曲线如图所示,d点恰好中和。假设混合时溶液体积变化忽略不计,下列说法不正确的是
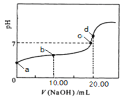
A.a点pH>1
B.c点时c(Na+)=c(H2A)+2c(A2-)+c(HA-)
C.b点时:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
D.滴定过程中c(Na+)+c(A2-)+c(HA-)+c(H2A)=0.1mol/L
高三化学单选题中等难度题查看答案及解析
温室下,向100 mL 0.1 mol·L-1二元酸H2A溶液中加入0.1 mol·L-1NaOH溶液,溶液的pH随NaOH溶液体积的变化曲线如图所示。下列说法不正确的是
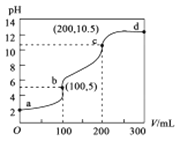
A. H2A为二元弱酸
B. a、b、c、d四种状态中水的电离程度最大的是c点
C. b点存在:c(Na+)>c(HA-)>c(H+)>c(OH-)>c(A2-)
D. c点存在:c(OH-)=c(H+)+c(HA-)+2c(H2A)
高三化学单选题中等难度题查看答案及解析
0.1 mol/L二元弱酸H2A溶液中滴加0.1mol/LNaOH溶液,溶液中的H2A、HA-、A2 -的物质的量分数δ(x)随pH的变化如图所示。下列说法错误的是
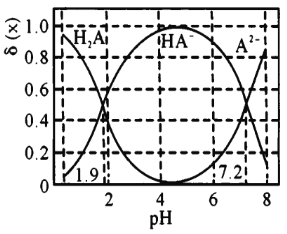
A.pH =1.9时,c(Na+)<c(HA-)+2c(A2-)
B.当c(Na+)=c(H2A)+c(HA-)+c(A2-)时,溶液pH>7
C.pH=6时,c(Na+)>c(HA-)>c(A2-)>c(H2A)
D.lg[Ka2(H2A)]=-7.2
高三化学单选题中等难度题查看答案及解析
向10 mL 0.1mol/L二元弱酸H2A溶液中滴加0.1mol/L NaOH 溶液,溶液中各组分物质的量分数δ(X) [δ(X)=]随pH的变化如图所示。下列叙述错误的是

A. Ka1(H2A) 为10-3.1
B. pH=5.0时,c(Na+)>c(HA-)>c(H+)>c(OH-) >c(A2-)
C. pH=8.2时,c (Na+) +c(H+) =c(OH-) +3c(A2-)
D. pH 由5.0 调至10.5 时,主要反应的离子方程式为HA-+OH-=A2-+H2O
高三化学单选题困难题查看答案及解析
H2A是二元弱酸,25℃时,配制一组c(H2A)+c(HA-)+c(A2-)=0.1mol·L-1的H2A和NaOH混合溶液,溶液中H2A、HA-和A2-所占三种粒子总数的物质的量分数(α)随溶液pH变化的关系如图所示。下列说法正确的是
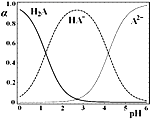
A.c(Na+)=0.1mol·L-1的溶液中:c(H+)=c(A2-)+c(OH-)-c(H2A)
B.c (HA-)=c(A2-)的溶液中:c(Na+)>3c(A2-)
C.c (HA-)=0.5mol·L-1的溶液中:2c(H2A)+c(H+)=c(OH-)+1.5mol·L-1
D.pH=2的溶液中:c(HA-)+2c(A2-)<0.1
高三化学多选题中等难度题查看答案及解析
常温下,向0.1mol·L−1二元弱酸H2A的溶液中逐滴加入NaOH溶液,H2A、HA-、A2−的物质的量分数随pH的变化如图所示。下列叙述正确的是( )
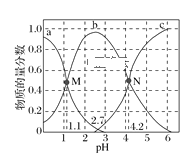
A.a曲线代表HA−的物质的量分数随pH的变化
B.M点pH=1.1时,溶液中微粒浓度关系为c(H+)>c(HA−)=c(H2A)
C.pH=2.7时,c(A2−)+c(HA−)+c(H2A)=0.1mol·L−1
D.N点pH=4.2时,c(A2−)=c(HA−),溶液中不存在H2A分子
高三化学单选题中等难度题查看答案及解析