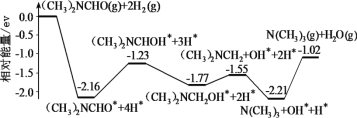-
我国科学家实现了在铜催化剂条件下将DMF[(CH3)2NCHO]转化为三甲胺[N(CH3)3]。计算机模拟单个DMF分子在铜催化剂表面的反应历程如图所示,下列说法正确的是
A.该历程中最小能垒的化学方程式为 (CH3)2NCH2OH*=(CH3)2NCH2+OH*
B.该历程中最大能垒(活化能)为2.16eV
C.该反应的热化学方程式为(CH3)2NCHO(g)+2H2(g)=N(CH3)3(g)+H2O(g) ΔH=-1.02ev•mol-1
D.增大压强或升高温度均能加快反应速率,并增大DMF平衡转化率
-
我国科学家结合实验与计算机模拟结果,研究了在铁掺杂W18O49纳米反应器催化剂表面上实现常温低电位合成氨,获得较高的氨产量和法拉第效率。反应历程如图所示,其中吸附在催化剂表面的物种用*标注。
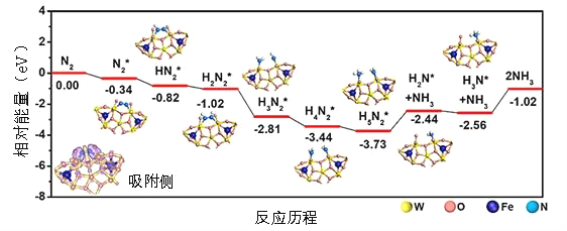
(1)需要吸收能量最大的能垒(活化能)E=__ev,该步骤的化学方程式为___;
(2)对于合成氨反应N2+3H2 2NH3,在标况下,平衡常数Kθ=
2NH3,在标况下,平衡常数Kθ= ,其中pθ为标准压强(1×105Pa),p(NH3)、p(N2)和p(H2)为各组分的平衡分压[已知p(NH3)=x(NH3)p,其中p为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数]。
,其中pθ为标准压强(1×105Pa),p(NH3)、p(N2)和p(H2)为各组分的平衡分压[已知p(NH3)=x(NH3)p,其中p为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数]。
①若起始N2和H2物质的量之比为1:3,反应在恒定温度和标准压强下进行,达到平衡时H2的转化率为ɑ,则Kθ=___(用含ɑ的最简式表示)。
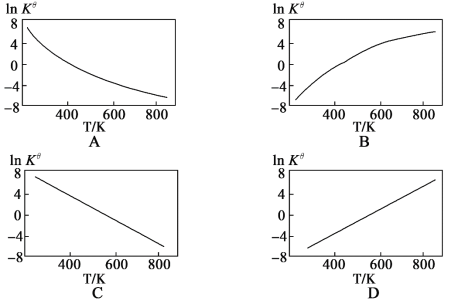
②图中可以示意标准平衡常数Kθ随温度T变化趋势的是___(填序号).
(3)利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如图所示。
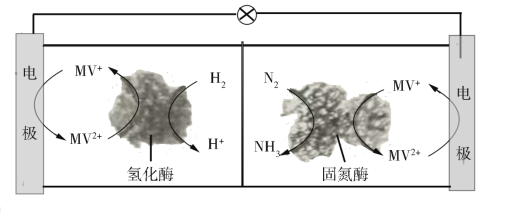
该电池工作时,正极的电极反应为___。中间所用的交换膜应该为___(填“阳离子交换膜”或“阴离子交换膜”或“质子交换膜”)。相比现有工业合成氨,该方法的优点是:___。(任写一条)
-
工业上可采用CH3OH CO+2H2的方法来制取高纯度的CO和H2。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。下图为计算机模拟的各步反应的能量变化示意图,下列说法正确的是
CO+2H2的方法来制取高纯度的CO和H2。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。下图为计算机模拟的各步反应的能量变化示意图,下列说法正确的是
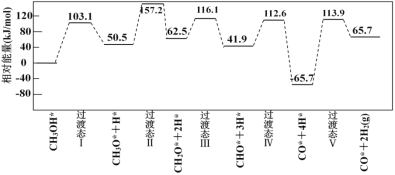
A.CH3OH脱氢反应的第一步历程为CH3OH* =CH3*+OH*
B.该历程中最大活化能E正=179.6 kJ•mol-1
C.该历程中,放热最多的步骤的化学方程式为CHO*+ 4H* =CO*+2H2(g)
D.CH3OH* = CO*+2H2(g) △H=65.7 kJ•mol-1
-
工业上可采用CH3OH CO+2H2的方法来制取高纯度的CO和H2。我国科研人员通过计算机模拟,研究了在钯基催化剂表面甲醇制氢的反应历程如图所示,其中吸附在钯催化剂表面上的物种用标注。下列说法正确的是( )
CO+2H2的方法来制取高纯度的CO和H2。我国科研人员通过计算机模拟,研究了在钯基催化剂表面甲醇制氢的反应历程如图所示,其中吸附在钯催化剂表面上的物种用标注。下列说法正确的是( )
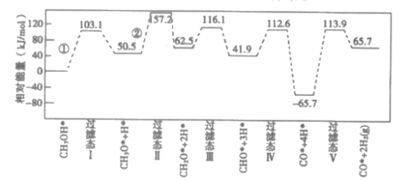
已知:甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ:CH3OH*→CH3O*+H* Ea=+103.1 kJ·mol-1
方式Ⅱ:CH3OH*→CH3*+OH* Eb=+249.3 kJ·mol-1
A.CH3OH*→CO*+2H2(g)的ΔH>0
B.①②都为O-H键的断裂过程
C.由活化能E值推测,甲醇裂解过程主要历经的方式应为Ⅱ
D.放热最多阶段的化学方程式为CHO*+3H*→CO*+4H*
-
科研人员利用Cu/ZnO作催化剂,在光照条件下实现了CO2和H2合成CH3OH,该反应历程示意图如下。
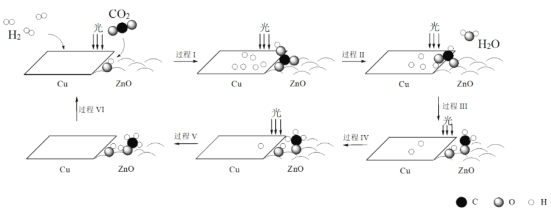
下列说法不正确的是
A.过程I中ZnO表面上进行CO2的吸附与转化
B.过程II中存在极性键的断裂与形成
C.过程V中生成CH3OH时吸收能量
D.总反应的化学方程式是CO2 + 3H2 CH3OH + H2O
CH3OH + H2O
-
科研人员利用Cu/ZnO作催化剂,在光照条件下实现了CO2和H2合成CH3OH,该反应历程示意图如下。
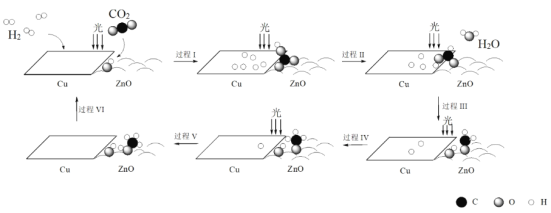
下列说法不正确的是
A.过程I中ZnO表面上进行CO2的吸附与转化
B.过程II中存在极性键的断裂与形成
C.过程V中生成CH3OH时吸收能量
D.总反应的化学方程式是CO2 + 3H2 CH3OH + H2O
CH3OH + H2O
-
二甲胺是农药螟铃畏的重要中间体,在一定温度压强及催化剂条件下由氨与甲醇作用而制得,反应原理为:2CH3OH(g)+NH3(g)⇌CH3NHCH3(g)+2H2O(g)
已知:①CH3OH(g)+ O2(g)=CO2(g)+2H2O(g) ΔH=-1560.8 kJ/mol kJ·mol-1
O2(g)=CO2(g)+2H2O(g) ΔH=-1560.8 kJ/mol kJ·mol-1
②2NH3(g)+ O2(g)=N2(g)+3H2O(g) ΔH=-236.0 kJ·mol-1
O2(g)=N2(g)+3H2O(g) ΔH=-236.0 kJ·mol-1
③CH3NHCH3(g)+ O2(g)=2CO2(g)+
O2(g)=2CO2(g)+ H2O(g)+
H2O(g)+ N2(g) ΔH=-1872.6 kJ·mol-1
N2(g) ΔH=-1872.6 kJ·mol-1
(1)写出CH3OH(g)与NH3(g)转化为CH3NHCH3(g)和H2O(g)的热化学方程式是____________。
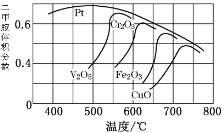
(2)不同的催化剂对二甲胺合成催化效率不同(如图所示),则最合适的催化剂及温度是_____________
(3)一定条件下,原料气中n(CH3OH)/n(NH3)比值和温度对NH3平衡转化率影响的实验数据如图:
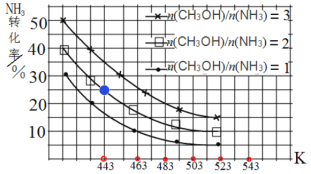
①温度为443 K时,在1 L反应容器中投入4 mol NH3和8 mol CH3OH进行反应,试计算达到平衡时CH3NHCH3(g)浓度为_________mol∙L-1,该温度下化学平衡常数为_____________
②结合图中数据,归纳 NH3平衡转化率受外界条件影响的变化规律:a:_______b:________
(4)二甲胺水溶液类似于氨水,呈碱性;则二甲胺在水中的电离方程式为__________
(5)常温下,将二甲胺和盐酸等体积混合,两种溶液的物质的量浓度和混合溶液的pH如表所示:
| 实验编号 | 二甲胺浓度(mol.L-1) | 盐酸浓度(mol.L-1) | 混合后溶液的PH |
| 甲 | 0.1 | 0.1 | a |
| 乙 | 0.15 | 0.1 | 8 |
| 丙 | 0.2 | 0.1 | 10 |
①实验甲中,a______(填“大于”、“小于”或“等于”)7
②实验丙混合后的溶液中离子浓度大小关系为______________
-
炭黑是雾霾中的重要颗粒物之一,研究发现它可以活化氧分子生成活化氧,活化氧可以快速氧化二氧化硫。活化过程的能量变化模拟计算结果如图所示,下列说法错误的是
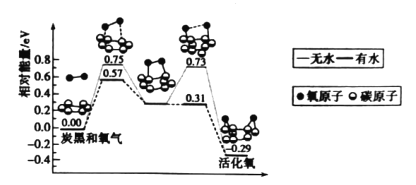
A.炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
B.氧分子的活化包括O-O键的断裂与C-O键的生成
C.水可使氧分子活化反应的活化能降低0.42 eV
D.每活化一个氧分子放出0.29 eV的能量
-
自然界中时刻存在着氮气的转化。实现氮气按照一定方向转化一直是科学领域研究的重要课题,如图为N2分子在催化剂的作用下发生的一系列转化示意图。下列叙述正确的是( )
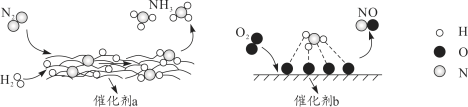
A.N2→NH3,NH3→NO均属于氮的固定
B.在催化剂a作用下,N2发生了氧化反应
C.催化剂a、b表面均发生了极性共价键的断裂
D.使用催化剂a、b均可以提高单位时间内生成物的产量
-
自然界中时刻存在着氮的转化。实现氮按照一定方向转化一直是科学领域研究的重要课题,如图为N2分子在催化剂的作用下发生的一系列转化示意图:

下列叙述正确的是
A.N2 NH3,NH3
NH3,NH3 NO均属于氮的固定
NO均属于氮的固定
B.催化剂a作用下氮原子发生了氧化反应
C.催化剂a、b表面均发生了极性共价键的断裂
D.使用催化剂a、b均可以提高单位时间内生成物的产量