-
镁、铝、硅、银、铁的单质及其化合物在建筑业、飞机制造业、电子工业和石油化工等方面应用广泛。回答下列问题:
(1)Fe3+价层电子的轨道表达式(电子排布图)为__。
(2)晶体硅属于______晶体。硅能形成多种化合物(如SiH4、Si2H4等),SiH4的分子的立体构型为____;Si2H4分子中含有的σ键和π键的数目之比为____。
有机物种类繁多的原因其中之一就是因为碳原子之间既可以形成单键又可以形成双键和三键,Si和Ge与C是同主族价电子数相同,但是Si和Ge就难形成双键或三键,原因是________
(3)Mg、Al、Si的第一电离能由大到小顺序:______________
(4)Ca和Fe属于同一周期,且核外最外层电子构型相同,但金属Ca的熔点、沸点等都比金属Fe低,原因是______。
(5)Ag晶体的堆积方式为面心立方最密堆积(如图所示),晶胞中Ag原子的配位数为______;设Ag原子半径为rcm,阿伏加德罗常数的值用NA表示,则Ag晶体的密度为______g·cm-3(写出表达式)。

-
有机玻璃(聚甲基丙烯酸甲酯、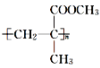 )广泛应用于商业、轻工业、建筑、化工甚至人工角膜等方面,下面是工业上由丙酮为起始反应物合成有机玻璃的一种路线图,请回答下列问题:
)广泛应用于商业、轻工业、建筑、化工甚至人工角膜等方面,下面是工业上由丙酮为起始反应物合成有机玻璃的一种路线图,请回答下列问题:

(1)A的化学式为__________;B的名称是_______。
(2)反应①、②的反应类型分别是____________、___________。
(3)下列有关 的说法错误的是________(填字母)。
的说法错误的是________(填字母)。
a.分子中所有碳原子均在同一平面上 b.能使溴水、酸性KMnO4溶液褪色
c.与丙酸互为同系物 d.能与新制的Cu(OH)2悬浊液反应
(4)写出反应④的化学方程式:_____________。
(5)C有多种同分异构体,其中满足下列条件的有______种(不包含C),在这些同分异构体中,核磁共振氢谱有3组峰的物质的结构简式为_______________。
①能发生水解反应但不能发生银镜反应; ②能使溴的CCl4溶液褪色。
-
钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从钛白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪(Sc2O3)的一种流程如下:
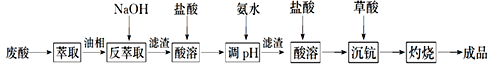
回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是______________________________。
(2)先加入氨水调节pH=3,过滤,滤渣主要成分是__________;再向滤液加入氨水调节pH=6,滤液中Sc3+的浓度为_____________。(已知:Ksp[Mn(OH)2]=1.9×10-13、Ksp[Fe(OH)3]=2.6×10-39,Ksp[Sc(OH)3]=9.0×10-31)
(3)用草酸“沉钪”。25 ℃时pH=2的草酸溶液中 =__________(保留两位有效数字)。写出“沉钪”得到草酸钪的离子方程式__________________________________。[已知Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5]
=__________(保留两位有效数字)。写出“沉钪”得到草酸钪的离子方程式__________________________________。[已知Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5]
(4)草酸钪“灼烧”氧化的化学方程式为_____________________________。
(5)废酸中含钪量为15 mg·L-1,V L废酸最多可提取Sc2O3的质量为____________。
-
请阅读下列材料,回答下列小题
将一定比例的三氧化硫和水混合可制得硫酸。硫酸是一种重要的化工原料,用途十分广泛,除用于化学工业外,还非常广泛应用于肥料、非碱性清洁剂、护肤品、油漆添加剂与炸药的制造等方面。
1.关于浓硫酸的说法正确的是
A.易挥发
B.见光分解
C.密度比水的小
D.常温下能使铝片钝化,浓硫酸作氧化剂
2.稀硫酸可以用于实验室制氢气,反应方程式为Zn+H2SO4=ZnSO4+H2↑,该反应的反应类型说法正确的是
A.化合反应 B.复分解反应 C.置换反应 D.分解反应
3.在其他条件不变的情况下,欲提高硫酸与锌反应产生氢气的速率,可以采用的措施有
A.选用颗粒更大的锌粒
B.升高反应温度
C.用98%浓硫酸来代替稀硫酸反应
D.加入硫酸钾溶液
4.下列反应中,生成物总能量高于反应物总能量的是
A.S+O2 SO2
SO2
B.CaO+H2O=Ca(OH)2
C.C+CO2 2CO
2CO
D.Zn+H2SO4=ZnSO4+H2↑
-
(18分)铁、铜等金属及其化合物在日常生活中应用广泛,回答下列问题。
(1)电子工业常用30%的FeCl3溶液腐蚀附在绝缘板上的铜箔制造印刷电路板,取其腐蚀后的废液,加 入一定量的铁粉后,若无固体剩余,则反应后的溶液中肯定有的离子是______________;若有红色固体,则反应后的溶液中肯定没有的离子是________,检验该离子的试剂为________。
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃-60℃,加入H2O2,反应一段时间后可制得硫酸铜,发生反应的化学方程式为:_____________________,
(3)实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾(FeSO4.7H2O),测定产品中绿矾含量的实验步骤:
a.称取5.7 g产品,溶解,配成250 mL溶液;
b.量取25 mL待测液于锥形瓶中;
c.用硫酸酸化的0.01 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液的体积为40 mL。
根据上述步骤回答下列问题:
①滴定时发生反应的离子方程式为(完成并配平离子反应方程式)

②用硫酸酸化的KMnO4溶液滴定至终点的标志是 _____。
③上述产品中FeSO4·7H2O的质量分数为 。
(4)铁氰化钾 K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6] 的混合溶液可用于太阳能电池的电解液,该太阳能电池的工作原理示意图如图所示,其中催化剂a为________极,电极反应式为_______________;

-
铝广泛应用于航空、建筑、汽车等行业,目前工业上采用电解氧化铝和冰晶石混合物的方法制取铝。回答下列问题:
(1)某同学写出了铝原子的4种不同状态的电子排布图:
A.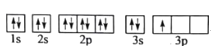
B.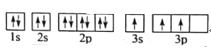
C.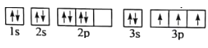
D.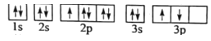
其中能量最低的是____(填字母),电子由状态C到状态B所得原子光谱为____光谱(填“发射”或“吸收”) ,状态D是铝的某种激发态,但该电子排布图有错误,主要是不符合_____。
(2)熔融态氯化铝可挥发出二聚分子Al2Cl6,其结构如图所示。
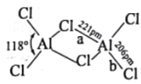
①a键的键能_____b键的键能(填“>”“<”或“=”),其理由是_______。
②Al2Cl6中铝原子的杂化方式为___;AlCl3的空间结构为______。
(3)冰晶石属于离子化合物,由Na+和AlF63−组成,在冰晶石的晶胞中,AlF63−占据的位置相当于氯化钠晶胞中Cl−的位置。
①冰晶石的化学式为_____,一个冰晶石晶胞中Na+的个数为_____。
②已知冰晶石的密度为2.95 g/cm3,则冰晶石晶胞的边长a=____pm(列出算式即可,阿伏加德罗常数值为6.02×1023)。
-
碳、 氮、磷、砷和硼的相关化合物在化工、医药、农药、材料等领域有着广泛的应用。锂、钠、铝、铁等金属在日常生活、工业生产中也占有举足轻重的地位,请回答下列问题:
(1)基态As原子的电子排布式为______________________;
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中B—N—B之间的夹角是___________________(填角度)。
(3)金属晶体的四种堆积如下图,金属钠的晶体堆积模型为___ (填字母)。
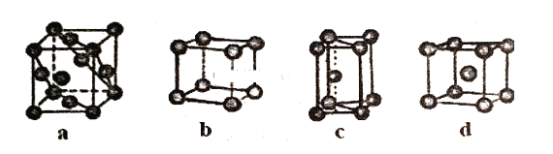
-
铁单质及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为:3FeS2+8O2 6SO2+Fe3O4,3 mol FeS2参加反应转移________mol电子。
6SO2+Fe3O4,3 mol FeS2参加反应转移________mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式________。
从腐蚀废液回收得到金属铜还需要的试剂为_________________________________。
(3)与明矾相似,硫酸铁也可用作絮凝剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是________。
(4)下表中,对陈述I、II的正确性及其有无因果关系的判断都正确的是____________。(填字母)
| 选项 | 陈述I | 陈述II | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | I对;II对;有 |
| B | 常温下铁与稀硫酸反应生成氢气 | 高温下氢气能还原氧化铁生成铁 | I对;II对;无 |
| C | 铁属于过渡金属元素 | 铁和铁的某些化合物可以用作催化剂 | I错;II对;无 |
| D | 铁在空气中表面生成致密氧化膜 | 可用铁罐储存运输浓硫酸、浓硝酸 | I对;II对;有 |
-
铁、铝、铜等金属及其化合物在日常生活中应用广泛,请回答下列问题:
(1)单质铁属于_______晶体。黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料,其中一个反应为3FeS2+8O2 6SO2+Fe3O4,氧化产物为_________,若有3molFeS2参加反应,转移_______mol电子。
6SO2+Fe3O4,氧化产物为_________,若有3molFeS2参加反应,转移_______mol电子。
(2)铝的价电子排布式为_________,明矾用作净水剂,其原理为_______________(用离子方程式表示)。
(3)金属Cu单独与氨水或单独与双氧水都不反应,但可与二者的混合溶液反应生成深蓝色溶液,Cu与氨水、双氧水反应的离子方程式_______________;
(4)铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160mL5mol•L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L氢气(标准状况),经检测溶液中无Fe3+,参加反应的铁粉的质量为_________。
-
铁单质及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料,其中发生的一个反应为3FeS2+8O2 6SO2+Fe3O4,若有3molFeS2参加反应,则转移__________mol电子。
6SO2+Fe3O4,若有3molFeS2参加反应,则转移__________mol电子。
(2)氯化铁溶液常用作印刷电路铜板的腐蚀剂,反应的离子方程式为__________。从腐蚀废液中回收金属铜需要的试剂是__________。
(3)与明矾相似,硫酸铁也可用于净水,其作用原理是____________(用离子方程式表示);在使用时发现硫酸铁并不能使酸性废水中悬浮物沉降除去,其原因是__________。
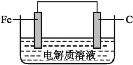
(4)钢铁的电化学腐蚀简单示意图如图所示,发生吸氧腐蚀时,负极名称为________;正极的电极反应式为________;
(5)铁红是一种红色颜料,其主要成分是Fe2O3。将一定量的铁红溶于160mL5mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L氢气(标准状况),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为__________。

 )广泛应用于商业、轻工业、建筑、化工甚至人工角膜等方面,下面是工业上由丙酮为起始反应物合成有机玻璃的一种路线图,请回答下列问题:
)广泛应用于商业、轻工业、建筑、化工甚至人工角膜等方面,下面是工业上由丙酮为起始反应物合成有机玻璃的一种路线图,请回答下列问题:








