-
铁单质及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为:3FeS2+8O2 6SO2+Fe3O4,3 mol FeS2参加反应转移________mol电子。
6SO2+Fe3O4,3 mol FeS2参加反应转移________mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式________。
从腐蚀废液回收得到金属铜还需要的试剂为_________________________________。
(3)与明矾相似,硫酸铁也可用作絮凝剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是________。
(4)下表中,对陈述I、II的正确性及其有无因果关系的判断都正确的是____________。(填字母)
| 选项 | 陈述I | 陈述II | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | I对;II对;有 |
| B | 常温下铁与稀硫酸反应生成氢气 | 高温下氢气能还原氧化铁生成铁 | I对;II对;无 |
| C | 铁属于过渡金属元素 | 铁和铁的某些化合物可以用作催化剂 | I错;II对;无 |
| D | 铁在空气中表面生成致密氧化膜 | 可用铁罐储存运输浓硫酸、浓硝酸 | I对;II对;有 |
-
铁单质及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料,其中发生的一个反应为3FeS2+8O2 6SO2+Fe3O4,若有3molFeS2参加反应,则转移__________mol电子。
6SO2+Fe3O4,若有3molFeS2参加反应,则转移__________mol电子。
(2)氯化铁溶液常用作印刷电路铜板的腐蚀剂,反应的离子方程式为__________。从腐蚀废液中回收金属铜需要的试剂是__________。
(3)与明矾相似,硫酸铁也可用于净水,其作用原理是____________(用离子方程式表示);在使用时发现硫酸铁并不能使酸性废水中悬浮物沉降除去,其原因是__________。
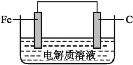
(4)钢铁的电化学腐蚀简单示意图如图所示,发生吸氧腐蚀时,负极名称为________;正极的电极反应式为________;
(5)铁红是一种红色颜料,其主要成分是Fe2O3。将一定量的铁红溶于160mL5mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L氢气(标准状况),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为__________。
-
铁、铝、铜等金属及其化合物在日常生活中应用广泛,请回答下列问题:
(1)单质铁属于_______晶体。黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料,其中一个反应为3FeS2+8O2 6SO2+Fe3O4,氧化产物为_________,若有3molFeS2参加反应,转移_______mol电子。
6SO2+Fe3O4,氧化产物为_________,若有3molFeS2参加反应,转移_______mol电子。
(2)铝的价电子排布式为_________,明矾用作净水剂,其原理为_______________(用离子方程式表示)。
(3)金属Cu单独与氨水或单独与双氧水都不反应,但可与二者的混合溶液反应生成深蓝色溶液,Cu与氨水、双氧水反应的离子方程式_______________;
(4)铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160mL5mol•L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L氢气(标准状况),经检测溶液中无Fe3+,参加反应的铁粉的质量为_________。
-
铁及铁的化合物在生活、生产中具有广泛应用,如亚铁氰化钾即K4[Fe(CN)6]是食盐中常用的抗结剂、铁基(氟掺杂镨氧铁砷化合物)是高温超导材料、“愚人金”是制备硫酸的主要矿物原料。请按要求回答下列问题。
(1)K4[Fe(CN)6]配合物中存在的作用力类型有__________________________(从“金属键”、“离子键”、“共价键”、“配位键”、“氢键”、“范德华力”中选填);其中CN-中各原子最外层均满足8电子稳定结构,其电子式为_____________,其中C原子的杂化形式是_________。
(2)铁基化合物中氟、氧、砷三种元素中电负性值由大到小的顺序是_____________(填元素符号)。其中氢化物(RH3)的某种性能(M)随R的核电荷数的变化趋势如图所示,则纵轴M可能表示为_____________________(从“沸点”、“稳定性”、“分子间作用力”、“R—H键能”中选填)。

(3)FeCl3晶体熔点为306℃,而FeF3晶体熔点高于1000℃,试解释两种化合物熔点差异较大的原因:____________________________________________。
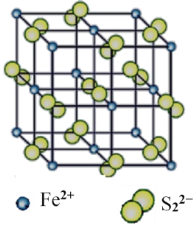
(4)“愚人金”是铁硫化合物,其晶体的晶胞如图所示。该晶体的化学式______________。
-
黄铁矿是生产硫酸的原料,其主要成分为FeS2。850〜950℃时,在空气中煅烧,发生反应
4FeS2 + 11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
试回答下列问题:
(1)含硫35%的黄铁矿样品(杂质不含硫),其FeS2的含量为_____________
(2)可用来表示该反应的化学反应速率的物质为_________________(填化学式)。
(3)某时刻测得生成SO2的速率为0.64 mol·L-1·s-1,则氧气减少的速率为_____________
(4)为了提高SO2的生成速率,下列措施可行的是______________(填选项字母)。
A.增加硫铁矿石的投入量 B.增加炉的高度
C.将硫铁矿石粉碎 D.升高温度
-
锌元素是重要的金属元素,锌及其化合物在生活、生产中有广泛应用,回答下列问题:
(1)ZnO和Al2O3的化学性质相似,写出ZnO和NaOH溶液反应的离子方程式为_____________。
(2)闪锌矿(主要成分为ZnS)、软锰矿(主要成分为MnO2)与稀硫酸共热时可以析出单质硫,该反应的化学方程式为_________________________。
(3)火法炼锌时在鼓风炉中加热到1 100 ~ 1 300 ℃,发生反应Ⅰ:
ZnO(s)+CO(g)= Zn(g)+CO2(g) ΔH=+198 mol•L-1。
①该反应的平衡常数表达式K=_________________。
②温度为T1时,反应Ⅰ的平衡常数为K1,则同温下反应Ⅱ:
 ZnO(s)+
ZnO(s)+ CO(g)=
CO(g)= Zn(g)+
Zn(g)+ CO2(g)的平衡常数K2=____________(用K1表示)。
CO2(g)的平衡常数K2=____________(用K1表示)。
③某温度时反应Ⅰ的平衡常数K=1.0 mol•L-1,起始时在容积固定的密闭鼓风炉中通入0.11 mol•L-1 CO(ZnO足量),达平衡时,CO的浓度为_____________mol•L-1 。
(4)粗铜电解精炼的废电解液中常含有Zn2+、Pb2+,向废电解液中加入Na2S溶液,当有PbS和ZnS沉淀时, =________________(已知:Ksp(PbS)=3.4×
=________________(已知:Ksp(PbS)=3.4× ,Ksp(ZnS)=1.6×
,Ksp(ZnS)=1.6× ) 。用平衡移动原理解释PbS难溶于水,却能溶于硝酸中_______________________________
) 。用平衡移动原理解释PbS难溶于水,却能溶于硝酸中_______________________________
-
金属钛(Ti)具有硬度大、熔点高、耐酸碱腐蚀的优点,被广泛用于航空航天、医疗卫生及日常生活中。以钛铁矿(主要成分为FeTiO3)为主要原料冶炼金属钛的生产工艺如图所示。
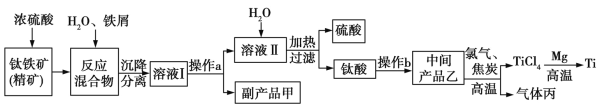
回答下列有关问题:
(1)钛铁矿(精矿)中加入浓硫酸除生成TiOSO4外,还生成水和另外一种硫酸盐,且反应前后Fe的化合价不变,则FeTiO3中Ti的化合价为____。
(2)上述流程图中加入“铁屑”的目的是___(填字母)。
A.防止Fe2+被氧化 B.与Fe3+反应
C.防止Fe2+水解 D.防止Fe3+水解
(3)溶液Ⅰ经“操作a”可得固体副产品甲,则操作a的名称为_______,副产品甲的化学式是_____。
(4)已知钛酸难溶于水,其化学式为H2TiO3。则溶液Ⅱ中加入水,加热时发生的化学方程式为_____。
(5)“操作b”为加热,则中间产品乙的化学式为______。
(6)一定条件下,利用气体丙与氢气可合成甲醇,该合成反应的化学方程式为____________,甲醇的电子式为______。
-
硼元素、钙元素、铜元素在化学战有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用.
(1)已知CaC2与水反应生成乙炔.请回答下列问题:
①将乙炔通入 [Cu(NH3)2]Cl溶液中生成Cu2C2红棕色沉淀, Cu+基态核外电子排布式为 ______ .
②CaC2中 与
与 互为等电子体. 1mol
互为等电子体. 1mol 中含有的π键数目为 ______ .
中含有的π键数目为 ______ .
③乙炔与氢氰酸反应可得丙烯睛(CH2=CHC=N),丙烯腈分子中碳原子轨道杂化类
型是 ______ ,构成丙烯腈元素中第一电离能最大的是 ______.
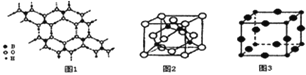
(2)硼酸 (H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子间通过氢健相连(如上图1),则1mol H3BO3的晶体中有 ______ mol氢键.硼酸溶于水生成弱电解质一水合硼酸B(OH)3·H2O,它电离生成少量[B(OH)4]-和H+,则[B(OH)4]-的空间构型为 ______
(3)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如上图2所示 黑点代表铜原子,空心圆代表M原子
黑点代表铜原子,空心圆代表M原子 .
.
 该晶体化学式为 ______ .
该晶体化学式为 ______ .
 已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于 ______
已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于 ______  填“离子”、“共价”
填“离子”、“共价” 化合物.
化合物.
(4)Cu3N的晶胞结构如右上图3, N3-的配位数为 ______ ,Cu+半径为apm,N3-半径为bpm,Cu3N的密度为 ______ g·cm-3。(阿伏加德罗常数用 表示)
表示)
-
铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)如图是自来水表的常见安装方式,发生腐蚀过程中,电流从___(填“接头流向水表”或“水表流向接头”)。

(2)某二次电池放电的电池反应为2Fe+O2+2H2O=2Fe(OH)2。反应结束时,电池的负极的质量___(“减小”“不变”或“增加”),该电池的正极反应式为___。
(3)有如图装置:
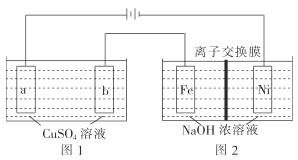
①图1中,用惰性电极电解过程中的实验数据如图,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中图1装置中产生气体的总体积(标准状况)。电解过程中转移n(e-)=0.4mol,b电极的实验现象为___;Q点时,a电极收集到的气体体积为___。

②图2中,装置通电后,溶液仍然保持澄清,铁电极附近呈紫红色(已知FeO42-在水溶液中呈紫红色),Fe电极上发生的电极反应式为___。
-
铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)如图是自来水表的常见安装方式,发生腐蚀过程中,电流从_______ (填“接头流向水表”或“水表流向接头”)。

(2)某二次电池放电的电池反应为2Fe+O2+2H2O = 2Fe(OH)2。反应结束时,电极a的质量__________(填“减小”“不变”或“增加”),该电池的正极反应式为____________。
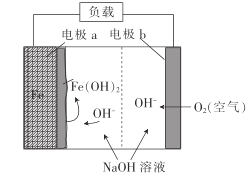
(3)有如图装置:
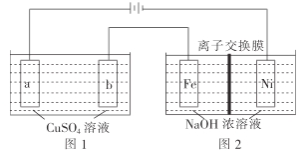
①图1中,用惰性电极电解过程中的实验数据如图,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中图1装置中产生气体的总体积(标准状况)。电解过程中转移n(e-)=0.4mol,b电极的实验现象为_______________;Q点时,a电极收集到的气体体积为________________。
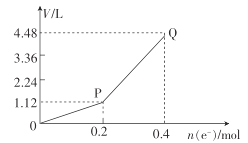
②图2中,装置通电后,溶液仍然保持澄清,铁电极附近呈紫红色(已知FeO42-在水溶液中呈紫红色),Fe电极上发生的电极反应式为___________。
6SO2+Fe3O4,若有3molFeS2参加反应,则转移__________mol电子。











