-
黄铁矿是生产硫酸的原料,其主要成分为FeS2。850〜950℃时,在空气中煅烧,发生反应
4FeS2 + 11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
试回答下列问题:
(1)含硫35%的黄铁矿样品(杂质不含硫),其FeS2的含量为_____________
(2)可用来表示该反应的化学反应速率的物质为_________________(填化学式)。
(3)某时刻测得生成SO2的速率为0.64 mol·L-1·s-1,则氧气减少的速率为_____________
(4)为了提高SO2的生成速率,下列措施可行的是______________(填选项字母)。
A.增加硫铁矿石的投入量 B.增加炉的高度
C.将硫铁矿石粉碎 D.升高温度
-
硫铁矿又称黄铁矿,是生产硫酸的原料,其主要成分为FeS2。850℃~950℃时,空气中煅烧,可能发生下列反应(设空气中N2与O2体积比为4:1):4FeS2+11O2→2Fe2O3+8SO2
(1)含硫35%的硫铁矿样品(杂质不含硫),其FeS2的含量为 。
(2)设1t纯净的FeS2完全反应,产生标准状况下SO2 m3。
(3)为使FeS2煅烧完全生成Fe2O3,工业上使用过量空气,当空气过量20%时,所得炉气中SO2的体积分数为多少?
-
煅烧硫铁矿石(主要成分是FeS2),可获得制取硫酸所需的SO2,反应方程式为:
4FeS2 + 11O2 = 2Fe2O3 + 8SO2,为了提高SO2的生成速率,下列措施可行的 ( )
A.增加硫铁矿石的投入量 B.增加炉的高度
C.降低温度 D.升高温度
-
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe2O3。
(1)将0.050mol SO2(g)和0.030mol O2(g)放入容积为1L的密闭容器中,反应:
2SO2(g)+O2(g) 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol·L-1。计算该条件下反应的平衡常数K和SO2的平衡转化率________、________。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol·L-1。计算该条件下反应的平衡常数K和SO2的平衡转化率________、________。

(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有________(填字母序号,多选倒扣分)。
A.升高温度 B.降低温度
C.增大压强 D.加入催化剂
E.移出氧气
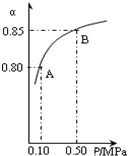
(3)某温度下,上述反应中SO2的平衡转化率(α)与体系总压强(p)的关系如右图所示。判断:平衡状态由A变到B时,平衡常数K(A)______K(B)(填“>”、“<”或“=”)。
-
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe2O3.
(1)将0.050mol SO2(g)和0.030mol O2(g)放入容积为1L的密闭容器中,反应:2SO2(g)+O2(g)⇌2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol•L-1.计算该条件下反应的平衡常数K和SO2的平衡转化率______、______(写出计算过程).
(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有______(填字母序号,多选倒扣分).
A.升高温度 B.降低温度 C.增大压强 D.加入催化剂 E.移出氧气
(3)某温度下,上述反应中SO2的平衡转化率(α)与体系总压强(p)的关系如右图所示.判断:平衡状态由A变到B时,平衡常数K(A)______K(B)(填“>”、“<”或“=”).
-
(14分)某研究小组模拟工业上以黄铁矿为原料制备硫酸的第一步反应:
4FeS2+11O2 2Fe2O3+8SO2,进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
2Fe2O3+8SO2,进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。

实验步骤:称取研细的样品4.000g放入上图b装置中,然后在空气中进行煅烧。为测定未反应高锰酸钾的量(假设其溶液体积保持不变),实验完成后取出d中溶液10mL置于锥形瓶里,用0.1000mol/L草酸(H2C2O4)标准溶液进行滴定。
(已知:5SO2 + 2KMnO4 + 2H2O == K2SO4 + 2MnSO4 + 2H2SO4 )
请回答下列问题:
(1)称量样品质量能否用托盘天平________(填“能”或“不能”);
(2)装置a的作用是________ ________;
(3)上述反应结束后,仍需通一段时间的空气,其目的是 ;
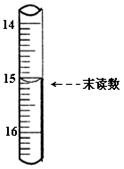
(4)滴定时,发生反应的离子方程式为________,已知滴定管初读数为0.10mL,末读数如上图所示,消耗草酸溶液的体积为 ________mL;
(5)该样品中FeS2的纯度为;
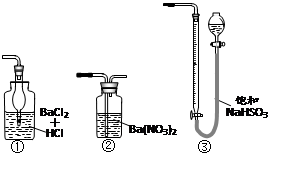
(6)若用下图装置替代上述实验装置d,同样可以达到实验目的的是________。(填编号)
-
(12分)黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4。
(1)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应:2SO2(g)+O2(g) 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol/L。计算该条件下反应的平衡常数K为 SO2的平衡转化率为 若将0.10molSO2(g)和0.060molO2(g)放入容积为1L的密闭容器中在该温度下达平衡,与前者比较,SO2的平衡转化率 SO2的体积分数 (填增大、减小、不变、无法确定)
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol/L。计算该条件下反应的平衡常数K为 SO2的平衡转化率为 若将0.10molSO2(g)和0.060molO2(g)放入容积为1L的密闭容器中在该温度下达平衡,与前者比较,SO2的平衡转化率 SO2的体积分数 (填增大、减小、不变、无法确定)
(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有 (填字母)
A.升高温度 B.降低温度
C.增大压强 D.减小压强
E.加入催化剂 G.移出氧气
(3)SO2尾气用饱和Na2SO3溶液吸收可得到更重要的化工原料,反应的化学方程式为
-
(12分)黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2 和Fe3O4。
(1)将0.5molSO2(g)和0.48molO2(g)放入容积为1L的密闭容器中,反应: 2SO2(g)+O2(g) 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.48mol/L。则该条件下SO2的平衡转化率为 。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.48mol/L。则该条件下SO2的平衡转化率为 。
(2)若锻烧12gFeS2产生的SO2全部转化为SO3气体时放出19.66kJ热量,产生的SO3与水全部化合生成H2SO4,放出26.06kJ热量,写出SO3气体转化为H2SO4的热化学方程式: 。
(3)将黄铁矿的煅烧产物Fe3O4溶于稀H2SO4后,加入铁粉,可制备FeSO4。酸溶过程中需保持溶液足够酸性,其目的是 。
(4)从吸收塔排出的尾气中SO2先用足量氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐,写出有关反应的化学方程式: 、 。
SO2既可作为生产硫酸的原料循环再利用,也可用于海水提溴过程中吸收潮湿空气中的Br2,则SO2吸收Br2的离子方程式是 。
-
(12分)黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4。
(1)将0.5molSO2(g)和0.48molO2(g)放入容积为1L的密闭容器中,反应:2SO2(g)+O2(g) 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.48mol/L。则该条件下SO2的平衡转化率为 。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.48mol/L。则该条件下SO2的平衡转化率为 。
(2)若锻烧12gFeS2产生的SO2全部转化为SO3气体时放出19.66kJ热量,产生的SO3与水全部化合生成H2SO4,放出26.06kJ热量,写出SO3气体转化为H2SO4的热化学方程式: 。
(3)将黄铁矿的煅烧产物Fe3O4溶于稀H2SO4后,加入铁粉,可制备FeSO4。酸溶过程中需保持溶液足够酸性,其目的是 。
(4)从吸收塔排出的尾气中SO2先用足量氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐,写出有关反应的化学方程式: 、 。
SO2既可作为生产硫酸的原料循环再利用,也可用于海水提溴过程中吸收潮湿空气中的Br2,则SO2吸收Br2的离子方程式是 。
-
黄铁矿(主要成分 FeS2)是工业制硫酸的主要原料,暴露在空气中会被缓慢氧化,其氧化过程如下图所示。
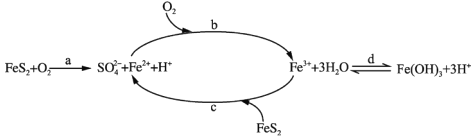
下列有关说法不正确的是
A. 为了验证b 溶液中含 Fe2+,可选用 KSCN 溶液和氯水
B. 氧化过程会产生较多酸性废水破坏矿区生态环境
C. 取 10mlb 溶液测定其成分,通入标准状况下Cl222.4ml 恰好完全反应。然后调节 pH,使溶液中的铁元算全部转化为沉淀,经过滤、洗涤、灼烧,冷却后称重,得固体质量为 0.32g,则溶液中 c(Fe3+)=0.2mol·L-1
D. 现有一含有 FeCl2和 FeCl3的混合样品,采用一定方法测得 n(Fe): n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为 10%。
2Fe2O3+8SO2





