-
下面是我们熟悉的物质:①O2②金刚石③NaBr ④H2SO4⑤Na2CO3⑥NH4Cl
⑦NaHSO4⑧Ne ⑨Na2O2⑩NaOH
(1)这些物质中,只含有共价键的是______________;只含有离子键的是______________;不存在化学键的______________;
(2)属于共价化合物的是______________;
(3)将NaHSO4溶于水,破坏了NaHSO4中的_______,写出电离方程式______________;NaHSO4熔融状态下电离,破坏了___________键,写成电离方程式
______________________。
高二化学填空题中等难度题查看答案及解析
-
下列物质的水溶液因水解而呈酸性的是
A. H2SO4 B. NaHSO4 C. NH3 D. NH4Cl
高二化学单选题中等难度题查看答案及解析
-
下列物质的水溶液,由于水解而呈酸性的是( )
A. NaCl B. Na2CO3 C. NaHSO4 D. NH4Cl
高二化学单选题简单题查看答案及解析
-
I.下列是中学化学中熟悉的物质,请用序号完成下列问题
①O2②Na2O2③NH4Cl ④HCl ⑤NaOH ⑥CaCl2⑦氦气
(1)这些物质中,只含共价键的是__________________。只含离子键的是__________________。既含共价键又含离子键的是__________________。
(2)属于离子化合物的是_____________。
II.(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是__________(填“吸热”或“放热”)反应,NO2和CO的总能量____________(填“大于”、“小于”或“等于”)CO2和NO的总能量。
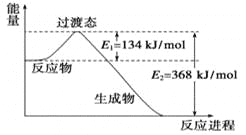
(2)已知拆开1molH﹣H键、1mol I﹣I、1mol H﹣I键分别需要吸收的能量为436kJ、151kJ、299kJ.则由氢气和碘反应生成1mol HI需要_____________(填“放出”或“吸收”)_____________kJ的热量.
高二化学填空题中等难度题查看答案及解析
-
下列物质属于共价化合物的是
A. Na2O2 B. H2 C. NH4Cl D. H2SO4
高二化学单选题中等难度题查看答案及解析
-
常温下,物质的量浓度均为0.1 mol·L-1的下列溶液:①Na2CO3溶液 ②NaOH溶液 ③NaHSO4溶液 ④NH4Cl溶液 ⑤NaNO3,溶液的pH由小到大的排列顺序是 ( )
A. ③ <④ <⑤ <① <② B. ④ <③ < ⑤ < ① <②
C. ④ <③ < ① <⑤ <② D. ① <④ < ③ < ⑤ <②
高二化学选择题中等难度题查看答案及解析
-
常温下,物质的量浓度均为0.1 mol·L-1的下列溶液:①Na2CO3溶液;②NaOH溶液;③NaHSO4溶液;④NH4Cl溶液;⑤NaNO3溶液;已知电离常数K(HSO4-)=1.2×10-2,K2(H2CO3)=5.6×10-11,K(NH3·H2O)=1.8×10-5,pH由小到大的排列顺序是
A.③<④<⑤<①<② B.④<③<⑤<①<②
C.④<③<①<⑤<② D.①<④<③<⑤<②
高二化学单选题中等难度题查看答案及解析
-
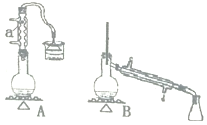
实验室用加热1一丁醇、浓H2SO4和溴化钠混合物的方法来制备1一溴丁烷,设计了如图所示的实验装置
其中的夹持仪器已省略
。
已知:H2SO4+NaBr=NaHSO4+HBr, H2SO4(浓)+2HBr=Br2+SO2↑+2H2O
请回答下列问题:
(1)仪器a的名称为______。
(2)制备操作中,加入的浓硫酸事先要进行稀释,其目的是______
填选项字母
。
减少副产物烯和醚的生成
减少
的生成
水是反应的催化剂
(3)写出此实验制1一溴丁烷的总化学方程式______。
(4)有同学拟通过红外光谱仪鉴定所得产物中是否含有“
”,来确定副产物中是否存在丁醚
请评价该同学设计的鉴定方案是否合理?理由是______。
(5)为了进一步提纯1一溴丁烷,该小组同学查得相关有机物的有关数据如表:
物质
熔点
沸点
1一丁醇
1一溴丁烷
丁醚
1一丁烯
则用B装置完成此提纯实验时;,实验中要迅速升高温度至______收集所得馏分。
(6)若实验中所取1一丁醇、NaBr分别为
、
,浓硫酸
,蒸出的粗产物经洗涤,干燥后再次蒸馏得到
一溴丁烷,则1一溴丁烷的产率是______
保留2位有效数字
。
高二化学实验题中等难度题查看答案及解析
-
实验室制备溴乙烷(C2H5Br)的方法为:
NaBr + H2SO4 = NaHSO4 + HBr
C2H5OH + HBr
C2H5Br + H2O
其中可能会发生副反应:
2HBr + H2SO4(浓) = Br2 ↑+ SO2↑ + 2H2O
制取的装置和步骤如图(已知溴乙烷的沸点38.4℃,不溶于水):
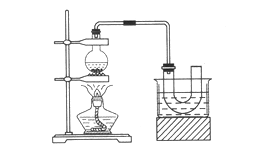
①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;
②在圆底烧瓶中加入10 mL 95%乙醇、28 mL 78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热.使其充分反应.
请根据信息回答下列问题:
(1)反应时若温度过高,可看到有红棕色气体产生,该气体分子式为___________,同时生成的无色气体分子式为________________。
(2)为了更好的控制温度,除用图示的小火加热外,更好的加热方式为________。
(3)反应结束后,U形管内粗制的C2H5Br呈棕黄色。为了除去粗产品中的杂质,可以选择下列试剂中的________________________(填序号)。
A.NaOH溶液 B.H2O C.Na2SO3溶液 D.CCl4
要进一步制得纯净的C2H5Br,可用水洗,然后加入无水CaCl2,再进行__________(填操作名称)。
(4)下列几项实验步骤,为了检验溴乙烷中溴元素,取出少量溴乙烷产品,而后正确的操作顺序是:___________________(填代号)。
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH水溶液;⑤冷却
A. ④①⑤③② B. ④③①⑤② C. ④③②①⑤ D. ④②①③⑤
高二化学实验题中等难度题查看答案及解析
-
下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是
A. NaAlO2和H2SO4 B. AlCl3和NaOH
C. NaHSO4和Ba(OH)2 D. Na2CO3和H2SO4
高二化学单选题中等难度题查看答案及解析