-
某二元弱酸(简写为H2B)溶液,按下式发生一级和二级电离:
H2B H++HB-
H++HB-
HB- H++B2-
H++B2-
已知相同浓度时的电离度a(H2B)>>a(HB-),现有下列四种溶液:
①0.01mol•L-1的H2B溶液
②0.01mol•L-1的NaHB溶液
③0.02mol•L-1的HCl溶液与0.04mol•L-1的NaHB溶液等体积混合后的溶液
④0.02mol•LL-1的NaOH溶液与0.02mol•L-1的NaHB溶液等体积混合后的溶液
下列说法错误的是( )
A.溶液④一定显碱性 B.c(H2B)最大的是③
C.c(B2-)最小的是① D.c(H+)最大的是③
-
某二元弱酸(简写为H2A)溶液,按下式发生一级或二级电离:
H2A H++HA-,HA-
H++HA-,HA- H++A2-
H++A2-
已知相同浓度时的电离度α(H2A)>α(HA-),设有下列四种溶液:
A.0.01 mol·L-1的H2A溶液
B.0.01 mol·L-1的NaHA溶液
C.0.02 mol·L-1的HCl与0.04 mol·L-1的NaHA溶液等体积混合液
D.0.02 mol·L-1的NaOH与0.02 mol·L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号):
(1)c(H+)最大的是_______________,最小的是_______________。
(2)c(H2A)最大的是_______________,最小的是_______________。
(3)c(A2-)最大的是_______________,最小的是_______________。
-
某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A⇌H++HA-;HA-⇌H++A2-.已知相同浓度时的电高度a(H2A)>d(HA-),设有下列四种溶液:
A.0.01mol.L-1的H2A溶液
B.0.01mol.L-1的NaHA溶液
C.0.01mol.L-1的HCl与0.04mol.L-1的NAHA溶液等体积混合液
D.0.02mol.L-1的NaOH与0.02mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号)
(1)[H+]最大的是______,最小的是______.
(2)[H2A]最大的是______,最小的是______.
(3)[A2-]最大的是______,最小的是______.
-
已知H2B在水溶液中存在以下电离:
一级电离:H2B H++HB-,二级电离:HB-
H++HB-,二级电离:HB- H++B2-
H++B2-
请回答以下问题:
(1)NaHB溶液______(填“呈酸性”、“呈碱性”或“无法确定”),原因是______.
(2)若0.1mol•L-1的H2B溶液在某温度下的pH=3,c(B2-)=1×10-6mol•L-1,则H2B的一级电离的电离度为______.
(3)某温度下,在0.1mol•L-1的NaHB溶液中,以下关系一定不正确的是______
A.c(H+)•c(OH-)=1×10-14
B.pH>1
C.c(OH-)=2c(H2B)+c(HB-)+c(H+)
D.c(Na+)=0.1mol•L-1≥c(B2-)
(4)某温度下,FeB(s) Fe2+(aq)+B2-(aq)的平衡常数表达式为KSP=c(Fe2+)•c(B2-),FeB在水中的沉淀溶解平衡曲线如图所示.下列说法错误的是______
Fe2+(aq)+B2-(aq)的平衡常数表达式为KSP=c(Fe2+)•c(B2-),FeB在水中的沉淀溶解平衡曲线如图所示.下列说法错误的是______
A.a点对应的KSP等于b点对应的KSP
B.d点无沉淀生成
C.可以通过升温实现由c点变到a点
D.此温度下,KSP=4×10-18.

-
已知H2B在水溶液中存在以下电离:
一级电离:H2B H++HB-,二级电离:HB-
H++HB-,二级电离:HB- H++B2-
H++B2-
请回答以下问题:
(1)NaHB溶液______(填“呈酸性”、“呈碱性”或“无法确定”),原因是______.
(2)若0.1mol•L-1的H2B溶液在某温度下的pH=3,c(B2-)=1×10-6mol•L-1,则H2B的一级电离的电离度为______.
(3)某温度下,在0.1mol•L-1的NaHB溶液中,以下关系一定不正确的是______
A.c(H+)•c(OH-)=1×10-14
B.pH>1
C.c(OH-)=2c(H2B)+c(HB-)+c(H+)
D.c(Na+)=0.1mol•L-1≥c(B2-)
(4)某温度下,FeB(s) Fe2+(aq)+B2-(aq)的平衡常数表达式为KSP=c(Fe2+)•c(B2-),FeB在水中的沉淀溶解平衡曲线如图所示.下列说法错误的是______
Fe2+(aq)+B2-(aq)的平衡常数表达式为KSP=c(Fe2+)•c(B2-),FeB在水中的沉淀溶解平衡曲线如图所示.下列说法错误的是______
A.a点对应的KSP等于b点对应的KSP
B.d点无沉淀生成
C.可以通过升温实现由c点变到a点
D.此温度下,KSP=4×10-18.

-
已知酸H2B在水溶液中存在下列关系:①H2B H++HB- ②HB-
H++HB- ②HB- H++B2-,关于该酸对应的酸式盐NaHB的溶液,下列说法中一定正确的是( )
H++B2-,关于该酸对应的酸式盐NaHB的溶液,下列说法中一定正确的是( )
A.NaHB属于弱电解质
B.溶液中的离子浓度[Na+]>[HB-]>[H+]>[OH-]
C.[Na+]=[HB-]+[B2-]+[H2B]
D.NaHB和NaOH溶液反应的离子方程式为H++OH-=H2O
-
已知某酸H2B在水溶液中存在下列关系:①H2B H++HB-,②HB-
H++HB-,②HB- H++B2-.关于该酸对应的酸式盐NaHB的溶液,下列说法中,一定正确的是( )
H++B2-.关于该酸对应的酸式盐NaHB的溶液,下列说法中,一定正确的是( )
A.NaHB属于弱电解质
B.溶液中的离子浓度c(Na+)>c(HB-)>c(H+)>c(OH-)
C.c(Na+)=c(HB-)+c(B2-)+c(H2B)
D.NaHB和NaOH溶液反应的离子方程式为H++OH-===H2O
-
回答下列问题:
(1)某二元酸(分子式用H2B表示)在水中的电离方程式是:H2B===H++HB-;HB- H++B2-。在0.1 mol/L的Na2B溶液中,下列粒子浓度关系式正确的是________。
H++B2-。在0.1 mol/L的Na2B溶液中,下列粒子浓度关系式正确的是________。
A.c(B2-)+c(HB-)=0.1 mol/L
B.c(B2-)+c(HB-)+c(H2B)= c(Na+)
c(Na+)
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
(2)下表为几种酸的电离平衡常数
| CH3COOH | H2CO3 | H2S |
| 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 |
则pH相同的CH3COONa、Na2CO3、NaHS溶液物质的量浓度由大到小的顺序为________________,少量CO2与NaHS反应的离子方程式为______________。
-
25℃时,向0.10mol·L-1的H2C2O4(二元弱酸)溶液中滴加NaOH溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法不正确的是
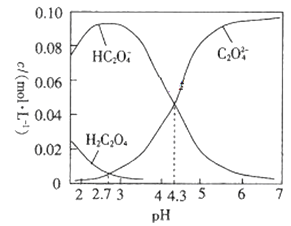
A. 25℃时H2C2O4的一级电离常数为Ka1=10‑4.3
B. pH=2.7的溶液中:c(H2C2O4)=c(C2O42-)
C. pH=7的溶液中:c(Na+)>2c(C2O42-)
D. 滴加NaOH溶液的过程中始终存在:c(OH-)+2c(C2O42-)+c(HC2O4-)=c(Na+)+c(H+)
-
25℃时,向0.10mol·L-1的H2C2O4(二元弱酸)溶液中滴加NaOH溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法不正确的是
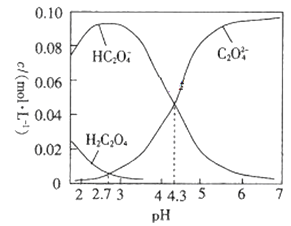
A. 25℃时H2C2O4的一级电离常数为Ka1=10‑4.3
B. pH=2.7的溶液中:c(H2C2O4)=c(C2O42-)
C. pH=7的溶液中:c(Na+)>2c(C2O42-)
D. 滴加NaOH溶液的过程中始终存在:c(OH-)+2c(C2O42-)+c(HC2O4-)=c(Na+)+c(H+)
H++HB-
H++B2-



