-
联氨(N2H4)可作火箭的燃料,燃烧时反应为2N2H4+2NO2=3N2+4H2O,下列说法错误的是( )
A.此反应是氧化还原反应
B.反应瞬间产生大量高温气体,推动火箭飞行
C.N2H4的摩尔质量为32g/mol
D.此反应中N2H4作氧化剂
高二化学单选题中等难度题查看答案及解析
-
肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知:N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ/mol,2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g) △H=-1 135.7kJ/mol;下列说法正确的是( )
A.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-1 068 kJ/mol
B.肼是与氨类似的弱碱,它易溶于水,其电离方程式:N2H4+H2O═N2H5++OH-
C.铂做电极,以KOH溶液为电解质溶液的肼--空气燃料电池,放电时的负极反应式:N2H4-4e-+4OH-=N2+4H2O
D.铂做电极,以KOH溶液为电解质溶液的肼--空气燃料电池,工作一段时间后,KOH溶液的pH将增大
高二化学选择题简单题查看答案及解析
-
肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知:N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g)△H=-1 135.7kJ/mol;下列说法正确的是( )
A.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-1 068 kJ/mol
B.肼是与氨类似的弱碱,它易溶于水,其电离方程式:N2H4+H2O═N2H5++OH-
C.铂做电极,以KOH溶液为电解质溶液的肼--空气燃料电池,放电时的负极反应式:N2H4-4e-+4OH-=N2+4H2O
D.铂做电极,以KOH溶液为电解质溶液的肼--空气燃料电池,工作一段时间后,KOH溶液的pH将增大高二化学选择题中等难度题查看答案及解析
-
肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。
已知:N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ/mol
2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g) △H=-1 135.7kJ/mol;
下列说法正确的是( )
A.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-1 068 kJ/mol
B.肼是与氨类似的弱碱,它易溶于水,其电离方程式:N2H4+H2O═N2H5++OH-
C.铂做电极,以KOH溶液为电解质溶液的肼--空气燃料电池,放电时的负极反应式:N2H4-4e-+4OH-=N2+4H2O
D.铂做电极,以KOH溶液为电解质溶液的肼--空气燃料电池,工作一段时间后,KOH溶液的pH将增大
高二化学选择题困难题查看答案及解析
-
(1)肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮的氢化物。
①肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g) ΔH=-1038.7 kJ·mol-1,若该反应中有4 mol N—H键断裂,则形成的π键有________mol。
②肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4晶体内不存在___(填标号)。
a.离子键 b.共价键 c.配位键 d.范德华力
(2)ⅥA族元素氧、硫、硒(Se)的化合物在研究和生产中有许多重要用途。请回答:
①H2Se的酸性比H2S________(填“强”或“弱”),SO32-离子的立体构型为________。
②H2SeO3的K1和K2分别为2.7×10-3和2.5×10-8,H2SeO4第一步几乎完全电离,K2为1.2×10-2,请根据结构与性质的关系解释:H2SeO4比H2SeO3酸性强的原因:__________。
(3)[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN)4]2-+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
①Zn2+基态核外电子排布式为___________________。
②与H2O分子互为等电子体的阴离子为________。
③)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为____________。
高二化学综合题简单题查看答案及解析
-
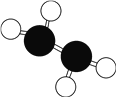
肼(N2H4)是火箭常用的高能燃料,常温下为液体,其球棍模型如图所示。肼能与双氧水发生反应N2H4+2H2O2=N2+4H2O,用NA表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,11.2 L N2中含有的电子总数为5NA
B.标准状况下,22.4 L N2H4中含有的原子总数为6NA
C.标准状况下,3.2 g N2H4中含有共价键的总数为0.6NA
D.若生成3.6 g H2O,则上述反应转移电子的数目为0.2NA
高二化学单选题中等难度题查看答案及解析
-
(1)肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:2N2H4(l)+N2O4(l)===3N2(g)+4H2O(g) ΔH1=-1048.9 kJ/mol
N2H4(l)+O2(g)=== N2(g)+2H2O(g) ΔH2=-534.2 kJ/mol
则N2(g)+2O2(g)===N2O4 (l) ΔH3=_________ kJ/mol
(2)化学反应中放出的热能(焓变,ΔH)与反应物和生成物在反应过程中断键和形成新键过程中吸收和放出能量的大小有关。
已知:H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ/mol,断裂1 mol H—H键吸收的能量为436 kJ,断裂1 mol Cl—Cl键吸收的能量为247 kJ,则形成1 mol H—Cl键放出的能量为________kJ。
(3).根据以下三个热化学方程式:
2H2S(g)+3O2(g)===2SO2(g)+2H2O(l) ΔH=-Q1 kJ/mol,
2H2S(g)+O2(g)===2S(s)+2H2O(l) ΔH=-Q2 kJ/mol,
2H2S(g)+O2(g)===2S(s)+2H2O(g) ΔH=-Q3 kJ/mol。
判断Q1、Q2、Q3三者大小关系_______>________>_______
高二化学综合题简单题查看答案及解析
-
(1)肼(N2H4)可作为
火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:2N2H4(l)+N2O4(l)===3N2(g)+4H2O(g) ΔH1=-1048.9 kJ/mol
N2H4(l)+O2(g)=== N2(g)+2H
2O(g) ΔH2=-534.2 kJ/mol
则N2(g)+2O2(g)===N2O4 (l) ΔH3
=_________ kJ/mol
(2)化学反应中放出的热能(焓变,ΔH)与反应物和生成物在反应过程中断键和形成新键过程中吸收和放出能量的大小有关。
已知:H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ/mol,断裂1 mol H—H键吸收的能量为436 kJ,断裂1 mol Cl—Cl键吸收的能量为247 kJ,则形成1 mol H—Cl键放出的能量为________kJ。
(3).根据以下三个热化学方程式:
2H2S(g)+3O2(g)===2SO2(g)+2H2O(l) ΔH=-Q1 kJ/mol,
2H2S(g)+O2(g)===2S(s)+2H2O(l) ΔH=-Q2 kJ/mol,
2H2S(g)+O2(g)===2S(s)+2H2O(g) ΔH=-Q3 kJ/mol。
判断Q1、Q2、Q3三者大小关系_______>________>_______
高二化学填空题简单题查看答案及解析
-
“除氢气外,烃、肼、甲醇、氨、煤气等液体或气体,均可作燃料电池的燃料”。已知肼燃烧时发生下列反应,N2H4+O2
N2+2H2O。以Pt为电极,以硫酸为电解质溶液组成肼燃料电池,下列关于肼燃料电池的说法中不正确是 )
A. 肼是燃料电池的负极反应物,O2是正极反应物
B. 肼燃料电池的正极反应为 O2 + 2H2O + 4e-= 4OH-
C. 肼燃料电池的负极反应为:N2H4 —4e—=N2↑+4H+
D. 电池工作过程中H+向正极移动,但H+物质的量不变
高二化学单选题困难题查看答案及解析
-
“除氢气外,烃、肼、甲醇、氨、煤气等液体或气体,均可作燃料电池的燃料”。已知肼燃烧时发生下列反应,N2H4+O2
N2+2H2O。以Pt为电极,以硫酸为电解质溶液组成肼燃料电池,下列关于肼燃料电池的说法中不正确是 )
A. 肼是燃料电池的负极反应物,O2是正极反应物
B. 肼燃料电池的正极反应为 O2 + 2H2O + 4e-= 4OH-
C. 肼燃料电池的负极反应为:N2H4 —4e—=N2↑+4H+
D. 电池工作过程中H+向正极移动,但H+物质的量不变
高二化学单选题困难题查看答案及解析